1 . 氮是自然界各种生命活动不可缺少的重要元素。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于______ (填“化学”或“物理)变化;通过雷电作用进行固氮过程中,第一步反应的化学方程式为______ 。
(2)某氮肥厂产生的氨氮废水中的氮元素多以 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:

①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为______ 。
②过程II:在微生物作用下实现 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为______ 。
II.实验室制氨气
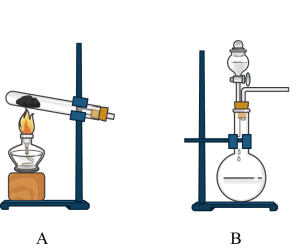
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为______ ;如果选择B装置,则分液漏斗中盛装的物质为______ (填名称):干燥氨气时,可选用的干燥剂为______ ;收集氨气采用______ 法。
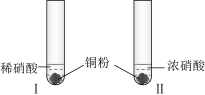
III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
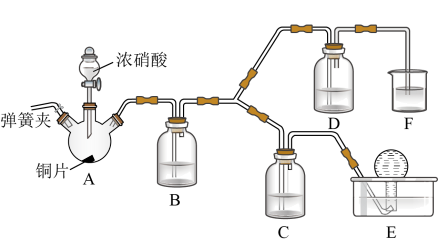
已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为______ 。
②装置A中发生反应的化学方程式为______ ;装置B的作用为______ 。
③装置D中的现象为______ ;C中盛放的试剂为______ 。
I.自然界中氮的循环(如图所示)

(1)豆科植物的根瘤进行固氮的过程属于
(2)某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 的形式存在,设计如下处理流程:
的形式存在,设计如下处理流程:
①过程I:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。加入NaOH溶液时,所发生反应的离子方程式为
②过程II:在微生物作用下实现
 的转化,称为硝化过程。在碱性条件下,
的转化,称为硝化过程。在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为II.实验室制氨气
(3)实验室制备氨气可以选择A或B装置,如果选择A装置,则发生反应的化学方程式为

III.浓硝酸和稀硝酸氧化性强弱比较
(4)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。

已知:NaOH溶液不与NO反应,能与NO2反应。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
您最近一年使用:0次
2 . 下列方案设计、现象和所得出的结论不匹配的是
| 实验目的 | 方案设计 | 实验现象及结论 | |
| A | 检验硫酸厂周边空气中是否含有二氧化硫 | 用注射器多次抽取空气,慢慢注入盛有Ba(NO3)2溶液中,观察实验现象 | 产生白色沉淀,说明空气中含有二氧化硫 |
| B | 除去二氧化碳中混有的二氧化硫气体 | 将混合气体通入过量饱和 NaHCO3溶液中,再通入品红溶液中 | 饱和NaHCO3溶液有气泡产生,品红溶液不褪色,证明已经除尽 |
| C | 检验浓硝酸的性质 | 向发黄的浓硝酸中通入氧气 | 浓硝酸颜色变深,说明浓硝酸易分解 |
| D | 检验浓硫酸的性质 | 向盛有蔗糖的烧杯中滴加适量浓硫酸并用玻璃棒迅速搅拌 | 蔗糖变黑,体积膨胀,产生有刺激性气味的气体,说明浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . “探究与创新能力”是化学的关键能力。下列各项中“操作或现象”能达到预期“实验目的”的是
| 选项 | 实验目的 | 操作或现象 |
| A | 制作简单原电池 | 将铁钉和铜丝连接插入乙醇中即可形成原电池 |
| B | 验证碳能与浓硝酸反应 | 向浓硝酸中加入红热的碳,产生红棕色气体 |
| C | 鉴别溴蒸气和 | 分别通入 溶液中,产生浅黄色沉淀的是溴蒸气 溶液中,产生浅黄色沉淀的是溴蒸气 |
| D | 除去乙烷中的少量乙烯 | 通入足量酸性高锰酸钾溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-07更新
|
350次组卷
|
2卷引用:安徽省合肥市第六中学2021-2022学年高一下学期期末考试化学试题
4 . (1)为了达到表中的实验目的,请选择合适的化学试剂,将其标号填入对应的空格中。
供选择的化学试剂及实验方法:
A.加入烧碱溶液 B.加热至恒重 C.加入足量的铁粉,过滤 D.加稀HNO3和AgNO3溶液,观察现象
(2)工业浓硝酸通常呈黄色,用化学方程式解释:_______ 。
(3)举出氮氧化物对环境的危害(2种):_______ 。
| 实验要求 | 化学试剂 |
| 除去FeCl2溶液中少量FeCl3 | |
| 检验自来水中是否含有Cl- | |
| 除去Na2CO3中少量NaHCO3 | |
| 鉴别MgCl2和AlCl3 |
供选择的化学试剂及实验方法:
A.加入烧碱溶液 B.加热至恒重 C.加入足量的铁粉,过滤 D.加稀HNO3和AgNO3溶液,观察现象
(2)工业浓硝酸通常呈黄色,用化学方程式解释:
(3)举出氮氧化物对环境的危害(2种):
您最近一年使用:0次
名校
5 . 用下列实验装置进行的实验,不能达到相应的实验目的的是


A.利用图1装置进行 的尾气处理 的尾气处理 |
B.利用图2装置和秒表测定反应产生的 的体积及反应时间,计算反应速率 的体积及反应时间,计算反应速率 |
| C.利用图3装置通过观察红棕色气体证明硝酸具有不稳定性 |
| D.利用图4装置加热氯化铵和氢氧化钙的混合物制取氨气 |
您最近一年使用:0次
2023-04-26更新
|
226次组卷
|
2卷引用:河北省唐山市十县一中联盟2022-2023学年高一下学期期中考试化学试题
6 . 下列装置用于进行指定实验时,能达到实验目的的是
甲.装置甲中有红棕色气体说明木炭与浓硝酸发生了反应
乙.用装置乙除去氨气中少量水
丙.挤压装置丙中胶头滴管的水,打开止水夹,左边烧瓶中导管口喷出白色的烟
丁.用装置丁吸收多余的氨气
 |  |  |  |
| 甲 | 乙 | 丙 | 丁 |
乙.用装置乙除去氨气中少量水
丙.挤压装置丙中胶头滴管的水,打开止水夹,左边烧瓶中导管口喷出白色的烟
丁.用装置丁吸收多余的氨气
| A.甲和乙 | B.乙和丙 |
| C.甲和丁 | D.丙和丁 |
您最近一年使用:0次
7 . 利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是

| a中反应 | b中检测试剂及现象 | |
| A | 浓 分解生成 分解生成 | 淀粉-KI溶液变蓝 |
| B | Cu与浓 生成 生成 | 品红溶液褪色 |
| C | 浓NaOH与 溶液生成 溶液生成 | 酚酞溶液变红 |
| D |  与浓盐酸生成 与浓盐酸生成 | NaBr溶液变为橙色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 某学习小组探究稀HNO3、浓HNO3与铜的反应。
(1)试管I中Cu与稀HNO3反应的离子方程式是_______ 。
(2)II中反应的速率比I中的快,原因是_______ 。
(3)针对II中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取II中绿色溶液,分为两等份。
①取一份加入如图所示装置中,_______ (填“操作”和“现象”),证实II中溶解了NO2。_______ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1:HNO3;浓度越稀,溶液中 的数目越少,被还原时,每个
的数目越少,被还原时,每个 从还原剂处获得较多电子的机会
从还原剂处获得较多电子的机会_______ (填“增多”或“减少”),因此被还原为更低价态。
解释2:浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
实验验证浓硝酸能将NO氧化成NO2,实验装置如下图:_______ 。
②C中盛放 和
和_______ 。
③该小组证实推测的合理性所依据的实验现象是_______ 。
装置(尾气处理装置略) | 现象 |
| I中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
| II中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管I中Cu与稀HNO3反应的离子方程式是
(2)II中反应的速率比I中的快,原因是
(3)针对II中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取II中绿色溶液,分为两等份。
①取一份加入如图所示装置中,

(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1:HNO3;浓度越稀,溶液中
 的数目越少,被还原时,每个
的数目越少,被还原时,每个 从还原剂处获得较多电子的机会
从还原剂处获得较多电子的机会解释2:浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
实验验证浓硝酸能将NO氧化成NO2,实验装置如下图:
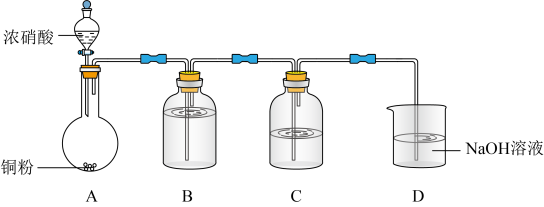
②C中盛放
 和
和③该小组证实推测的合理性所依据的实验现象是
您最近一年使用:0次
9 . 自然界中的氮循环部分过程如图所示,回答下列问题:_______ (任写一种)。
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为_______ 。
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为_______ 。
(3)除反硝化作用外,铵态氮( )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式_______ 。该反应中,当产生0.02mol氮气时,转移电子的物质的量为_______ 。
为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是_______ 。
(5)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈_______ 色,原因是_______ 。
(6)氧化铜和氨气发生反应,化学方程式是_______ 。
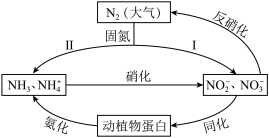
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为
(3)除反硝化作用外,铵态氮(
 )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
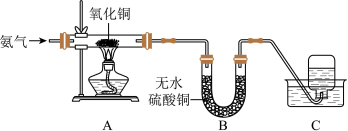
A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是
(5)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈
(6)氧化铜和氨气发生反应,化学方程式是
您最近一年使用:0次
解题方法
10 . 某教师设计了如图装置(省略夹持装置)探究碳与浓硝酸的反应,已知铂丝在实验过程中不参与反应,下列说法错误的是 可与
可与 反应生成物质的量相同的两种盐。
反应生成物质的量相同的两种盐。

 可与
可与 反应生成物质的量相同的两种盐。
反应生成物质的量相同的两种盐。| A.将红热的木炭伸进浓硝酸中可以观察到有红棕色气体产生 |
B.通过三颈烧瓶内的现象可知该反应的化学方程式为 (浓) (浓) |
C.反应结束后,将 溶液加入三颈烧瓶中吸收 溶液加入三颈烧瓶中吸收 ,反应的离子方程式为 ,反应的离子方程式为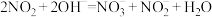 |
D.浓硝酸呈黄色的原因可能是浓硝酸分解生成的 溶解在溶液中 溶解在溶液中 |
您最近一年使用:0次
2023-04-28更新
|
392次组卷
|
3卷引用:陕西省部分名校2022-2023学年高一下学期期中联考化学试题
陕西省部分名校2022-2023学年高一下学期期中联考化学试题辽宁省抚顺市重点高中六校协作体2022-2023学年高一下学期期中考试化学试题(已下线)第18讲 硝酸-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)