解题方法
1 . 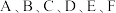 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的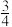 倍,
倍,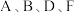 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物. 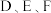 三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
(1)写出题中 所代表的元素名称
所代表的元素名称_________ ,指出 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置_________________________ 。
(2)写出 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为_________________ , 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为_________________ 
_________________ (写出相应离子符号)
(3)可以验证 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)_____________ 。
①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)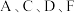 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_____________ 、_____________ ,这两种酸式盐相互反应的离子方程式为___________________ 。
(5) 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为________________________________ 。
(6)写出 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:_____________________ 。
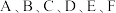 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的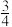 倍,
倍,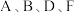 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.  三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:(1)写出题中
 所代表的元素名称
所代表的元素名称 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置(2)写出
 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为
(3)可以验证
 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)
 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为(5)
 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为(6)写出
 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:
您最近一年使用:0次
名校
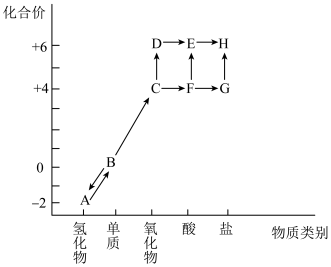
2 . “价—类”二维图是预测物质性质的重要思维工具。下图是硫元素的常见化合价与部分物质类别的对应关系。___________ 氧化物。
(2)A 中硫元素处于最低化合价,具有___________ 性,预测 A 溶液久置于空气会出现的现象为___________ ,写出发生反应的化学方程式___________ 。
(3)试管内壁附着的单质B可用热的NaOH溶液洗涤,反应过程中仅生成G、水以及另一种钠盐,上述反应过程中生成的“另一种钠盐”的化学式为___________ 。
(4)检验某溶液中是否含有 的方法为
的方法为___________ 。
(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有CO2和SO2可选择以下试剂进行实验:①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水
合理的顺序为___________ :
___________→___________→ ___________→___________(填序号)。
(2)A 中硫元素处于最低化合价,具有
(3)试管内壁附着的单质B可用热的NaOH溶液洗涤,反应过程中仅生成G、水以及另一种钠盐,上述反应过程中生成的“另一种钠盐”的化学式为
(4)检验某溶液中是否含有
 的方法为
的方法为(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有CO2和SO2可选择以下试剂进行实验:①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水
合理的顺序为
___________→___________→ ___________→___________(填序号)。
您最近一年使用:0次
名校
解题方法
3 . 下列指定反应的离子方程式正确的是
A.钠与水的反应: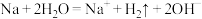 |
B.用 溶液吸收足量的 溶液吸收足量的 气体: 气体: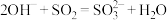 |
C.向 溶液中加过量的 溶液中加过量的 溶液并加热: 溶液并加热: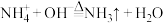 |
D. 和 和 溶液共热的反应: 溶液共热的反应: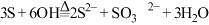 |
您最近一年使用:0次
4 . 下列有关物质应用的说法错误的是
A. 可用作食品添加剂 可用作食品添加剂 |
B. 可用于鉴别溴水和碘水 可用于鉴别溴水和碘水 |
C.室温时,可用 溶液来清洗试管壁的硫黄 溶液来清洗试管壁的硫黄 |
D. 可除去污水中的 可除去污水中的 |
您最近一年使用:0次
名校
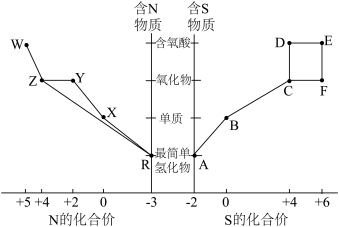
5 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题: 反应的化学方程式
反应的化学方程式______
(2)下列有关图中所示含N、S物质的叙述,正确的是______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠( ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应
(3)写出B与氢氧化钠溶液反应的离子反应方程式______
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是______ 。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: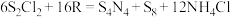 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有______ ,该反应每生成 转移电子
转移电子______ mol。
 反应的化学方程式
反应的化学方程式(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(
 ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应(3)写出B与氢氧化钠溶液反应的离子反应方程式
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: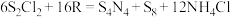 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近一年使用:0次
名校
6 . 部分含硫物质的类别与相应化合价及部分物质间转化关系如图。下列说法错误的是
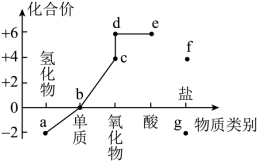
| A.c可以使滴有酚酞的NaOH溶液褪色,适量c可做食品添加剂 |
| B.b附着在试管壁上可以用热的浓NaOH溶液洗涤 |
| C.a在O2中燃烧可以生成d |
| D.e的浓溶液长时间暴露在空气中,质量增大,质量分数减小 |
您最近一年使用:0次
2024-04-17更新
|
278次组卷
|
2卷引用:广东省肇庆市四会中学、广州市广信中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
7 . 请按要求书写下列方程式。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为___________ (用化学方程式表示)。
(2)实验室中可利用 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为___________ 。
(3)写出氨气实验室制法的化学方程式___________ 。
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:___________ 。
(5)铜与稀硝酸的离子方程式为:___________ 。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为
(2)实验室中可利用
 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为(3)写出氨气实验室制法的化学方程式
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(5)铜与稀硝酸的离子方程式为:
您最近一年使用:0次
名校
解题方法
8 . 含硫物质的价类二维图及部分物质间转化关系如图,下列说法错误的是
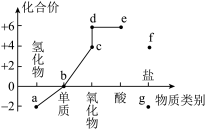
| A.工业制硫酸时将d通入水中得到浓硫酸 |
| B.b附着在试管壁上可以用热的浓NaOH溶液洗涤 |
| C.c可以使滴有酚酞的NaOH溶液褪色,适量c可做食品添加剂 |
| D.e的浓溶液长时间暴露在空气中,质量增大,质量分数减小 |
您最近一年使用:0次
名校
9 . 部分含硫物质的类别与相应化合价及部分物质间转化关系如图。下列说法正确的是
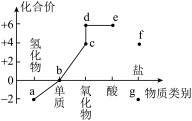

A.a在 中燃烧可以生成d 中燃烧可以生成d |
B.b附着在试管壁上可以用热的浓 溶液洗涤 溶液洗涤 |
C.c可以使滴有酚酞的 溶液褪色,利用了c的漂白性 溶液褪色,利用了c的漂白性 |
| D.e的浓溶液长时间暴露在空气中质量分数减小,说明e具有挥发性 |
您最近一年使用:0次
名校
解题方法
10 . 为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分,请回答以下问题:
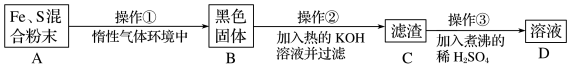
(1)混合粉末A中硫粉过量的原因是________ 。
(2)操作①使用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明________ 。
(3)操作②的化学方程式是_______ ;为了实现操作②的目的,也可改用加入_______ 。
(4)操作③稀 煮沸的目的是
煮沸的目的是________ 。

(1)混合粉末A中硫粉过量的原因是
(2)操作①使用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明
(3)操作②的化学方程式是
(4)操作③稀
 煮沸的目的是
煮沸的目的是
您最近一年使用:0次



