名校
解题方法
1 . 一些物质的分类如图,根据所学知识填空。

(1)A组物质中属于碱性氧化物的电解质是________ 。A组物质中Na2O2具有强氧化性,和A组中CO2一样SO2也为非电解质,但SO2有还原性,写出Na2O2和SO2反应的化学方程式________ 。
(2)B组中两种金属均可在氯气中燃烧,l个Cl2与足量金属铁粉充分反应生成+3价的三氯化铁,理论上转移电子数为_______ 个。
(3)D组中两种单质均能与H2O反应,写出熔点低的那种金属与H2O反应的方程式________ (属于离子反应的写离子方程式)。
(4)写出A组物质中属于酸式盐的物质在熔融状态下的电离方程式___________ 。
(5)向少量的Ba(OH)2溶液中逐滴加入稀硫酸可生成硫酸钡,其反应的离子方程式为:Ba2++2OH-+2H++ =BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
=BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
(6)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种。其中已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。则NaH2PO2属于___________ (填“正盐”或“酸式盐”)。

(1)A组物质中属于碱性氧化物的电解质是
(2)B组中两种金属均可在氯气中燃烧,l个Cl2与足量金属铁粉充分反应生成+3价的三氯化铁,理论上转移电子数为
(3)D组中两种单质均能与H2O反应,写出熔点低的那种金属与H2O反应的方程式
(4)写出A组物质中属于酸式盐的物质在熔融状态下的电离方程式
(5)向少量的Ba(OH)2溶液中逐滴加入稀硫酸可生成硫酸钡,其反应的离子方程式为:Ba2++2OH-+2H++
 =BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。
=BaSO4↓+2H2O。下列三种情况下,离子方程式与题干中相同的是___________(填序号)。| A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性 |
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至 恰好完全沉淀 恰好完全沉淀 |
| C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 |
| D.向少量的稀硫酸溶液中逐滴加入Ba(OH)2至溶液显中性 |
您最近一年使用:0次
解题方法
2 . 工厂烟气中含有的 ,直接排放会污染空气。
,直接排放会污染空气。
(1)从元素价态、物质类别的角度,预测并验证 的部分化学性质。
的部分化学性质。
①从硫元素的价态角度分析,预测 既有氧化性又有还原性。将
既有氧化性又有还原性。将 通入酸性高锰酸钾溶液中,紫色褪去,生成了
通入酸性高锰酸钾溶液中,紫色褪去,生成了 ,反应中体现了
,反应中体现了 的
的___________ 性。 还能与
还能与 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为___________ ,该反应中,作氧化剂的是___________ (填化学式)。
②从物质类别角度分析, 属于酸性氧化物,类似
属于酸性氧化物,类似 ,
, 和过量
和过量 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(2)工业上燃煤时常在煤炭中加入石灰石,从源头上减少 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应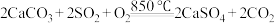 。
。
①通入的气体中氧气的浓度偏低时,产生的CO与 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为___________ ,被氧化的元素为___________ (填元素符号)。
②从物质类别角度分析,上述涉及的物质中,既属于电解质又属于盐的是___________ 。
 ,直接排放会污染空气。
,直接排放会污染空气。(1)从元素价态、物质类别的角度,预测并验证
 的部分化学性质。
的部分化学性质。①从硫元素的价态角度分析,预测
 既有氧化性又有还原性。将
既有氧化性又有还原性。将 通入酸性高锰酸钾溶液中,紫色褪去,生成了
通入酸性高锰酸钾溶液中,紫色褪去,生成了 ,反应中体现了
,反应中体现了 的
的 还能与
还能与 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为②从物质类别角度分析,
 属于酸性氧化物,类似
属于酸性氧化物,类似 ,
, 和过量
和过量 溶液反应的离子方程式为
溶液反应的离子方程式为(2)工业上燃煤时常在煤炭中加入石灰石,从源头上减少
 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应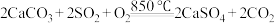 。
。①通入的气体中氧气的浓度偏低时,产生的CO与
 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为②从物质类别角度分析,上述涉及的物质中,既属于电解质又属于盐的是
您最近一年使用:0次
2023-11-23更新
|
313次组卷
|
4卷引用:广东省茂名市七迳中学2023-2024学年高一上学期期中考试化学试卷
广东省茂名市七迳中学2023-2024学年高一上学期期中考试化学试卷广东省湛江市2023-2024学年高一上学期11月期中考试化学试题辽宁省葫芦岛市协作校2023-2024学年高一上学期第二次考试化学试题(已下线)第01讲 硫及其化合物-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)
名校
3 . 利用“价一类”二维图是研究、推测元素的单质、化合物化学性质的重要学习手段。如下图是硫元素的“价-类”二维图,请回答下列问题:

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
(2)将X的溶液与Y混合反应,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)Z的浓溶液与S单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为___________ 。
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________(填字母)。
(5)Z的浓溶液具有强的氧化性、吸水性和脱水性,常可作干燥剂,则下列气体可用乙干燥的是___________
(6)已知Na2SO3能被K2X2O7氧化为Na2SO4,则24mL0.05mol·L-1的Na2SO3溶液与20mL0.02mol·L-1的K2X2O7溶液恰好反应时,X元素在还原产物中的化合价为___________ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X的溶液与Y混合反应,该反应中氧化剂与还原剂的物质的量之比为
(3)Z的浓溶液与S单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________(填字母)。
| A.Na2S+S | B.Na2SO3+S | C.SO2+Na2SO4 | D.Na2SO3+Na2SO4 |
| A.X | B.Y | C.氨气 | D.HI |
您最近一年使用:0次
2023-05-16更新
|
501次组卷
|
3卷引用:广东省广州市真光中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
4 . 写出下列方程式
(1)将SO2通入足量的澄清石灰水中的化学方程式:_________________
(2)过量铁粉与稀硝酸反应的离子方程式:________________________
(3)工业上制备粗硅的化学方程式:_____________
(4)焦亚硫酸钠(Na2S2O5)可用作食品的抗氧化剂,在测定某葡萄酒中Na2S2O5残留量时,用碘溶液(I2)进行滴定,已知氧化产物为SO ,该反应的离子方程式:
,该反应的离子方程式:______________________
(1)将SO2通入足量的澄清石灰水中的化学方程式:
(2)过量铁粉与稀硝酸反应的离子方程式:
(3)工业上制备粗硅的化学方程式:
(4)焦亚硫酸钠(Na2S2O5)可用作食品的抗氧化剂,在测定某葡萄酒中Na2S2O5残留量时,用碘溶液(I2)进行滴定,已知氧化产物为SO
 ,该反应的离子方程式:
,该反应的离子方程式:
您最近一年使用:0次
名校
5 . 按照要求书写离子方程式
(1)把二氧化硫通入酸性高锰酸钾溶液中:___________
(2)酸性环境下,把双氧水加入硫酸亚铁溶液中:___________
(3)用高锰酸钾和浓盐酸制备氯气:___________
(4)实验室制备氯气:___________
(5)稀硝酸和铜反应:___________
(1)把二氧化硫通入酸性高锰酸钾溶液中:
(2)酸性环境下,把双氧水加入硫酸亚铁溶液中:
(3)用高锰酸钾和浓盐酸制备氯气:
(4)实验室制备氯气:
(5)稀硝酸和铜反应:
您最近一年使用:0次
名校
6 . 元素的“价—类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价—类”二维图。根据图示回答下列问题:

(1)X在水中的电离方程式为_______ 。
(2)根据“价—类”二维图预测, 与酸性
与酸性 溶液反应表现
溶液反应表现_______ 性,反应的离子方程式为_______ 。
(3)下列物质与 反应,
反应, 能表现出氧化性的是
能表现出氧化性的是_______ (填序号)
a.NaOH溶液 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(4) 与
与 类似,
类似, 与足量石灰水反应的离子方程式为
与足量石灰水反应的离子方程式为_______ 。
(5)下列事实能说明硫的非金属性弱于氯的是_______ (填序号)。
a.稳定性:
b.酸性:
c.酸性: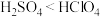
d.往氢硫酸溶液中通入 ,产生淡黄色沉淀:
,产生淡黄色沉淀:
(6)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是_______ (填字母)。请写出相应的化学方程式_______ 。
A. B.
B. C.
C. D.
D.

(1)X在水中的电离方程式为
(2)根据“价—类”二维图预测,
 与酸性
与酸性 溶液反应表现
溶液反应表现(3)下列物质与
 反应,
反应, 能表现出氧化性的是
能表现出氧化性的是a.NaOH溶液 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(4)
 与
与 类似,
类似, 与足量石灰水反应的离子方程式为
与足量石灰水反应的离子方程式为(5)下列事实能说明硫的非金属性弱于氯的是
a.稳定性:

b.酸性:

c.酸性:
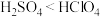
d.往氢硫酸溶液中通入
 ,产生淡黄色沉淀:
,产生淡黄色沉淀:
(6)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
名校
解题方法
7 . 以硫铁矿(主要成分为 还有少量CuS、
还有少量CuS、 等杂质)为原料制备绿矾晶体(
等杂质)为原料制备绿矾晶体( )的工艺流程如下:
)的工艺流程如下:
(1)烟气中的 会污染环境,可用足量氨水吸收,写出该反应的离子方程式
会污染环境,可用足量氨水吸收,写出该反应的离子方程式_______ 。
(2)仅用一种试剂检验溶液中金属阳离子,则所用试剂及现象分别为_______ 、_______ 。
(3)写出由滤液得到绿矾晶体实验操作方法为:在隔绝空气的条件下_______ 、_______ 、过滤,洗涤,干燥。
(4)细菌脱硫法是用氧化亚铁硫杆菌做对硫铁矿进行催化脱硫,同时得到 溶液。其总反应为:
溶液。其总反应为: ,过程如下图所示:
,过程如下图所示:

写出过程Ⅱ反应的离子方程式_______ 。
(5)大量排放 容易造成酸雨等环境问题,工业上可用双脱硫法处理废气,过程如下图所示,其中可循环使用的试剂是
容易造成酸雨等环境问题,工业上可用双脱硫法处理废气,过程如下图所示,其中可循环使用的试剂是_______ ,写出双碱法脱硫法的总反应方程式:_______ 。

 还有少量CuS、
还有少量CuS、 等杂质)为原料制备绿矾晶体(
等杂质)为原料制备绿矾晶体( )的工艺流程如下:
)的工艺流程如下:(1)烟气中的
 会污染环境,可用足量氨水吸收,写出该反应的离子方程式
会污染环境,可用足量氨水吸收,写出该反应的离子方程式(2)仅用一种试剂检验溶液中金属阳离子,则所用试剂及现象分别为
(3)写出由滤液得到绿矾晶体实验操作方法为:在隔绝空气的条件下
(4)细菌脱硫法是用氧化亚铁硫杆菌做对硫铁矿进行催化脱硫,同时得到
 溶液。其总反应为:
溶液。其总反应为: ,过程如下图所示:
,过程如下图所示:
写出过程Ⅱ反应的离子方程式
(5)大量排放
 容易造成酸雨等环境问题,工业上可用双脱硫法处理废气,过程如下图所示,其中可循环使用的试剂是
容易造成酸雨等环境问题,工业上可用双脱硫法处理废气,过程如下图所示,其中可循环使用的试剂是
您最近一年使用:0次
2022-05-16更新
|
369次组卷
|
2卷引用:广东省广州市广州中学2021-2022学年高一下学期期中考试化学试题
名校
8 . 研究大气中含硫化合物(主要是H2S和SO2)的转化具有重要意义。
(1)H2S资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。

①电极b为电池的_______ 极,电极a上发生的电极反应为:_______ 。
②每17gH2S参与反应,正极消耗的O2为_______ mol。
(2)低浓度SO2废气的处理是工业难题,目前常用的方法如下:

①Na2SO3溶液吸收SO2的化学方程式是_______ 。
②如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是_______ 。
A.Na2SO3 B.Na2S C.溴水 D.酸性KMnO4
(1)H2S资源化利用途径之一是回收能量并得到单质硫,如图为质子膜(该膜的作用就是只容许固体电解质中的H+自由通过)H2S燃料电池的示意图。

①电极b为电池的
②每17gH2S参与反应,正极消耗的O2为
(2)低浓度SO2废气的处理是工业难题,目前常用的方法如下:

①Na2SO3溶液吸收SO2的化学方程式是
②如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是
A.Na2SO3 B.Na2S C.溴水 D.酸性KMnO4
您最近一年使用:0次
名校
9 . I.研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。以下是硫元素形成物质的价类二维图及含硫物质相互转化的部分信息。
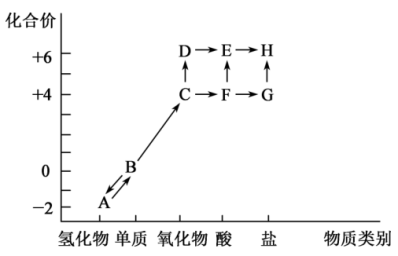
(1)A的化学式是_______ ;G既是一种钠盐,也是酸式盐,它的电离方程式是_______ 。
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的化学方程式是_______ 。
(3)检验H中阴离子的实验操作及现象是_______ 。
II.燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
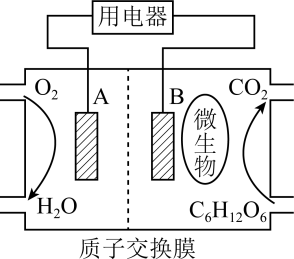
(4)A为生物燃料电池的_______ (填“正”或“负”)极。
(5)正极的电极反应式为_______ 。
(6)放电过程中,H+由_______ 极区向_______ 极区迁移(填“正”或“负”)。

(1)A的化学式是
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的化学方程式是
(3)检验H中阴离子的实验操作及现象是
II.燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

(4)A为生物燃料电池的
(5)正极的电极反应式为
(6)放电过程中,H+由
您最近一年使用:0次



