名校
解题方法
1 . 某工厂每天燃烧含硫质量分数为0.64%的煤100吨,如果煤中的硫元素全部转化为 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为_______ 吨。
 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
您最近一年使用:0次
名校
解题方法
2 . 已知:SO2+I2+2H2O=SO +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
(1)所用碘水溶液的物质的量浓度_____ mol/L。
(2)空气样品中SO2的含量_____ mg/L。
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量_____ (填“合格”或“不合格”)。
 +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:(1)所用碘水溶液的物质的量浓度
(2)空气样品中SO2的含量
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量
您最近一年使用:0次
3 . 将一定量 通入
通入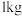 质量分数为
质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:
(1) 溶液中
溶液中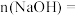
___________  。
。
(2)已知混合溶液中 ,则混合溶液中
,则混合溶液中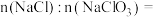
___________ 。
(3)所通 在标准状况下的体积为
在标准状况下的体积为___________ L。
 通入
通入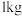 质量分数为
质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:(1)
 溶液中
溶液中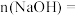
 。
。(2)已知混合溶液中
 ,则混合溶液中
,则混合溶液中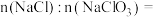
(3)所通
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2022-05-04更新
|
901次组卷
|
4卷引用:浙江省杭州地区(含周边)重点中学2021-2022学年高一下学期期中考试化学试题
4 . 按要求填空。
(1) 固体与水完全反应时的化学方程式为
固体与水完全反应时的化学方程式为_______ ,该反应转移的电子数为_______ 。
(2)工业上由辉铜矿生产铜的主要反应为: ,该反应中被还原的元素是
,该反应中被还原的元素是_______ (填元素符号)。该反应中产生的 尾气可用NaOH溶液吸收,若用1L1mol/L的NaOH溶液恰好吸收标准状况下
尾气可用NaOH溶液吸收,若用1L1mol/L的NaOH溶液恰好吸收标准状况下 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(1)
 固体与水完全反应时的化学方程式为
固体与水完全反应时的化学方程式为(2)工业上由辉铜矿生产铜的主要反应为:
 ,该反应中被还原的元素是
,该反应中被还原的元素是 尾气可用NaOH溶液吸收,若用1L1mol/L的NaOH溶液恰好吸收标准状况下
尾气可用NaOH溶液吸收,若用1L1mol/L的NaOH溶液恰好吸收标准状况下 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
2018·浙江温州·二模
5 . 一定量的SO2通入到含0.16mol NaOH的溶液中,充分反应后生成的Na2SO3和 NaHSO3物质的量之比为3:2。再向反应后溶液中通入Cl2使硫元素全部转化为SO42-。
请计算:
(1)SO2的质量为___________________ g。
(2)通入Cl2的物质的量至少为___________________ mol。
请计算:
(1)SO2的质量为
(2)通入Cl2的物质的量至少为
您最近一年使用:0次
2018-03-10更新
|
615次组卷
|
6卷引用:【新东方】高中化学156
9-10高一下·上海·期中
6 . 接触法制硫酸排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前设法进行综合利用。某硫酸厂每天排放的1万米3(已换算成标准状况)尾气中含0.2%(体积百分数)的SO2。
(1)若用生石灰及氧气处理后,假设硫元素不损失,理论上可得到_______ 千克生石膏?
(2)若用氨水处理,最少需要标况下的氨气_______ 升?最多需要标准状况下的氨气_____ 升?
(1)若用生石灰及氧气处理后,假设硫元素不损失,理论上可得到
(2)若用氨水处理,最少需要标况下的氨气
您最近一年使用:0次



