解题方法
1 . 实验室用如图装置制备 并验证相关物质的性质。下列有关试剂A说法正确的是
并验证相关物质的性质。下列有关试剂A说法正确的是
 并验证相关物质的性质。下列有关试剂A说法正确的是
并验证相关物质的性质。下列有关试剂A说法正确的是
A.若为 水溶液,可验证 水溶液,可验证 的还原性 的还原性 |
B.若为 溶液,则发生氧化还原反应 溶液,则发生氧化还原反应 |
| C.若为溴水,观察到溶液出现淡黄色浑浊 |
D.若为含 和AgCl的浊液,可证明 和AgCl的浊液,可证明 : :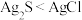 |
您最近一年使用:0次
2 . 微型实验药品用量少,绿色环保。如图所示为探究 性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法不正确的是
性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法不正确的是
 性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法不正确的是
性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法不正确的是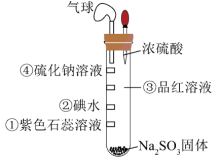
A.滤纸①变红,体现了 酸性氧化物的性质 酸性氧化物的性质 |
B.滤纸②、③褪色均证明 具有还原性 具有还原性 |
C.滤纸④上有黄色固体生成,证明 具有氧化性 具有氧化性 |
D.实验中可用 固体代替 固体代替 固体 固体 |
您最近一年使用:0次
名校
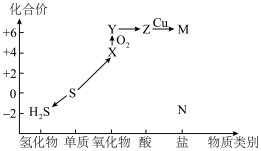
3 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系: 的电子式为
的电子式为________ ;将 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为________ 。
(2)S粉与热的Z浓溶液反应可转化为________ ,反应的化学方程式为________ 。
(3)配平下列反应:_____
____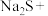 ____
____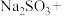 ____
____ ____
____ ____
____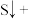 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。________ 。
②C的作用是________ ,装置D中试管口放置的棉花应浸有一种液体,这种液体是________ 。
 的电子式为
的电子式为 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为(2)S粉与热的Z浓溶液反应可转化为
(3)配平下列反应:
____
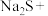 ____
____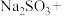 ____
____ ____
____ ____
____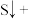 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
| A.X能使溴水褪色,证明X有漂白性 | B.将X通入 溶液中有白色沉淀生成 溶液中有白色沉淀生成 |
C.硫在过量的 中燃烧可以生成Y 中燃烧可以生成Y | D.若N为钠盐,则N与Z的稀溶液反应可生成 |
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。

②C的作用是
您最近一年使用:0次
名校
解题方法
4 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。已知: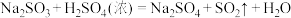 ,下列说法错误的是
,下列说法错误的是
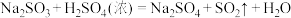 ,下列说法错误的是
,下列说法错误的是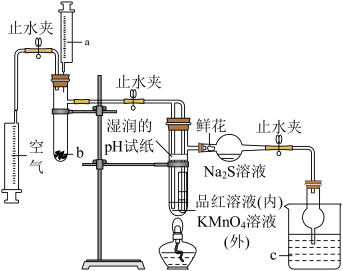
A.a、b、c中盛装物质可以分别为浓硫酸、 固体、 固体、 溶液 溶液 |
B.实验时,湿润的pH试纸、鲜花、品红溶液、酸性 溶液均褪色, 溶液均褪色, 溶液中出现淡黄色沉淀 溶液中出现淡黄色沉淀 |
C.此设计可证明 水溶液呈酸性, 水溶液呈酸性, 具有氧化性、还原性、漂白性 具有氧化性、还原性、漂白性 |
D.点燃酒精灯加热,可证明 使品红溶液褪色具有可逆性,使酸性 使品红溶液褪色具有可逆性,使酸性 溶液褪色不具有可逆性 溶液褪色不具有可逆性 |
您最近一年使用:0次
2024-02-02更新
|
468次组卷
|
3卷引用:河南省南阳市2023-2024学年高一上学期1月期末化学试题
河南省南阳市2023-2024学年高一上学期1月期末化学试题(已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题
5 . 为探究硫酸亚铁的分解产物,将硫酸亚铁装入如图所示的装置a中,打开 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管中残留固体为红色粉末。下列说法中错误的是
,加热。实验后反应管中残留固体为红色粉末。下列说法中错误的是
 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管中残留固体为红色粉末。下列说法中错误的是
,加热。实验后反应管中残留固体为红色粉末。下列说法中错误的是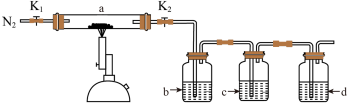
A.反应管中残留的红色粉末是 |
B.若装置b中的试剂为 溶液,反应中有白色沉淀生成,则可以证明分解产物中有 溶液,反应中有白色沉淀生成,则可以证明分解产物中有 生成 生成 |
C.装置c中的试剂可以是品红溶液,作用是检验混合气体中有无 生成 生成 |
| D.d为尾气处理装置 |
您最近一年使用:0次
名校
解题方法
6 . 某小组同学探究SO2与新制Cu(OH)2悬浊液反应的实验装置图如下所示:
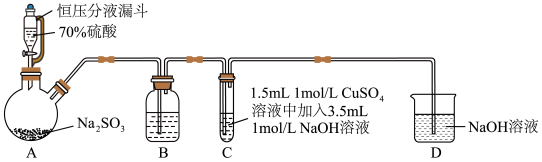
| A.配制70%的硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管 |
| B.装置B的作用是监控SO2流速,其中试剂可以用饱和 NaHSO3溶液 |
| C.反应开始时C中出现砖红色沉淀(Cu2O),氧化剂和还原剂的物质的量之比为2:1 |
| D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl2溶液,有白色沉淀生成,证明反应中SO2作还原剂 |
您最近一年使用:0次
名校
7 .  和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是

 和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
A.①中品红褪色证明 有氧化性 有氧化性 |
| B.②中的试剂X应该是浓硫酸 |
| C.③中的试剂Y应该是NaOH溶液 |
D.②中颜色变浅,但不消失,且③中出现浑浊,即可证明气体中有 |
您最近一年使用:0次
2023-07-17更新
|
281次组卷
|
5卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题
黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题新疆石河子第一中学2023-2024学年高二上学期9月月考化学试题(已下线)第01讲 硫及其化合物-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)福建省福清第一中学2023-2024学年高一下学期开学适应性练习化学试题(已下线)5.1.2 硫酸
解题方法
8 . 为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。实验装置如图所示:(固定装置已略去)
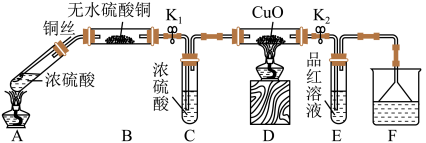
下列说法不正确的是

下列说法不正确的是
| A.F烧杯中的溶液通常是氢氧化钠溶液 |
| B.实验过程中,D装置中黑色固体颜色无变化,E中溶液褪色,能证明浓硫酸中硫元素的氧化性强于氢元素 |
| C.不放入铜丝进行实验,观察无水硫酸铜是否变蓝,能说明浓硫酸中的水是否影响B装置现象的判断 |
| D.将57.6g的Cu片加入50mL18mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量等于0.45mol |
您最近一年使用:0次
9 . 利用下图装置制取 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是
 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是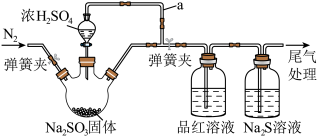
| A.导管a的作用是保证浓硫酸顺利滴下 |
B.品红溶液褪色,说明 可能具有漂白性 可能具有漂白性 |
C. 溶液中出现浑浊,证明 溶液中出现浑浊,证明 具有氧化性 具有氧化性 |
D.三颈烧瓶内反应开始前通 与反应结束后通 与反应结束后通 目的相同 目的相同 |
您最近一年使用:0次
名校
解题方法
10 . 二氧化硫是中学化学的重要物质。某化学兴趣小组设计如图实验探究SO2的性质。
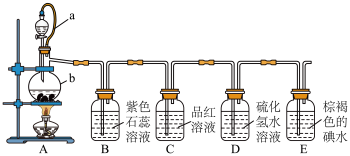
(1)已知b中放入的是纯铜片,写出装置A中的化学方程式_______ 。
(2)同学甲认为该套装置存在一个明显缺陷,其理由是_______ 。
(3)关于该探究实验,下列说法错误的是_______ 。
①装置A中,橡皮管a的作用是使分液漏斗中的液体能顺利流下
②装置B中,紫色溶液变红,证明二氧化硫是酸性氧化物
③装置C中,品红溶液褪色;证明二氧化硫具有漂白性
④装置D中溶液变浑浊,生成了硫单质,证明SO2具有还原性
(4)装置E中溶液褪色,发生的反应离子方程式是_______ 。
(5)实验过程中,同学乙观察到E中溶液在完全褪色后开始逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究(实验中溶液的体积及溶质的物质的量浓度均相同)。
【实验装置】
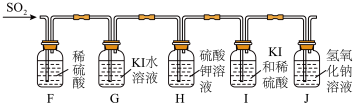
【实验现象】一段时间后,F、H中无明显现象,I中比G中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为_______ 。该反应中的催化剂是_______ (填写序号)。
①H⁺ ②I⁻ ③H⁺、I⁻ ④K⁺、H⁺ ⑤K⁺、I⁻

(1)已知b中放入的是纯铜片,写出装置A中的化学方程式
(2)同学甲认为该套装置存在一个明显缺陷,其理由是
(3)关于该探究实验,下列说法错误的是
①装置A中,橡皮管a的作用是使分液漏斗中的液体能顺利流下
②装置B中,紫色溶液变红,证明二氧化硫是酸性氧化物
③装置C中,品红溶液褪色;证明二氧化硫具有漂白性
④装置D中溶液变浑浊,生成了硫单质,证明SO2具有还原性
(4)装置E中溶液褪色,发生的反应离子方程式是
(5)实验过程中,同学乙观察到E中溶液在完全褪色后开始逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究(实验中溶液的体积及溶质的物质的量浓度均相同)。
【实验装置】

【实验现象】一段时间后,F、H中无明显现象,I中比G中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为
①H⁺ ②I⁻ ③H⁺、I⁻ ④K⁺、H⁺ ⑤K⁺、I⁻
您最近一年使用:0次



