名校
解题方法
1 . 下列实验能达到实验目的的是
|
|
|
|
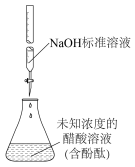
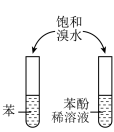
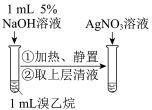
| A.测定醋酸的浓度 | B.实验室制备并收集SO2 | C.证明羟基使苯环活化 | D.检验溴乙烷的水解产物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-02更新
|
590次组卷
|
4卷引用:2024届东北三省三校高三下学期第二次联合模拟考试理综重组卷-高中化学
解题方法
2 . 如图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。
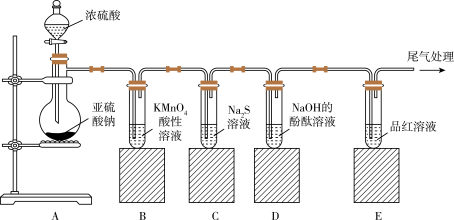
(1)装置A中装浓硫酸的仪器名称:_____ 。
(2)装置B中的离子方程式是_____ ,该反应说明SO2具有_____ 性。
(3)装置C中的实验现象是_____ 。
(4)装置E中的现象是_____ ,尾气处理所用的试剂是_____ 。
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体,可以选择下图洗气装置设计实验,洗气装置中的溶液顺序_____ 。
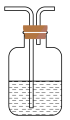
洗气装置中的溶液是: A.浓硫酸、B.氢氧化钠溶液、C.硫酸铜溶液、D.品红溶液、E.澄清石灰水、F.酸性高锰酸钾溶液、G.碳酸氢钠溶液。

(1)装置A中装浓硫酸的仪器名称:
(2)装置B中的离子方程式是
(3)装置C中的实验现象是
(4)装置E中的现象是
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体,可以选择下图洗气装置设计实验,洗气装置中的溶液顺序

洗气装置中的溶液是: A.浓硫酸、B.氢氧化钠溶液、C.硫酸铜溶液、D.品红溶液、E.澄清石灰水、F.酸性高锰酸钾溶液、G.碳酸氢钠溶液。
您最近一年使用:0次
名校
解题方法
3 . 微型实验药品用量少,绿色环保。如图所示为探究 性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法正确的是
性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法正确的是
 性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法正确的是
性质的微型实验,滤纸①~④分别浸泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法正确的是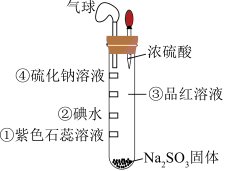
A.滤纸①先变红后褪色,体现了 具有漂白性和酸性氧化物的性质 具有漂白性和酸性氧化物的性质 |
B.滤纸②、③褪色均证明 具有还原性 具有还原性 |
C.滤纸④上有黄色固体生成,证明 具有氧化性 具有氧化性 |
D.若滤纸④上析出了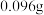 固体,则在滤纸④上发生的反应转移了 固体,则在滤纸④上发生的反应转移了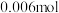 电子 电子 |
您最近一年使用:0次
2024-02-24更新
|
1458次组卷
|
13卷引用:云南师范大学附属中学2023-2024学年高一下学期第一次月考化学试题
云南师范大学附属中学2023-2024学年高一下学期第一次月考化学试题云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题广东省2024届高三下学期2月份大联考 化学试题(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)宁夏石嘴山市平罗中学2023-2024学年高一下学期4月月考化学试题河北省廊坊市2023-2024学年高一下学期3月月考化学试题广东省高州市2024届高三2月份大联考化学试题广东省惠州市实验中学2023-2024学年高一下学期4月月考化学试题湖北省武汉市第三中学2023-2024学年高一下学期3月月考化学试卷广东省惠州市第一中学2023-2024学年高二下学期4月月考化学试题广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷广东省梅州市梅江区梅州中学2024届高三下学期5月模拟考试化学试题
4 . 实验室利用SO2合成硫酰氯(SO2Cl2),并对H2SO3和HClO的酸性强弱进行探究。硫酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应,制取少量的SO2Cl2(SO2(g)+Cl2(g)=SO2Cl2(l),该反应放热。装置如图所示(部分夹持装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应,并产生白雾。回答下列问题。

(1)甲装置用于制SO2,则下列试剂组合中最合适的是_______。(填序号)
(2)导管a的作用是_______ ,装置乙和丁中可以使用同一种试剂,该试剂为_______ 。仪器b中盛放的试剂的作用是_______ 。
(3)若反应中消耗的氯气体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的硫酰氯4.05 g,则硫酰氯的产率为_______ (保留两位有效数字)。
(4)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→_______ 。能证明H2SO3的酸性强于HClO的实验现象为_______ 。


(1)甲装置用于制SO2,则下列试剂组合中最合适的是_______。(填序号)
| A.18.4 mol·L-1的硫酸和Al | B.5 mol·L-1的硝酸和Na2SO3固体 |
| C.10 mol·L-1的硫酸和Na2SO3固体 | D.0.5 mol·L-1的硫酸和Na2SO3固体 |
(3)若反应中消耗的氯气体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的硫酰氯4.05 g,则硫酰氯的产率为
(4)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→

您最近一年使用:0次
2023-02-17更新
|
2074次组卷
|
8卷引用:云南省昆明市第一中学2022-2023学年高二下学期期中考试化学试题
解题方法
5 . 如图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。
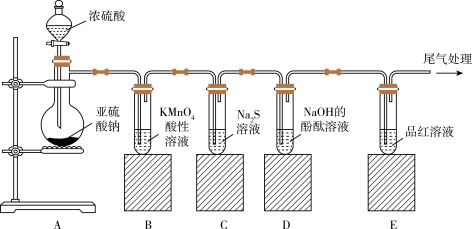
(1)装置A中装浓硫酸的仪器名称:______ 。
(2)装置B中的离子方程式是_____ ,该反应说明SO2具有_____ 性。
(3)装置C中的实验现象是_____ ,该实验现象说明SO2具有_____ 性。
(4)装置E中的现象是_____ ,尾气处理所用的试剂是____ 。
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。可以选择如图洗气装置设计实验:
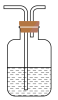
洗气装置中的溶液是。
A.浓硫酸 B.氢氧化钠溶液 C.硫酸铜溶液 D.品红溶液 E.澄清石灰水 F.酸性高锰酸钾溶液 G.碳酸氢钠溶液
为达到实验目的,按气流方向从左到右,上述装置所装试剂的连接顺序是_____ (用字母表示,所给试剂可以重复使用,有些试剂也可以不用)。

(1)装置A中装浓硫酸的仪器名称:
(2)装置B中的离子方程式是
(3)装置C中的实验现象是
(4)装置E中的现象是
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。可以选择如图洗气装置设计实验:

洗气装置中的溶液是。
A.浓硫酸 B.氢氧化钠溶液 C.硫酸铜溶液 D.品红溶液 E.澄清石灰水 F.酸性高锰酸钾溶液 G.碳酸氢钠溶液
为达到实验目的,按气流方向从左到右,上述装置所装试剂的连接顺序是
您最近一年使用:0次
名校
解题方法
6 . 学习小组在实验室中利用下图所示装置制备 并进行相关性质的探究。回答下列问题:
并进行相关性质的探究。回答下列问题:

(1)盛装浓硫酸的仪器名称为___________ ;装置c中品红溶液褪色,可证明 具有
具有___________ 性,装置b的作用是___________ 。
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间 ,此操作的目的是
,此操作的目的是___________ 。
(3)装置a中反应的化学方程式为___________ 。
(4)探究:探究 在KI溶液体系中的反应产物
在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应: 。但有同学提出上述反应生成的
。但有同学提出上述反应生成的 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。
I.取适量装置d中溶液,向其中滴加几滴溶液___________ (填试剂名称),振荡,无明显变化,溶液中无 。
。
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液:取适量分离后的澄清溶液于试管中,___________ ,出现白色沉淀,则产物溶液中存在 ,其离子方程式为
,其离子方程式为___________ 。
综上可知, 在KI溶液中发生了歧化反应,其反应的离子方程式为
在KI溶液中发生了歧化反应,其反应的离子方程式为___________ 。
 并进行相关性质的探究。回答下列问题:
并进行相关性质的探究。回答下列问题:
(1)盛装浓硫酸的仪器名称为
 具有
具有(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间
 ,此操作的目的是
,此操作的目的是(3)装置a中反应的化学方程式为
(4)探究:探究
 在KI溶液体系中的反应产物
在KI溶液体系中的反应产物实验开始后,发现装置d中的溶液迅速变黄,继续通入
 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应: 。但有同学提出上述反应生成的
。但有同学提出上述反应生成的 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。I.取适量装置d中溶液,向其中滴加几滴溶液
 。
。Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液:取适量分离后的澄清溶液于试管中,
 ,其离子方程式为
,其离子方程式为综上可知,
 在KI溶液中发生了歧化反应,其反应的离子方程式为
在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
7 . 下图是实验室制取SO2并验证SO2的某些性质的装置,请回答:

(1)在⑥中发生反应的化学方程式为_______ 。
(2)①中的实验现象为石蕊溶液_______ ,此实验证明SO2具有_______ 的性质。
(3)②中的品红溶液_______ ,证明SO2有_______ 性。
(4)③中的实验现象是_______ ,证明SO2有_______ 性。
(5)④中的实验现象是_______ ,证明SO2有_______ 性。
(6)⑤的作用是_______ ,反应的化学方程式为_______ 。
(7)写出铜与浓硫酸反应的化学方程式_______ 。

(1)在⑥中发生反应的化学方程式为
(2)①中的实验现象为石蕊溶液
(3)②中的品红溶液
(4)③中的实验现象是
(5)④中的实验现象是
(6)⑤的作用是
(7)写出铜与浓硫酸反应的化学方程式
您最近一年使用:0次
8 . 如图是实验室制取SO2并验证SO2的某些性质的装置,请回答:

(1)在⑥中发生反应的化学方程式为_______ 。
(2)①中的实验现象为紫色石蕊溶液_______ ,此实验证明SO2具有_______ 的性质。
(3)②中的品红溶液_______ ,证明SO2具有_______ 性。
(4)③中的实验现象是_______ ,证明SO2具有_______ 性。
(5)④中的实验现象是_______ ,证明SO2具有_______ 性。
(6)⑤的作用是_______ ,反应的化学方程式为_______ 。

(1)在⑥中发生反应的化学方程式为
(2)①中的实验现象为紫色石蕊溶液
(3)②中的品红溶液
(4)③中的实验现象是
(5)④中的实验现象是
(6)⑤的作用是
您最近一年使用:0次
2022-10-23更新
|
143次组卷
|
2卷引用:云南省建水县第二中学2021-2022学年高一下学期期中考试化学(理科)试题
9 . 某化学兴趣小组为了探究铜与浓硫酸的反应以及产物的性质,设计了如图所示装置进行实验。回答下列问题:
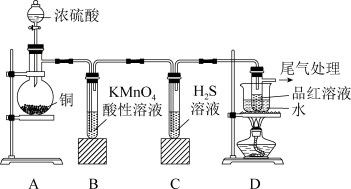
(1)若要使装置A中反应发生还缺少的实验仪器是_______ 。写出装置A中发生反应的化学反应方程式_______ 。
(2)装置C中发生反应的化学方程式是_______ ,说明 具有
具有_______ 性。
(3)装置D的目的是探究 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象_______ 。
(4)尾气可采用_______ 溶液吸收。
(5)装置A中,足量的铜与浓硫酸反应结束后,烧瓶里溶液中的溶质除了 外,
外,_______ (填“一定”、“一定不”或“不一定”)含有 。下列药品中,可用来证明该观点的是
。下列药品中,可用来证明该观点的是_______ (选填字母编号)。
A.铁粉 B. 溶液 C.NaOH溶液 D.CuO
溶液 C.NaOH溶液 D.CuO

(1)若要使装置A中反应发生还缺少的实验仪器是
(2)装置C中发生反应的化学方程式是
 具有
具有(3)装置D的目的是探究
 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象(4)尾气可采用
(5)装置A中,足量的铜与浓硫酸反应结束后,烧瓶里溶液中的溶质除了
 外,
外, 。下列药品中,可用来证明该观点的是
。下列药品中,可用来证明该观点的是A.铁粉 B.
 溶液 C.NaOH溶液 D.CuO
溶液 C.NaOH溶液 D.CuO
您最近一年使用:0次
2022-04-23更新
|
299次组卷
|
3卷引用:云南省红河哈尼族彝族自治州第一中学2022-2023学年高一下学期5月期中化学试题
名校
解题方法
10 . 某小组使用Y形管、注射器和三个横口管进行二氧化硫气体的制备和性质探究的创新实验。图1为球形横口管,其下部带有一个横口,有利于气体和液体通过。回答下列问题:

(1)装入药品前,检查图2中装置气密性的方法为:先拉开注射器活塞以吸入空气,然后组装仪器,再将注射器中的空气推入,若观察到_____ 证明气密性良好。
(2)浓硫酸与亚硫酸钠反应的化学方程式为________ 。
(3)实验中可观察到品红溶液褪色、硫化钠溶液中________ 、高锰酸钾溶液褪色、紫色石蕊溶液____ 分别体现了SO2的漂白性、______ 、_______ 和______ ;其中,SO2与高锰酸钾溶液反应的离子方程式为________ 。
(4)脱脂棉用NaOH溶液浸湿,其作用是________________ 。
(5)与常规的探究实验(装置如图)比较,该创新实验的优点有________ (答出两点即可)。


(1)装入药品前,检查图2中装置气密性的方法为:先拉开注射器活塞以吸入空气,然后组装仪器,再将注射器中的空气推入,若观察到
(2)浓硫酸与亚硫酸钠反应的化学方程式为
(3)实验中可观察到品红溶液褪色、硫化钠溶液中
(4)脱脂棉用NaOH溶液浸湿,其作用是
(5)与常规的探究实验(装置如图)比较,该创新实验的优点有

您最近一年使用:0次