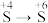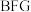解题方法
1 . 在周末的化学探究活动中,同学小苏在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。如图所示,则下列有关说法正确的是
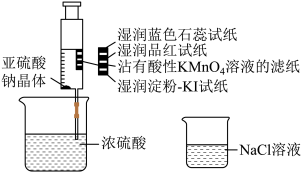
| A.蓝色石蕊试纸先变红后褪色 |
| B.品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性 |
| C.湿润的淀粉KI试纸未变蓝说明SO2的氧化性强于I2 |
| D.注射器中发生反应的基本类型是复分解反应 |
您最近半年使用:0次
2 . 利用下图装置制取 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是
 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是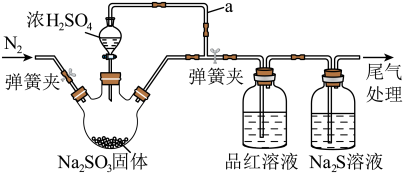
| A.导管a的作用是保证浓硫酸顺利滴下 |
B.品红溶液褪色,说明 可能具有漂白性 可能具有漂白性 |
C. 溶液中出现浑浊,证明 溶液中出现浑浊,证明 具有氧化性 具有氧化性 |
D.三颈烧瓶内反应开始前通 与反应结束后通 与反应结束后通 目的相同 目的相同 |
您最近半年使用:0次
名校
解题方法
3 . 某小组同学探究SO2与新制Cu(OH)2悬浊液反应的实验装置图如下所示:
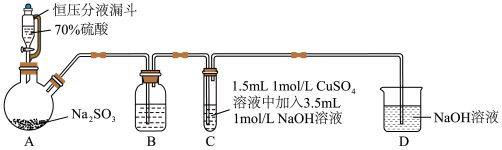
下列说法不正确的是

下列说法不正确的是
| A.配制70%硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管 |
| B.装置B的作用是监控SO2流速,其中试剂可以用饱和NaHSO4溶液 |
| C.反应开始时C中出现砖红色沉淀,氧化剂和还原剂的物质的量之比为2:1 |
| D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl2溶液、有白色沉淀生成,证明反应中SO2作还原剂 |
您最近半年使用:0次
2024-04-07更新
|
400次组卷
|
2卷引用:2024届甘肃省兰州市高三下学期诊断考试化学试卷
解题方法
4 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。回答下列问题:
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A. 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液
D.稀硫酸 E.酸性 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝
实验i选择的试剂是E和______ (填字母),证明实现转化的现象是______ 。
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。
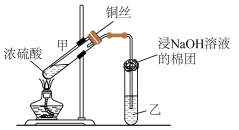
①试管甲中发生反应的化学方程式是__________ 。
②试管乙中的现象是_______ ;若实验结束后,将试管乙中的溶液加热,可以观察到的现象是______ 。
③下列关于 的说法,不正确的是
的说法,不正确的是__________ 。(填字母)
a.正常雨水的 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7
b.金属冶炼时产生的含 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸
c. 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A.
 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液D.稀硫酸 E.酸性
 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
i |
| ||
ii |
|
|
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。

①试管甲中发生反应的化学方程式是
②试管乙中的现象是
③下列关于
 的说法,不正确的是
的说法,不正确的是a.正常雨水的
 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7b.金属冶炼时产生的含
 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸c.
 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
您最近半年使用:0次
名校
5 .  和
和 在生产、生活和科学研究中有着广泛的应用。葡萄酒中添加适量的二氧化硫可以起到抗氧化等作用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成
在生产、生活和科学研究中有着广泛的应用。葡萄酒中添加适量的二氧化硫可以起到抗氧化等作用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成 ;
; 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应:
在接触室中发生可逆反应: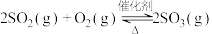 ;生成的
;生成的 在吸收塔中用98.3%的浓硫酸吸收。同学们在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在吸收塔中用98.3%的浓硫酸吸收。同学们在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是

 和
和 在生产、生活和科学研究中有着广泛的应用。葡萄酒中添加适量的二氧化硫可以起到抗氧化等作用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成
在生产、生活和科学研究中有着广泛的应用。葡萄酒中添加适量的二氧化硫可以起到抗氧化等作用。工业上常用接触法制备硫酸,过程如下:将硫黄或其他含硫矿物在沸腾炉中与氧气反应生成 ;
; 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应:
在接触室中发生可逆反应: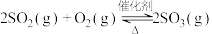 ;生成的
;生成的 在吸收塔中用98.3%的浓硫酸吸收。同学们在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在吸收塔中用98.3%的浓硫酸吸收。同学们在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
A.①中品红褪色证明 有氧化性 有氧化性 |
| B.②中的试剂X应该是浓硫酸 |
| C.③中的试剂Y应该是NaOH溶液 |
D.②中颜色变浅,但不消失,即可由③验证 |
您最近半年使用:0次
2023-05-13更新
|
383次组卷
|
2卷引用:江苏省海安高级中学2022-2023学年高一下学期期中考试化学(必修)试题
解题方法
6 . 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
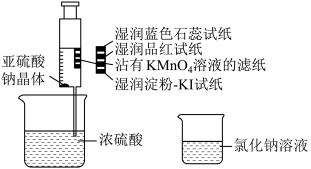

| A.蓝色石蕊试纸变红 |
| B.品红试纸、沾有高锰酸钾溶液的滤纸均褪色,证明SO2具有漂白性 |
| C.湿润的淀粉碘化钾试纸未变蓝,说明SO2的氧化性弱于I2 |
| D.NaCl溶液可用于除去实验中多余的SO2 |
您最近半年使用:0次
解题方法
7 . T℃时,在体积为2L的密闭容器内,与同一个化学反应有关的A、B、C、D四种物质(D为固体,其余均为气体)的物质的量随反应时间变化的曲线如图所示,回答下列问题。
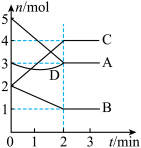
(1)该反应的化学方程式为_______ 。
(2)物质D在反应中的作用是______ 。
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是______ (填字母);在0~2min内用O2表示的反应速率v(O2)=______ 。
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是_______ 。
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。
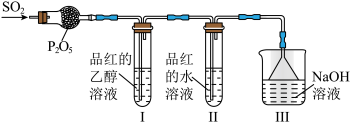
查阅资料:SO2通入水中存在如下反应:SO2+xH2O SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。
通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.______ ;iii.______ 。
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
该实验说明,两种粒子中,______ 使品红水溶液褪色程度更大。
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明______ ;取实验2所得溶液直接加热,则慢慢恢复浅红色,说明NaHSO3与品红生成的物质不稳定。

(1)该反应的化学方程式为
(2)物质D在反应中的作用是
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。

查阅资料:SO2通入水中存在如下反应:SO2+xH2O
 SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
| 实验序号 | 实验1 | 实验2 |
| 实验操作 |  2mL0.20mol•L-1Na2SO3溶液 |  2mL0.20mol•L-1NaHSO3溶液 |
| 实验现象 | 迅速褪色 | 褪色较慢 |
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明
您最近半年使用:0次
2023-04-28更新
|
377次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
8 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
(1)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是___________ 。
(2)用化学方程式表示氢氧化钠溶液的作用是___________ 。
(3)装置A中反应的化学方程式是___________ 。
(4)装置B中反应的离子方程式是___________ 。装置C中反应的化学方程式是___________ 。
(5)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、 和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、CuS不溶于稀硫酸。
、CuS不溶于稀硫酸。
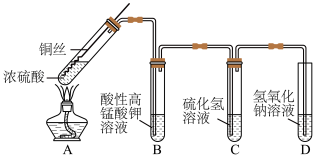
(1)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(2)用化学方程式表示氢氧化钠溶液的作用是
(3)装置A中反应的化学方程式是
(4)装置B中反应的离子方程式是
(5)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、
 和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、CuS不溶于稀硫酸。
、CuS不溶于稀硫酸。硫酸浓度/(mol·L ) ) | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
B.黑色物质消失过程中有 、 、 生成 生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16 mol/L时,先升温至:250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近半年使用:0次
名校
解题方法
9 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
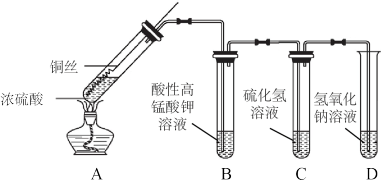
回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是_______ 。
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是_______ 。
(3)用化学方程式表示氢氧化钠溶液的作用是_______ 。
(4)装置A中反应的化学方程式是_______ 。
(5)装置B和装置C分别验证了二氧化硫的_______ 性质。
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。

回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(3)用化学方程式表示氢氧化钠溶液的作用是
(4)装置A中反应的化学方程式是
(5)装置B和装置C分别验证了二氧化硫的
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。
| 硫酸浓度/(mol· L-1) | 黑色物质出现的温度/°C | 黑色物质消失的温度/°C |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
| B.黑色物质消失过程中有SO2、H2S生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16mol/L时,先升温至250°C以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近半年使用:0次
2022-04-27更新
|
230次组卷
|
2卷引用:山西省运城市高中联合体2021-2022学年高一下学期期中联考化学试题
10 . 利用如图所示装置进行 的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
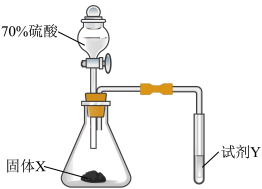
 的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
| A.固体X可为Cu |
| B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀 |
C.为证明 具有还原性,试剂Y可为酸性 具有还原性,试剂Y可为酸性 溶液 溶液 |
D.该装置中试管口应塞一团浸有 溶液的棉团 溶液的棉团 |
您最近半年使用:0次