解题方法
1 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。下列说法不正确的是
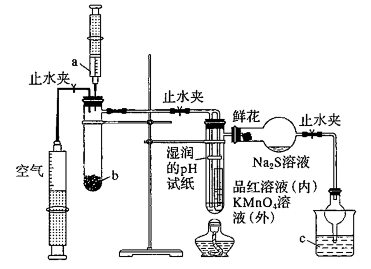

A.a、b、c中依次盛装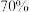 硫酸、 硫酸、 固体、NaOH溶液 固体、NaOH溶液 |
B.点燃酒精灯加热,可证明 使品红溶液褪色具有可逆性,使 使品红溶液褪色具有可逆性,使 溶液褪色不具有可逆性 溶液褪色不具有可逆性 |
C.此设计可证明 水溶液的酸性, 水溶液的酸性, 的氧化性、还原性、漂白性 的氧化性、还原性、漂白性 |
D.实验时,湿润的pH试纸、鲜花、品红溶液、 溶液均褪色, 溶液均褪色, 溶液出现淡黄色沉淀 溶液出现淡黄色沉淀 |
您最近一年使用:0次
名校
解题方法
2 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是


| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5mol Na2O2,转移电子数为2NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
名校
3 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是
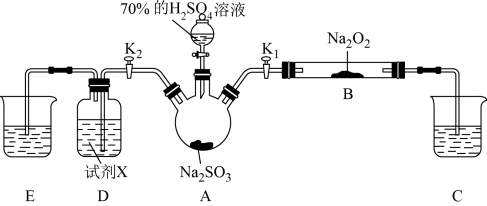

| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5molNa2O2,转移电子数为3NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
2021-11-03更新
|
316次组卷
|
5卷引用:山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题
4 . 如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。下列有关说法正确的是
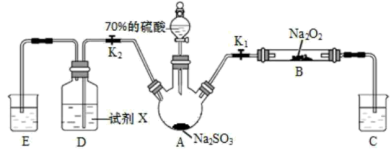

| A.为防止环境污染,装置C和E中的试剂均取用饱和的石灰水 |
| B.关闭K1,打开K2,试剂X是酸性KMnO4或FeCl3溶液,均可证明SO2有还原性 |
| C.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性 |
| D.关闭K2,打开K1,滴加硫酸,则装置B中每消耗1molNa2O2,转移1mol电子 |
您最近一年使用:0次
2021-10-21更新
|
122次组卷
|
2卷引用:黑龙江省宾县第一中学校2021-2022学年高三上学期第一次月考化学试题
20-21高一上·全国·假期作业
名校
解题方法
5 . 如图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中有淡黄色沉淀生成,⑤中的溴水褪色,下列说法错误的是
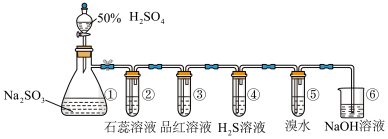

A.①中发生反应的离子方程式是SO +2H+=H2O+SO2↑ +2H+=H2O+SO2↑ |
| B.②中溶液变为红色 |
| C.③的品红溶液褪色,证明SO2有漂白性 |
| D.④中SO2作还原剂 |
您最近一年使用:0次
2021-01-14更新
|
310次组卷
|
3卷引用:练习15 含硫化合物的性质和应用-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)
(已下线)练习15 含硫化合物的性质和应用-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)陕西省西安市西航一中2021~2022学年高一上学期期末考试化学试题甘肃省天水市第一中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
6 . 某同学用如图装置进行铜与浓硫酸反应的实验(加热和夹持装置已略去):

实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A;
③将铜丝上提离开液面,停止加热。
(1)A中发生反应的化学方程式为____ 。
(2)若仪器B的作用是收集反应产生的SO2,请在虚线框中将该装置补充完整___ 。
(3)证明仪器B中SO2气体已经收集满的现象是___ 。
(4)下列有关该实验说法不正确 的是___ 。
A.浓硫酸与铜的反应中,浓硫酸只表现酸性
B.上下移动A中铜丝可控制生成SO2的量
C.实验后为避免仪器A中残留SO2泄漏,可将导管通入盛有NaOH溶液的烧杯中,打开旋塞E,缓缓从E向A中鼓入足量空气
D.如果铜丝足量,仪器A中的硫酸可反应完全

实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A;
③将铜丝上提离开液面,停止加热。
(1)A中发生反应的化学方程式为
(2)若仪器B的作用是收集反应产生的SO2,请在虚线框中将该装置补充完整
(3)证明仪器B中SO2气体已经收集满的现象是
(4)下列有关该实验说法
A.浓硫酸与铜的反应中,浓硫酸只表现酸性
B.上下移动A中铜丝可控制生成SO2的量
C.实验后为避免仪器A中残留SO2泄漏,可将导管通入盛有NaOH溶液的烧杯中,打开旋塞E,缓缓从E向A中鼓入足量空气
D.如果铜丝足量,仪器A中的硫酸可反应完全
您最近一年使用:0次
2021-06-25更新
|
366次组卷
|
3卷引用:浙江省杭州市余杭、临平、萧山2020-2021学年高一下学期期末学业水平测试化学试题
名校
解题方法
7 . 为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是__ ;
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用___ (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中SO2的体积分数为__ 。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中除SO2外还可能含有Q1和Q2两种气体,其中Q1气体,存标准状况下密度为0.0893g/L。为此设计了下列探究实验装置(假设有关气体完全反应)。___ 。
(4)分析Y气体中的Q2气体是如何生成的___ (用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加M于____ (填序号)。
A.A之前 B.A—B间 C.B—C间 D.C—D间
(6)确认Q1气体存在的实验现象是____ 。
[探究三]如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。___
A.关闭K2,打开Kl,滴加硫酸,则装置B中每消耗1molNa2O2,转移电子数为2NA
B.关闭Kl,打丌K2,试剂X是酸性KmnO4或FeCl3溶液,均可证明SO2有还原性
C.为防止环境污染,装置C和E中的试剂均取用NaOH溶液
D.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性
[探究一]
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中SO2的体积分数为
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中除SO2外还可能含有Q1和Q2两种气体,其中Q1气体,存标准状况下密度为0.0893g/L。为此设计了下列探究实验装置(假设有关气体完全反应)。

(4)分析Y气体中的Q2气体是如何生成的
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加M于
A.A之前 B.A—B间 C.B—C间 D.C—D间
(6)确认Q1气体存在的实验现象是
[探究三]如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。

A.关闭K2,打开Kl,滴加硫酸,则装置B中每消耗1molNa2O2,转移电子数为2NA
B.关闭Kl,打丌K2,试剂X是酸性KmnO4或FeCl3溶液,均可证明SO2有还原性
C.为防止环境污染,装置C和E中的试剂均取用NaOH溶液
D.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性
您最近一年使用:0次
8 . 如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。下列有关说法正确的是
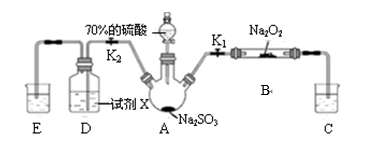

| A.为防止环境污染,装置C和E中的试剂均取用饱和的石灰水 |
| B.关闭 K2,打开 K1,滴加硫酸,则装置 B 中每消耗1mol Na2O2,转移1mol电子 |
| C.关闭 K1,打开 K2,试剂 X 是酸性 KMnO4 或 FeCl3 溶液,均可证明 SO2 有还原性 |
| D.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性 |
您最近一年使用:0次
2018-10-22更新
|
465次组卷
|
4卷引用:黑龙江省哈尔滨师范大学附属中学2019届高三上学期第一次月考化学试题
9 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。下列说法不正确的是
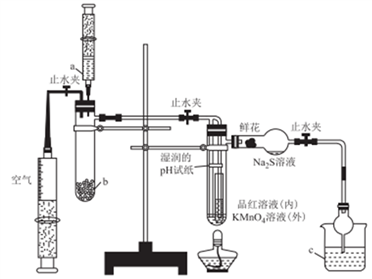

| A.a、b、c中依次盛装70%硫酸.Na2SO3固体、NaOH溶液 |
| B.实验时,湿润的pH试纸、鲜花、品红溶液、KMnO4溶液均褪色,Na2S溶液出现淡黄色沉淀 |
| C.此设计可证明SO2水溶液的酸性,SO2的氧化性、还原性、漂白性 |
| D.点燃酒精灯加热,可证明SO2使品红溶液褪色具有可逆性,使KMnO4溶液褪色不具有可逆性 |
您最近一年使用:0次
2018-04-27更新
|
1785次组卷
|
10卷引用:湖南省益阳市2018届高三4月调研考试理综化学试题
湖南省益阳市2018届高三4月调研考试理综化学试题湖南省浏阳市第一中学2018届高三上学期入学测试化学试题(已下线)第15讲 硫及其化合物(精练)-2021年高考化学一轮复习讲练测人教版2019必修第二册 第五章 本章达标检测(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)上海交通大学附属中学2022-2023学年高一上学期期末考试化学试题上海交通大学附属中学2022-2023学年高一上学期期末考试化学试题湖南省衡阳市第八中学2023-2024学年高一下学期开学考试化学试题江苏省常州市田家炳2高级中学023-2024学年高一上学期12月阶段性调研化学学科试卷
10 . 已知 可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:
可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:
实验一:探究亚硫酸与次氯酸的酸性强弱。选用的装置和药品如下。

 装置A气密性检查的方法是
装置A气密性检查的方法是________ 。
 装置连接顺序为A、
装置连接顺序为A、________ 、B、E、________ 、F,其中装置E中反应的离子方程式为________ ,通过现象________ 即可证明亚硫酸的酸性强于次氯酸。
实验二:探究氯气与硫化氢气体混合能发生反应。选用的装置和药品如下。

 通过现象
通过现象________ 即可证明氯气与硫化氢发生了反应。
 该装置存在一个不妥之处,你的改进措施为
该装置存在一个不妥之处,你的改进措施为________ 。
实验三:探究氯元素和硫元素非金属性强弱。
 为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是
为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是________ 。
A.实验一能说明硫元素非金属性强于氯元素 B.实验二能说明硫元素非金属性弱于氯元素
C.通过测定盐酸和氢硫酸的pH来判断非金属性强弱 D.已知硫化氢的沸点为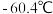 ,氯化氢的沸点为
,氯化氢的沸点为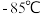 ,则硫元素非金属性强于氯元素
,则硫元素非金属性强于氯元素
 可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:
可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动: 实验一:探究亚硫酸与次氯酸的酸性强弱。选用的装置和药品如下。

 装置A气密性检查的方法是
装置A气密性检查的方法是 装置连接顺序为A、
装置连接顺序为A、实验二:探究氯气与硫化氢气体混合能发生反应。选用的装置和药品如下。

 通过现象
通过现象 该装置存在一个不妥之处,你的改进措施为
该装置存在一个不妥之处,你的改进措施为实验三:探究氯元素和硫元素非金属性强弱。
 为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是
为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是A.实验一能说明硫元素非金属性强于氯元素 B.实验二能说明硫元素非金属性弱于氯元素
C.通过测定盐酸和氢硫酸的pH来判断非金属性强弱 D.已知硫化氢的沸点为
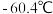 ,氯化氢的沸点为
,氯化氢的沸点为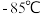 ,则硫元素非金属性强于氯元素
,则硫元素非金属性强于氯元素
您最近一年使用:0次



