1 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括________ 、水泥和玻璃。
(2) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是________ (用化学方程式表示)。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是________(填字母)。
(4)硅单质可作为硅半导体材料。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:________ 。
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是________ 。
(5)新型陶瓷材料氮化硅( )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为________  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是________(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作为硅半导体材料。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图: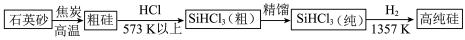
②整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是(5)新型陶瓷材料氮化硅(
 )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近一年使用:0次
2 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是_______ (填化学式,下同),光导纤维的主要成分是_______ 。
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为_______ 。
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:_______ 。
(4)高纯度单晶硅可以按下列方法制备:SiO2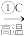 Si(粗)
Si(粗)  SiiHCl3
SiiHCl3 Si(纯)。写出步骤①的化学方程式:
Si(纯)。写出步骤①的化学方程式:_____ 。该反应中C作____ 剂,此方程式能否说明非金属性:C>Si____ 。若要证明C和Si的非金属性强弱,请设计实验并预测实验现象____ 。
(1)可用于制作计算机芯片和太阳能电池的是
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(4)高纯度单晶硅可以按下列方法制备:SiO2
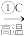 Si(粗)
Si(粗)  SiiHCl3
SiiHCl3 Si(纯)。写出步骤①的化学方程式:
Si(纯)。写出步骤①的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料所含元素在元素周期中的位置___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石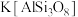 和钠长石
和钠长石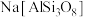 等,
等,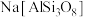 用氧化物形式表示为
用氧化物形式表示为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石
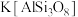 和钠长石
和钠长石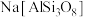 等,
等,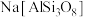 用氧化物形式表示为
用氧化物形式表示为
您最近一年使用:0次
解题方法
4 . 材料是人类赖以生存和发展的重要物质基础。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是_________ 。
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是_________ (填字母)。
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生_________ (填“化学”或“电化学”)腐蚀,在铁制闸门上常嵌入_________ (填“铜块”、“锌块”)来保护闸门防止腐蚀。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生
您最近一年使用:0次
5 . 第24届冬奥会于2022年2月4日——2月20日在北京举行。
(1)建造体育馆门窗玻璃框架使用的合金材料为_______ (填字母代号)。
A.铝合金 B.钢铁 C.青铜
(2)运动员的防切割竞赛服的主要材料是聚氨酯,它属于_______ (填字母代号)。
A.无机非金属材料 B.有机高分子材料 C.金属材料
(3)装修材料挥发出的居室污染物常见的有_______ (写名称)和苯等。
(4)国家速滑馆的冰面温度差不超过0.5℃,与信息的高速传递密不可分。光导纤维被称为信息高速公路的骨架,其主要成分是_______ 。
(1)建造体育馆门窗玻璃框架使用的合金材料为
A.铝合金 B.钢铁 C.青铜
(2)运动员的防切割竞赛服的主要材料是聚氨酯,它属于
A.无机非金属材料 B.有机高分子材料 C.金属材料
(3)装修材料挥发出的居室污染物常见的有
(4)国家速滑馆的冰面温度差不超过0.5℃,与信息的高速传递密不可分。光导纤维被称为信息高速公路的骨架,其主要成分是
您最近一年使用:0次
6 . 请根据物质在生产、生活中的应用填空:
(1)自来水厂对水消毒,常使用的物质是_______ (填“液氯”或“明矾”)。
(2)制造光导纤维的基本原料是_______ 。
(3)常温下盛装浓硝酸可使用的容器是_______ (填“铁罐”或“铜罐”)。
(4)电子工业常用30%的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式_______ 。
(5)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是_______ 。
(6)大型中央空调的制冷剂可用液氨,原因是_______ 。
(1)自来水厂对水消毒,常使用的物质是
(2)制造光导纤维的基本原料是
(3)常温下盛装浓硝酸可使用的容器是
(4)电子工业常用30%的
 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(5)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是
(6)大型中央空调的制冷剂可用液氨,原因是
您最近一年使用:0次
解题方法
7 . (1)石英耐高温,可制成石英坩埚,下列试剂可用石英坩埚加热的是________ ;
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(2)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为________________________ ;
(3)有以下13种物质,请回答下列问题(填序号):
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
其中能导电的是_________ ; 属于电解质的是 _________ ;属于非电解质的是 _________ 。
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(2)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为
(3)有以下13种物质,请回答下列问题(填序号):
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
其中能导电的是
您最近一年使用:0次



