名校
1 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。
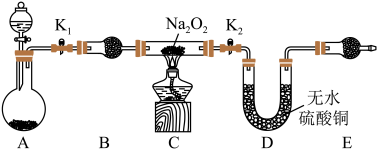
Ⅰ.实验探究
(1)装置A中用粗锌和稀盐酸制取氢气,B装置的作用是______ ,里面所盛放的试剂是______ (①浓硫酸②碱石灰③无水硫酸铜)。
(2)下面是实验过程中的重要操作,正确的顺序是________ (填序号)
A.加热至Na2O2逐渐熔化,反应一段时间 B.用小试管收集气体并检验其纯度
C.打开K1、K2,通入氢气 D.停止加热,充分冷却,关闭K1、K2
(3)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为_____ 。
Ⅱ.数据处理
(4)实验结束后,该同学欲测定C装置内白色固体中未反应完的Na2O2含量。其操作流程如图:
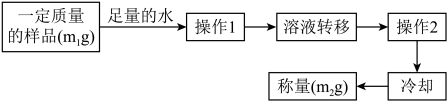
①测定过程中需要的仪器除固定、夹持仪器外,还有天平、烧杯、酒精灯、蒸发皿和____ ,操作2的名称是____ 。
②白色固体中Na2O2的质量分数为_____________ (用含m1和m2的式子表示)。
③在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数________ (填“偏大”“偏小”或“不变”)。

Ⅰ.实验探究
(1)装置A中用粗锌和稀盐酸制取氢气,B装置的作用是
(2)下面是实验过程中的重要操作,正确的顺序是
A.加热至Na2O2逐渐熔化,反应一段时间 B.用小试管收集气体并检验其纯度
C.打开K1、K2,通入氢气 D.停止加热,充分冷却,关闭K1、K2
(3)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为
Ⅱ.数据处理
(4)实验结束后,该同学欲测定C装置内白色固体中未反应完的Na2O2含量。其操作流程如图:

①测定过程中需要的仪器除固定、夹持仪器外,还有天平、烧杯、酒精灯、蒸发皿和
②白色固体中Na2O2的质量分数为
③在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
2020-11-11更新
|
344次组卷
|
3卷引用:作业(八) 氧化钠和过氧化钠
2 . 研究小组探究Na2O2与水反应。向1.56 gNa2O2粉末中加入40 mL水,充分反应得溶液A(溶液体积变化忽略不计),进行实验。
实验1:向2 mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为_______ 。溶液A中NaOH溶液的质量分数为_______ 。
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2 mL溶液A中加入黑色粉末_______ (填化学式),快速产生了能使带火星木条复燃的气体。
②实验3:向2 mL NaOH质量分数为_______ %的NaOH溶液中滴入1滴酚酞,溶液变红色,10分钟后溶液褪色。向褪色的溶液中加入_______ ,溶液变红色。
【得出结论】
由以上实验可得出的结论是_______ 。
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为_______ 、_______ ,但课本上没有写出中间产物H2O2,可能的原因是_______ 。
实验1:向2 mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2 mL溶液A中加入黑色粉末
②实验3:向2 mL NaOH质量分数为
【得出结论】
由以上实验可得出的结论是
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为
您最近一年使用:0次
3 . 过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂。
实验探究一:过氧化钙与水反应除生成氧气外,还生成什么物质?
(1)进行实验:取适量过氧化钙放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式:______________ 。
(2)此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是否变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。有同学不认同上述方案的理由是_______________________ 。
实验探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
(3)取一定质量的供氧剂溶于水,按照图1装置进行装配。读出体积时要注意:①该反应为放热反应,待气体恢复至室温再读数;②____________________________ ;③视线和凹液面最低处保持水平再读数。
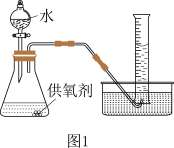
(4)用此装置测得的含量会偏大,原因是________________ ,为了避免此误差可将发生装置换成图2中的装置B或C。
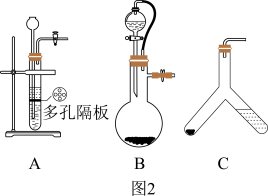
方案二:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图3。
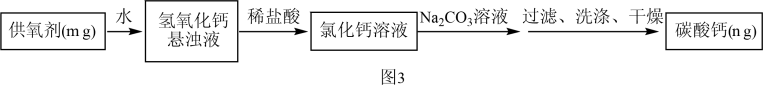
(5)滴加的Na2CO3溶液要过量的原因是_________________________ 。
实验探究一:过氧化钙与水反应除生成氧气外,还生成什么物质?
(1)进行实验:取适量过氧化钙放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式:
(2)此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是否变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。有同学不认同上述方案的理由是
实验探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
(3)取一定质量的供氧剂溶于水,按照图1装置进行装配。读出体积时要注意:①该反应为放热反应,待气体恢复至室温再读数;②

(4)用此装置测得的含量会偏大,原因是

方案二:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图3。

(5)滴加的Na2CO3溶液要过量的原因是
您最近一年使用:0次
名校
4 . 在鲜活水产品的长途运输中,必须考虑以下几点:①水中需要保持适量的氧气;②及时去除鱼排出的二氧化碳;③防止细菌的大量繁殖。
(1)过氧化物具有杀菌消毒的性质,金属的过氧化物能与水反应产生氧气,现有两种在水中能起供氧灭菌作用的物质:过氧化钠和过氧化钙(CaO2),已知过氧化钙能缓慢与水反应。根据以上介绍,运输鲜活水产品时应选择_______ 放入水中,理由是_______ 。
(2)写出过氧化钙与水反应的化学方程式_______ 。
(3)一养鱼爱好者欲测定过氧化钙样品中过氧化钙的质量分数,做如下实验:称取样品2.0g,加入到足量的水中,生成224mL氧气(氧气的密度为1.43g·L-1,杂质不产生氧气)。试计算所用样品中过氧化钙的质量分数_______ 。
(1)过氧化物具有杀菌消毒的性质,金属的过氧化物能与水反应产生氧气,现有两种在水中能起供氧灭菌作用的物质:过氧化钠和过氧化钙(CaO2),已知过氧化钙能缓慢与水反应。根据以上介绍,运输鲜活水产品时应选择
(2)写出过氧化钙与水反应的化学方程式
(3)一养鱼爱好者欲测定过氧化钙样品中过氧化钙的质量分数,做如下实验:称取样品2.0g,加入到足量的水中,生成224mL氧气(氧气的密度为1.43g·L-1,杂质不产生氧气)。试计算所用样品中过氧化钙的质量分数
您最近一年使用:0次
2021-10-19更新
|
154次组卷
|
3卷引用:作业(二) 研究物质的基本方法
21-22高一·全国·课后作业
名校
5 . 如图所示,甲、乙、丙、丁四个烧杯中分别盛有100mL蒸馏水,然后分别放入0.23 g Na、0.62 g Na2O、0.78 g Na2O2、0.40 g NaOH,待固体完全溶解,则四个烧杯中溶液的质量分数的大小顺序为
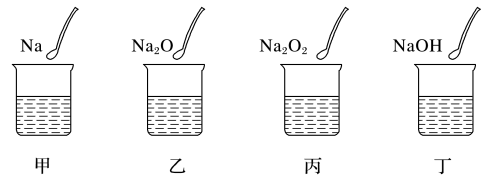

| A.甲<乙<丙<丁 | B.丁<甲<乙=丙 |
| C.甲=丁<乙=丙 | D.丁<甲<乙<丙 |
您最近一年使用:0次
2021-08-25更新
|
375次组卷
|
9卷引用:1.2.1 研究物质的基本方法-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)1.2.1 研究物质的基本方法-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)(已下线)3.2.1 钠的性质与制备-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)山东省济南市历城第二中学2021-2022学年高一上学期第一次月考化学试题河南省郑州励德双语学校2021-2022学年高一上学期第一次月考化学试题广东省茂名市七迳中学2023-2024学年高一上学期期中考试化学试卷广东省湛江市2023-2024学年高一上学期11月期中考试化学试题甘肃省白银市靖远县2023-2024学年高一上学期11月期中联考化学试题宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题河南省创新发展联盟2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
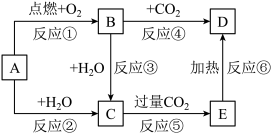
(1)写出下列物质的化学式:B___ 。
(2)以上6个反应中属于氧化还原反应的有___ (填写编号)。
(3)写出A →C反应的离子方程式___ 。
(4)写出B→C反应的离子方程式:___ ;E→D的化学方程式:___ 。
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为___ 。

(1)写出下列物质的化学式:B
(2)以上6个反应中属于氧化还原反应的有
(3)写出A →C反应的离子方程式
(4)写出B→C反应的离子方程式:
(5)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量分数为
您最近一年使用:0次
2019-12-16更新
|
399次组卷
|
4卷引用:鲁科版(2019)高一必修第一册第3章 物质的性质与转化 专题6 元素及其化合物的转化与推断
7 . 将等物质的量钠、过氧化钠、氧化钠、氢氧化钠加入到足量且等量的水中,形成溶液质量分数分别为X、Y、Z、W,下列关系正确的是
| A.X<W<Y<Z | B.W<X<Y<Z | C.W<X<Y=Z | D.W<X<Y<Z |
您最近一年使用:0次



