解题方法
1 . 如图所示, 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题:
B____________ ,C____________ ,D____________ .
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:____________ (写化学方程式);
②A→C:____________ (写离子方程式):
③B→C:____________ (写离子方程式).
 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题: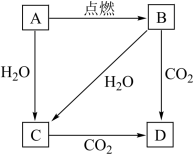
B
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:
②A→C:
③B→C:
您最近一年使用:0次
2 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。(提示:铬元素的化合价有+6、+3)_______ 。
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目_______ 。
②上述反应中氧化产物和还原产物的质量比为_______ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是
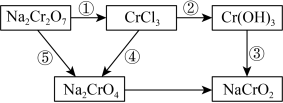
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目
②上述反应中氧化产物和还原产物的质量比为
您最近一年使用:0次
3 . 下列有关物质的性质与用途对应关系错误的是
| A.浓硫酸具有吸水性,可用于干燥氨气 |
| B.Na2O2能与CO2反应,可用作供氧剂 |
| C.SO2具有漂白性,可用于漂白纸浆 |
| D.SiC熔点高,可用作耐高温材料 |
您最近一年使用:0次
解题方法
4 . 金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是_____________ 色固体。
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出 和
和 反应的化学方程式:
反应的化学方程式:__________________ ,消耗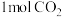 时,反应中转移的电子总数为
时,反应中转移的电子总数为__________ mol。
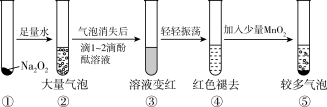
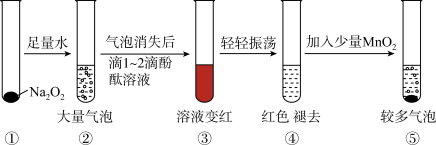
(4)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
(5)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: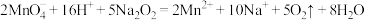
①比较氧化性强弱:
______  (选填“>”或“<”)。
(选填“>”或“<”)。
②该反应说明 具有
具有______ (选填“氧化性”或“还原性”)。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
A.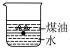 | B.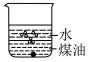 |
C.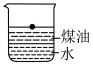 | D.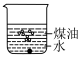 |
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出
 和
和 反应的化学方程式:
反应的化学方程式: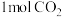 时,反应中转移的电子总数为
时,反应中转移的电子总数为(4)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(5)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: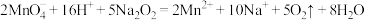
①比较氧化性强弱:

 (选填“>”或“<”)。
(选填“>”或“<”)。②该反应说明
 具有
具有
您最近一年使用:0次
5 . 下表中,对陈述I、II的正确性及二者间是否具有因果关系的判断都正确的是
| 选项 | 陈述I | 陈述II | 判断 |
| A | 小苏打可用于治疗胃酸过多 | Na2CO3可与盐酸反应 | I对;II对;有关系 |
| B | 向滴有酚酞的水溶液中加入Na2O2,溶液变红 | Na2O2与水反应生成氢氧化钠 | I对;II错;无关系 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | I对;II对;有关系 |
| D | 过氧化钠可用作航天员的供氧剂 | Na2O2能和CO2、H2O反应生成O2 | I对;II对;有关系 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-07更新
|
91次组卷
|
2卷引用: 陕西省咸阳市高新一中2023-2024学年高一上学期第二次质量检测化学试题
6 . 在给定条件下,下列选项所示的物质间转化均能实现的是
A. |
B. |
C.稀盐酸 漂白粉 漂白粉 |
D.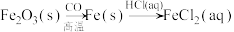 |
您最近一年使用:0次
7 . 下列有关物质的性质与用途具有对应关系的是
| A.钠具有导电性,可用于冶炼部分金属 |
| B.小苏打能与碱反应,可用于治疗胃酸过多 |
| C.次氯酸具有弱酸性,可用作漂白剂 |
| D.Na2O2能吸收CO2产生O2,可用作呼吸面具的供氧剂 |
您最近一年使用:0次
解题方法
8 . 某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
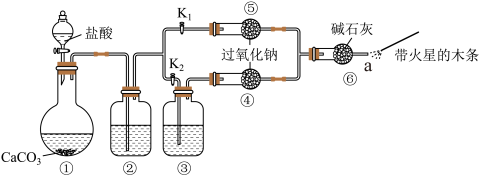
(1)装置①中盛放盐酸的仪器是___________ 。
(2)已知盐酸具有挥发性。装置②中的试剂是饱和 溶液,②中反应的离子方程式是
溶液,②中反应的离子方程式是___________ 。
(3)装置③中的试剂是___________ 。
(4)步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤1和步骤2中,a处带火星的木条产生的实验现象分别是___________ 、___________ 。
(5)下列说法正确的是___________ 。
A.金属钠的氧化物都是淡黄色的固体
B.金属钠的密度比水小
C.纯碱和小苏打都能溶于水
D.氢氧化钠是白色固体,能溶于水
E.氧化钠的阴阳离子比是 ,过氧化钠的阴阳离子比是
,过氧化钠的阴阳离子比是

(1)装置①中盛放盐酸的仪器是
(2)已知盐酸具有挥发性。装置②中的试剂是饱和
 溶液,②中反应的离子方程式是
溶液,②中反应的离子方程式是(3)装置③中的试剂是
(4)步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
(5)下列说法正确的是
A.金属钠的氧化物都是淡黄色的固体
B.金属钠的密度比水小
C.纯碱和小苏打都能溶于水
D.氢氧化钠是白色固体,能溶于水
E.氧化钠的阴阳离子比是
 ,过氧化钠的阴阳离子比是
,过氧化钠的阴阳离子比是
您最近一年使用:0次
名校
解题方法
9 . 现有一定量含有 杂质的
杂质的 试样,用如图所示的实验装置测定
试样,用如图所示的实验装置测定 试样的纯度(通过
试样的纯度(通过 与样品反应后生成
与样品反应后生成 的量测定
的量测定 的含量。可供选用的反应物:
的含量。可供选用的反应物: 固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
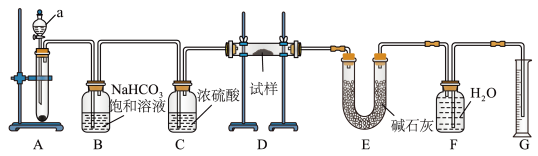
(1)装置 的名称为
的名称为_______ 。
(2)写出装置B中除杂反应的离子方程式_______ 。
(3)写出装置D中反应的化学方程式_______ 。
(4)装置 中碱石灰的主要作用是
中碱石灰的主要作用是_______ ,如果缺少 装置会导致测定结果
装置会导致测定结果_______ 。(填“偏大”、“偏小”、“无影响”)
(5)已知装置 中试样质量为
中试样质量为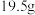 ,装置
,装置 中所得
中所得 体积为
体积为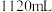 (已折算成标准状况下体积,且
(已折算成标准状况下体积,且 全部逸出)。求试样中
全部逸出)。求试样中 的质量分数
的质量分数_______ 。
(6)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是______________。
与水的反应,下列说法正确的是______________。
 杂质的
杂质的 试样,用如图所示的实验装置测定
试样,用如图所示的实验装置测定 试样的纯度(通过
试样的纯度(通过 与样品反应后生成
与样品反应后生成 的量测定
的量测定 的含量。可供选用的反应物:
的含量。可供选用的反应物: 固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
(1)装置
 的名称为
的名称为(2)写出装置B中除杂反应的离子方程式
(3)写出装置D中反应的化学方程式
(4)装置
 中碱石灰的主要作用是
中碱石灰的主要作用是 装置会导致测定结果
装置会导致测定结果(5)已知装置
 中试样质量为
中试样质量为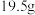 ,装置
,装置 中所得
中所得 体积为
体积为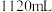 (已折算成标准状况下体积,且
(已折算成标准状况下体积,且 全部逸出)。求试样中
全部逸出)。求试样中 的质量分数
的质量分数(6)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是______________。
与水的反应,下列说法正确的是______________。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
您最近一年使用:0次
名校
解题方法
10 . 过量的 与
与 混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是
混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是
 与
与 混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是
混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是A. 和 和 | B. 和 和 | C. | D. 和 和 |
您最近一年使用:0次
2024-03-13更新
|
93次组卷
|
2卷引用:河南省南阳市第一中学校2023-2024学年高一上学期第四次月考化学试题



