1 . 爆炸盐( )是一种日常生活中的无机盐,白色粉末,易溶于水,遇水后迅速分解产生氧气和水。它可以用作洗涤助剂、漂白剂和园艺用品。下列有关爆炸盐的说法正确的是
)是一种日常生活中的无机盐,白色粉末,易溶于水,遇水后迅速分解产生氧气和水。它可以用作洗涤助剂、漂白剂和园艺用品。下列有关爆炸盐的说法正确的是
 )是一种日常生活中的无机盐,白色粉末,易溶于水,遇水后迅速分解产生氧气和水。它可以用作洗涤助剂、漂白剂和园艺用品。下列有关爆炸盐的说法正确的是
)是一种日常生活中的无机盐,白色粉末,易溶于水,遇水后迅速分解产生氧气和水。它可以用作洗涤助剂、漂白剂和园艺用品。下列有关爆炸盐的说法正确的是A.漂白原理与 相同 相同 |
| B.溶于水后所得溶液呈中性,该反应为氧化还原反应 |
| C.0.1mol爆炸盐与足量的酸性高锰酸钾溶液反应生成标准状况下11.2L气体 |
| D.可与硫、磷等在同一个药品柜中存放 |
您最近一年使用:0次
2 . 类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实验的验证。下列类推的结论正确的是
A. 与 与 反应生成 反应生成 ,则 ,则 与 与 反应生成 反应生成 |
B.Fe与 反应生成 反应生成 ,则Fe与 ,则Fe与 反应生成 反应生成 |
C.F与Cl同主族, 与 与 反应生成HClO,则 反应生成HClO,则 与 与 反应生成HFO 反应生成HFO |
| D.钠和钾保存在煤油里,则金属锂也保存在煤油里 |
您最近一年使用:0次
名校
3 . 下列说法正确的有几个
(1)高温下,0.2molFe与足量水蒸气反应,生成的 分子数目为
分子数目为
(2)任何气体的气体摩尔体积都约为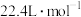
(3)常温常压下,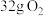 与
与 的混合气体所含原子数为
的混合气体所含原子数为
(4)同温同体积时,气体的物质的量越大,则压强越大
(5)两种物质的物质的量相同,则它们在标准状况下的体积也相同
(6)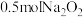 固体中含有阴离子的数目为
固体中含有阴离子的数目为
(7)足量的浓盐酸与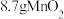 反应,被氧化的HCl为0.2mol
反应,被氧化的HCl为0.2mol
(8)1mol/L的 溶液中,
溶液中, 离子的数目为
离子的数目为
(9)Na与水反应时,水表现出氧化性
(10)Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取
(11)Na2O2与CO2反应生成Na2CO3和O2,故Na2O2与SO2反应生成Na2SO3和O2
(12)热稳定性:HCl>H2S>PH3
(13)离子半径:O2->Al3+>Na+
(14)元素原子失电子能力:Be>K>Mg
(15)F2能从NaCl水溶液中置换出Cl2
(1)高温下,0.2molFe与足量水蒸气反应,生成的
 分子数目为
分子数目为
(2)任何气体的气体摩尔体积都约为
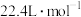
(3)常温常压下,
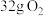 与
与 的混合气体所含原子数为
的混合气体所含原子数为
(4)同温同体积时,气体的物质的量越大,则压强越大
(5)两种物质的物质的量相同,则它们在标准状况下的体积也相同
(6)
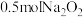 固体中含有阴离子的数目为
固体中含有阴离子的数目为
(7)足量的浓盐酸与
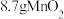 反应,被氧化的HCl为0.2mol
反应,被氧化的HCl为0.2mol(8)1mol/L的
 溶液中,
溶液中, 离子的数目为
离子的数目为
(9)Na与水反应时,水表现出氧化性
(10)Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取
(11)Na2O2与CO2反应生成Na2CO3和O2,故Na2O2与SO2反应生成Na2SO3和O2
(12)热稳定性:HCl>H2S>PH3
(13)离子半径:O2->Al3+>Na+
(14)元素原子失电子能力:Be>K>Mg
(15)F2能从NaCl水溶液中置换出Cl2
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
名校
4 . 二氧化硫和亚硫酸在工农业生产中具有重要的用途。某化学兴趣小组对SO2和H2SO3的一些性质进行了探究。
Ⅰ.探究SO2的性质_______ ;关闭旋塞2,打开旋塞1,注入硫酸至浸没三颈烧瓶中的固体,反应的化学方程式为_______ 。
(2)装置B中试剂X是_______ ,装置C中发生反应的化学方程式:_______ ,装置D中NaOH溶液的作用是_______ 。
Ⅱ.探究H2SO3的酸性强于HClO(可能需要的装置和试剂如图所示)_______ (填字母),装置J中反应的离子方程式为_______ 。
(4)能证明H2SO3的酸性强于HClO的实验现象是_______ 。
Ⅰ.探究SO2的性质
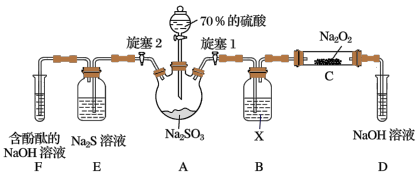
(2)装置B中试剂X是
Ⅱ.探究H2SO3的酸性强于HClO(可能需要的装置和试剂如图所示)

(4)能证明H2SO3的酸性强于HClO的实验现象是
您最近一年使用:0次
名校
5 . 下列有关 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是A.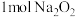 固体中所含有离子总数约为 固体中所含有离子总数约为 |
B. 和 和 的反应产物 的反应产物 和氧气 和氧气 |
C.向酚酞溶液中加 ,溶液先变红后褪色 ,溶液先变红后褪色 |
D.取久置的 粉末,向其中滴加过量的盐酸,产生无色气体, 粉末,向其中滴加过量的盐酸,产生无色气体, 没有变质 没有变质 |
您最近一年使用:0次
6 . 下列化学方程式或离子方程式书写正确的是
A. 与 与 反应: 反应: |
B.侯氏制碱法: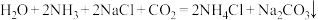 |
C. 与 与 反应: 反应: |
D.漂白粉的制备: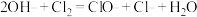 |
您最近一年使用:0次
7 . 下列实验操作、现象和结论均正确的是
| 选项 | 操作及现象 | 结论 |
| A | 向含淀粉的KI溶液中滴加氯水,溶液变蓝 | 氯的非金属性比碘的强 |
| B | 在FeSO4溶液中加入Na2O2,产生红褐色沉淀 | FeSO4已变质 |
| C | 在铝片上滴加浓硝酸,无明显现象 | 铝不和浓硝酸反应 |
| D | 在蔗糖中滴加浓硫酸,产生黑色固体并放出气体 | 浓硫酸表现吸水性和还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-07-23更新
|
85次组卷
|
3卷引用:湖南省湘西土家族苗族自治州2023-2024学年高一下学期期末考试化学试卷
8 . 下列化学方程式正确的是
A.过氧化钠和SO2反应: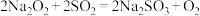 |
B.甲苯和Cl2光照下的反应: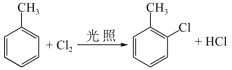 |
C.乙二醇的催化氧化: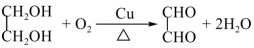 |
D.甲醛和足量新制氢氧化铜悬浊液反应: |
您最近一年使用:0次
9 .  具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中错误的是
具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中错误的是
 具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中错误的是
具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中错误的是A. 与炭、铝粉等还原性物质的燃烧实验可以在硬质玻璃管中进行 与炭、铝粉等还原性物质的燃烧实验可以在硬质玻璃管中进行 |
B. 与木炭反应时 与木炭反应时 表现出强氧化性 表现出强氧化性 |
C. 与 与 反应的方程式为 反应的方程式为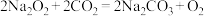 |
D. 与 与 反应可生成 反应可生成 |
您最近一年使用:0次
解题方法
10 . 甲、乙、丙、X是中学化学中常见的物质,在一定条件下,它们之间的转化关系如下图所示(部分产物已略去)。请回答下列问题:
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的化学方程式_____ 。
(3)若X是一种黄绿色气体,丙的结构特点可以证明甲的空间构型为正四面体形而非平面构型,则甲生成乙的化学方程式为______ 。
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与二氧化硫反应的化学方程式为_____ ;1 mol丙与SO2充分反应时转移电子的物质的量为______ mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。则甲的分子式可能是______ ,保存丙溶液常加入少量X,其目的是_____ 。



| A.Na | B.N2 | C.S | D.Si |
(3)若X是一种黄绿色气体,丙的结构特点可以证明甲的空间构型为正四面体形而非平面构型,则甲生成乙的化学方程式为
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与二氧化硫反应的化学方程式为
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。则甲的分子式可能是
您最近一年使用:0次



