解题方法
1 . 氧、硫及其化合物应用广泛。 可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中
可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中 在液态
在液态 中被
中被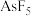 氧化成
氧化成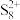 ,反应方程式为
,反应方程式为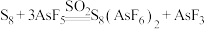 。氧能形成
。氧能形成 、
、 、
、 、
、 、
、 等重要氧化物。
等重要氧化物。 是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(
是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物( )等方法来制取。
)等方法来制取。 在
在 催化作用下与
催化作用下与 反应生成
反应生成 。下列关于化学反应的表示或说法正确的是
。下列关于化学反应的表示或说法正确的是
 可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中
可用作燃料电池的氧化剂。单质硫有多种同素异形体,其中 在液态
在液态 中被
中被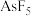 氧化成
氧化成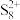 ,反应方程式为
,反应方程式为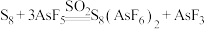 。氧能形成
。氧能形成 、
、 、
、 、
、 、
、 等重要氧化物。
等重要氧化物。 是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(
是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物( )等方法来制取。
)等方法来制取。 在
在 催化作用下与
催化作用下与 反应生成
反应生成 。下列关于化学反应的表示或说法正确的是
。下列关于化学反应的表示或说法正确的是A.碱性氢氧燃料电池的正极反应: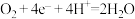 |
B. 与 与 反应: 反应: |
C. 与 与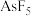 反应中,n(氧化剂):n(还原剂)=3:1 反应中,n(氧化剂):n(还原剂)=3:1 |
D.温度越高, 越大,硫酸钙制取 越大,硫酸钙制取 的反应正向进行程度越大 的反应正向进行程度越大 |
您最近一年使用:0次
2 . 过氧化钠有着独特的结构和性质,因而具有广泛的用途,如作为漂白剂,印染剂,空气中二氧化碳吸收剂,潜艇中供氧剂等。
(1)在下列溶液中分别加入一定量的过氧化钠固体,不会出现浑浊现象的是_______。
(2)关于 和
和 的异同,下列说法错误的是_______。
的异同,下列说法错误的是_______。
(3)下列各组物质相互混合进行反应,最终既有气体又有沉淀生成的是______。
(4)过氧化钠与单质硫都是淡黄色固体,请设计一个实验鉴别它们,描述预期现象和结论:_______ 。
(1)在下列溶液中分别加入一定量的过氧化钠固体,不会出现浑浊现象的是_______。
A.饱和 溶液 溶液 | B. 稀溶液 稀溶液 | C. 稀溶液 稀溶液 | D.饱和 |
(2)关于
 和
和 的异同,下列说法错误的是_______。
的异同,下列说法错误的是_______。| A.常温常压下状态相同,颜色不同 |
| B.包含的正负离子相同,但个数比不同 |
| C.均可由Na和氧气反应得到,但反应条件不同 |
| D.均可与水反应,但产物不同 |
(3)下列各组物质相互混合进行反应,最终既有气体又有沉淀生成的是______。
A.金属钠投入 溶液中 溶液中 | B. 投入 投入 溶液中 溶液中 |
C. 投入 投入 溶液中 溶液中 | D. 投入到 投入到 溶液中 溶液中 |
(4)过氧化钠与单质硫都是淡黄色固体,请设计一个实验鉴别它们,描述预期现象和结论:
您最近一年使用:0次
解题方法
3 . 过氧化钠可用于医药、印染、漂白等。某学习兴趣小组探究Na2O2与NO2、NO的反应,设计如图所示实验。

(1)盛放浓硝酸的仪器M名称为_________ ,A中发生反应的离子方程式为________ 。
(2)Na2O2与NO2反应,根据化合价升降原则有下列两种观点。
观点一:Na2O2氧化NO2,生成NaNO3;
观点二:NO2氧化Na2O2,生成O2。
为验证以上观点的正确性进行如下实验:
①关闭K2和弹簧夹,打开K1和A中仪器M的活塞,再将带火星的木条放在a处,观察到_______ 。甲同学认为观点二正确。
②乙同学认为该装置不能确认观点二正确,应在A、G之间增加一个装置,该装置的作用为______ 。改进后重复甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条没有复燃。判断观点一正确。
(3)丙同学根据NO易与O2反应,预测NO也易与Na2O2反应。
①丙同学关闭K1,打开K2,用上图的装置进行实验,为防止NO与空气中氧气反应,反应前的操作是___________ 。
②装置B的作用为___________ 。
③反应一段时间后,取D装置中产物少许,加入稀硫酸,产生无色气体遇到空气变为红棕色。完成反应的化学方程式:___________ 。
6___________ 4___________
4___________
④根据D装置中产物的判断结果,说明Na2O2与NO反应中Na2O2的作用是___________ 。(填标号)
A.氧化剂 B.还原剂 C.即是氧化剂也是还原剂

(1)盛放浓硝酸的仪器M名称为
(2)Na2O2与NO2反应,根据化合价升降原则有下列两种观点。
观点一:Na2O2氧化NO2,生成NaNO3;
观点二:NO2氧化Na2O2,生成O2。
为验证以上观点的正确性进行如下实验:
①关闭K2和弹簧夹,打开K1和A中仪器M的活塞,再将带火星的木条放在a处,观察到
②乙同学认为该装置不能确认观点二正确,应在A、G之间增加一个装置,该装置的作用为
(3)丙同学根据NO易与O2反应,预测NO也易与Na2O2反应。
①丙同学关闭K1,打开K2,用上图的装置进行实验,为防止NO与空气中氧气反应,反应前的操作是
②装置B的作用为
③反应一段时间后,取D装置中产物少许,加入稀硫酸,产生无色气体遇到空气变为红棕色。完成反应的化学方程式:
6___________
 4___________
4___________
④根据D装置中产物的判断结果,说明Na2O2与NO反应中Na2O2的作用是
A.氧化剂 B.还原剂 C.即是氧化剂也是还原剂
您最近一年使用:0次
4 . 下列关于Na2O2的说法不正确的是
| A.将一定量的Na2O2粉末加入滴有紫色石蕊溶液的水中并振荡,有气泡产生,最终溶液褪色 |
| B.向饱和NaOH溶液中放入一定量的Na2O2粉末,充分反应后恢复到原来温度,溶液pH不变,溶液中Na+数目不变 |
| C.将足量的Na2O2投入到盛有FeCl22溶液的试管中,有气泡产生,试管壁发烫,最终沉淀呈红褐色 |
| D.Na2O2的漂白原理与次氯酸、臭氧的相同,但与SO2、活性炭的漂白原理不同 |
您最近一年使用:0次
2023-12-04更新
|
98次组卷
|
2卷引用:上海市南洋中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
5 . 下列操作过程中实验现象的变化只有一次的是
| A.石蕊试液中逐滴滴加氯水 | B.酚酞试液中加入过氧化钠固体 |
| C.氢氧化铁胶体中逐滴滴加硫酸 | D.碳酸钠溶液中逐滴滴加盐酸 |
您最近一年使用:0次
2023-09-16更新
|
207次组卷
|
4卷引用:14-2023新东方高一上期中考化学14
名校
解题方法
6 . 向盛有少量Na2O2的密闭容器(体积不变)中通入SO2,测定容器中O2的含量随时间变化曲线如图
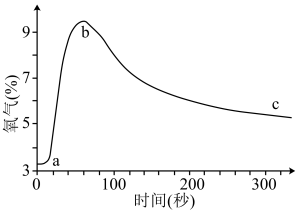
则下列说法错误的是

则下列说法错误的是
| A.ab段O2含量增加的原因:2Na2O2+2SO2=2Na2SO3+O2 |
| B.bc段O2含量缓慢降低的可能原因:反应生成O2的速率小于消耗O2的速率 |
| C.c点O2含量高于a点,则此时反应产物中含有Na2SO3 |
| D.取c点少量固体,加入BaCl2溶液有白色固体生成,证实有Na2SO4生成 |
您最近一年使用:0次
2022-10-17更新
|
187次组卷
|
3卷引用:陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷
7 . 有关Na2O2性质实验如下:
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
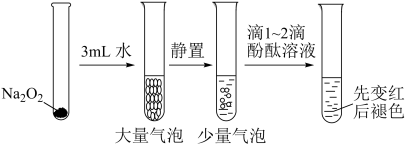
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
| A.双氧水能使酚酞褪色 |
| B.浓氢氧化钠能使酚酞褪色 |
| C.双氧水和浓氢氧化钠都能使酚酞褪色 |
| D.可利用二氧化锰和水来完善实验方案 |
您最近一年使用:0次
2022-06-14更新
|
2179次组卷
|
10卷引用:河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题
河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题江苏省盐城市亭湖高级中学2023-2024学年高一上学期期末考试化学试题上海市浦东新区2021-2022学年高三下学期教学质量检测化学试题上海市川沙中学2021-2022学年高一下学期期末考试化学试题(已下线)第二章《海水中的重要元素----钠和氯》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)上海市育才中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题内蒙古乌兰浩特第一中学2022-2023学年高一上学期第三次月考化学试题上海市建平中学2022-2023学年高一下学期期中考试化学试题湖北省十堰市郧阳中学2022-2023学年高一上学期10月月考化学试题



