解题方法
1 . 高氯酸铜晶体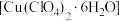 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
Ⅰ.称取12.5g 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀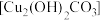 ;
;
Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70% 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;
Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g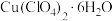 晶体。
晶体。
回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是________ ,“步骤Ⅴ”中蒸发需要用到下列仪器中的________ (填字母序号). 和
和 研细的目的是
研细的目的是________________ ,写出它们在溶液中反应生成 的离子方程式:
的离子方程式:________________ ,实际操作中 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是________________ 。
(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为________ 。
(4)“步骤Ⅴ”在通风橱中进行的原因是________________ 。
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)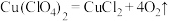 ;(B)
;(B)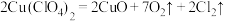 ,若测得
,若测得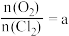 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为________ (用含a的代数式表示)。
(6)上述过程中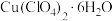 的产率为
的产率为________ 。
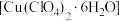 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:Ⅰ.称取12.5g
 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀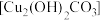 ;
;Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70%
 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g
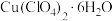 晶体。
晶体。回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是
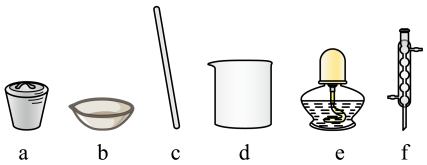
 和
和 研细的目的是
研细的目的是 的离子方程式:
的离子方程式: 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为
(4)“步骤Ⅴ”在通风橱中进行的原因是
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)
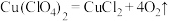 ;(B)
;(B)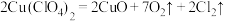 ,若测得
,若测得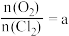 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为(6)上述过程中
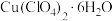 的产率为
的产率为
您最近一年使用:0次
2024-05-20更新
|
80次组卷
|
2卷引用:河南省九师联盟2023-2024学年高三下学期5月月考理综试题-高中化学
名校
解题方法
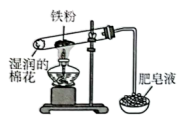
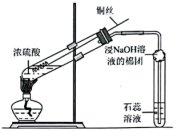
2 . 用下列仪器或装置进行相应实验,描述正确的是
|
|
|
|
| A.该装置可用于验证铁粉与水蒸气的反应 | B.用该装置制备氧气,关闭右侧止水夹后,反应停止 | C.试管中逐渐有气泡产生,石蕊溶液先变红后不褪色 | D.上述装置用于鉴别 溶液和 溶液和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-03更新
|
285次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一下学期3月月考化学试题
解题方法
3 . 以酚酞为指示剂,用 的盐酸标准溶液滴定某未知浓度的Na2CO3溶液,以测定Na2CO3的浓度。下列说法错误的是
的盐酸标准溶液滴定某未知浓度的Na2CO3溶液,以测定Na2CO3的浓度。下列说法错误的是
 的盐酸标准溶液滴定某未知浓度的Na2CO3溶液,以测定Na2CO3的浓度。下列说法错误的是
的盐酸标准溶液滴定某未知浓度的Na2CO3溶液,以测定Na2CO3的浓度。下列说法错误的是| A.以甲基橙为指示剂也可以达到相应的实验目的 |
| B.准确移取Na2CO3溶液于锥形瓶中,若又加入少量蒸馏水,对滴定结果无影响 |
| C.滴定时,当观察到锥形瓶内溶液颜色由浅红色变为无色时,即可判断达到滴定终点 |
| D.滴定结束后若仰视观察滴定管中液面刻度读数,则测定结果偏大(滴定前读数正确) |
您最近一年使用:0次
名校
解题方法
4 . 劳动是创造物质财富和精神财富的过程,是人类特有的基本社会实践活动。下列生产活动所对应的化学知识正确的是
选项 | 生产活动 | 化学知识 |
A | 用铁罐车运输浓硝酸 | 常温下,铁与浓硝酸不反应 |
B | 制作馒头时加入苏打 | 苏打受热易分解,产生的气体能使馒头疏松多孔 |
C | 给农作物施用磷酸氢二铵 | N、P是植物生长的营养元素 |
D | 用漂白粉给游泳池杀菌 | 漂白粉中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-27更新
|
214次组卷
|
3卷引用:河南省创新发展联盟2023-2024学年高一下学期3月月考化学试题
解题方法
5 . 某兴趣小组用下列装置探究膨松剂反应时单位质量产生标准状况下气体的体积。下列说法不正确的是
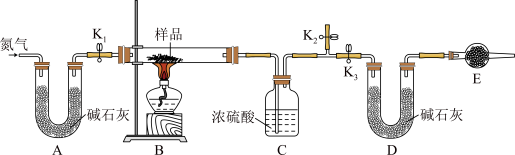

| A.实验装置组装好之后,要先检查装置的气密性 |
B.E装置中盛放的试剂可以用无水 |
| C.加热前鼓入氮气数分钟,目的是除去装置中的水蒸气和二氧化碳 |
D.实验装置B中发生反应的化学方程式为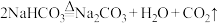 |
您最近一年使用:0次
6 . 写出下列物质的颜色及状态。
①Na2O___________ ;②Na2O2 ___________ ;③Na2CO3 ___________ ;④FeO___________ ;
⑤Fe2O3___________ ;⑥Fe3O4___________ ;⑦Fe(OH)2___________ ;⑧Fe(OH)3___________ ;
⑨Na___________ ;⑩铁粉___________ 。
①Na2O
⑤Fe2O3
⑨Na
您最近一年使用:0次
7 . 化学与人类社会的生产、生活有着密切联系。下列叙述错误的是
| A.面食点心加工时加入少量小苏打能使点心松软可口 |
B.葡萄酒中添加的微量 的作用是杀菌、抗氧化 的作用是杀菌、抗氧化 |
C. 胶体具有吸附性,可用于自来水的杀菌消毒 胶体具有吸附性,可用于自来水的杀菌消毒 |
| D.石油裂解的主要目的是获得乙烯和丙烯等基础化工原料 |
您最近一年使用:0次
解题方法
8 . 基于核心元素的化合价和物质类别研究物质,为我们认识物质性质和实现物质转化提供了新思路,碳元素的价一类二维图如图所示。下列说法错误的是
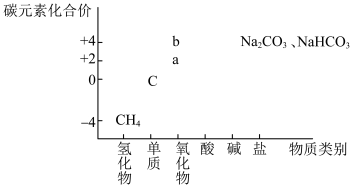

| A.NaHCO3可用作胃酸中和剂 | B.a、b互为同素异形体 |
| C.a不属于酸性氧化物 | D.a→b→c可实现一步转化 |
您最近一年使用:0次
解题方法
9 . 写出对应的化学式。
(1)六大强酸:_______ 、_______ 、_______ 、_______ 、_______ 、_______ 。
(2)四大强碱:_______ 、_______ 、_______ 、_______ 。
(3)苛性钠:_______ ;纯碱:_______ ;苏打:_______ ;小苏打:_______ ;胆矾:_______ 。
(1)六大强酸:
(2)四大强碱:
(3)苛性钠:
您最近一年使用:0次
名校
10 . 某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图1所示(部分产物已略去):
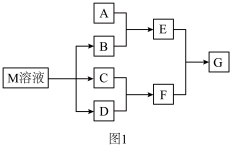
(1)写出B的水溶液中电离方程式_______ 。
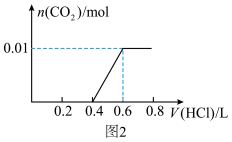
(2)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,生成的CO2物质的量与所用盐酸体积如图2所示,则A与B溶液反应后溶液中所有溶质的化学式为_______ ;c(HCl)=_______ mol/L。
(3)若A是地壳中含量最多的金属单质,将A的氯化物和氢氧化钠溶液等体积混合,得到的沉淀物中与溶液中A元素的质量相等,则A的氯化物溶液和氢氧化钠溶液的物质的量浓度之比可能为_______ 。
Ⅱ.磷元素的含氧酸有 (磷酸)、
(磷酸)、 (亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠
(亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠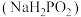 的化学方程式为
的化学方程式为 ,则
,则
(4) 属于
属于_______ (填“正盐”、“酸式盐”或“碱式盐”)。
(5) (亚磷酸)具有较强的还原性,能被酸性
(亚磷酸)具有较强的还原性,能被酸性 溶液氧化为
溶液氧化为 (磷酸),其中涉及的离子方程式为:
(磷酸),其中涉及的离子方程式为:_______ 。

(1)写出B的水溶液中电离方程式
(2)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,生成的CO2物质的量与所用盐酸体积如图2所示,则A与B溶液反应后溶液中所有溶质的化学式为

(3)若A是地壳中含量最多的金属单质,将A的氯化物和氢氧化钠溶液等体积混合,得到的沉淀物中与溶液中A元素的质量相等,则A的氯化物溶液和氢氧化钠溶液的物质的量浓度之比可能为
Ⅱ.磷元素的含氧酸有
 (磷酸)、
(磷酸)、 (亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠
(亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠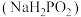 的化学方程式为
的化学方程式为 ,则
,则(4)
 属于
属于(5)
 (亚磷酸)具有较强的还原性,能被酸性
(亚磷酸)具有较强的还原性,能被酸性 溶液氧化为
溶液氧化为 (磷酸),其中涉及的离子方程式为:
(磷酸),其中涉及的离子方程式为:
您最近一年使用:0次



 具有强氧化性,能杀菌消毒
具有强氧化性,能杀菌消毒

