1 . 下列实验设计及原理都错误的是
选项 | 实验设计 | 原理 |
A | 利用NaOH溶液鉴别Al与Mg | Al会与NaOH溶液反应,而Mg不与其反应 |
B | 分别加热Na2CO3与NaHCO3固体,并将可能产生的气体通入澄清石灰水,鉴别Na2CO3与NaHCO3 | 碳酸氢钠受热易分解,生成的CO2使澄清石灰水变浑浊 |
C | 利用苯鉴别碘单质与高锰酸钾 | 二者在苯中的溶解度不同 |
D | 利用紫色石蕊试液鉴别二氧化碳与二氧化硫 | SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 某种天然碱的化学式为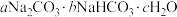 ,某实验小组欲测定该天然碱中
,某实验小组欲测定该天然碱中 与
与 的比例,进行了如下实验。回答下列问题
的比例,进行了如下实验。回答下列问题
(1)配制一定物质的量浓度的稀盐酸溶液。
①若要配制250mL 稀盐酸,需量取
稀盐酸,需量取 的浓盐酸
的浓盐酸__________  (计算结果保留1位小数)。
(计算结果保留1位小数)。
②配制溶液过程中,下列关于容量瓶的操作,正确的是__________ (填字母,下同)。
A.检验容量瓶是否漏水 B.定容
B.定容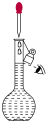
C.转移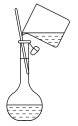 D.摇匀
D.摇匀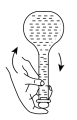
③下列情况会使所配溶液浓度偏低的是__________ 。
A.容量瓶清洗后,未经过干燥处理
B.转移时,没有洗涤烧杯和玻璃棒
C.溶液未经冷却直接倒入容量瓶中
D.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)取一定质量该天然碱溶于水,逐滴加入稀盐酸,溶液中 的物质的量与加入
的物质的量与加入 的物质的量关系如图所示。
的物质的量关系如图所示。
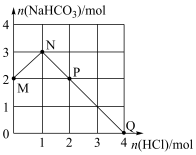
①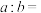
__________ ;
②P点处溶液中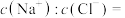
__________ ;
③若Q点时溶液体积为5L,则溶液中 的浓度为
的浓度为__________ ;
④“M→N”过程中发生反应的离子方程式是____________________ 。
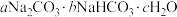 ,某实验小组欲测定该天然碱中
,某实验小组欲测定该天然碱中 与
与 的比例,进行了如下实验。回答下列问题
的比例,进行了如下实验。回答下列问题(1)配制一定物质的量浓度的稀盐酸溶液。
①若要配制250mL
 稀盐酸,需量取
稀盐酸,需量取 的浓盐酸
的浓盐酸 (计算结果保留1位小数)。
(计算结果保留1位小数)。②配制溶液过程中,下列关于容量瓶的操作,正确的是
A.检验容量瓶是否漏水
 B.定容
B.定容
C.转移
 D.摇匀
D.摇匀
③下列情况会使所配溶液浓度偏低的是
A.容量瓶清洗后,未经过干燥处理
B.转移时,没有洗涤烧杯和玻璃棒
C.溶液未经冷却直接倒入容量瓶中
D.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)取一定质量该天然碱溶于水,逐滴加入稀盐酸,溶液中
 的物质的量与加入
的物质的量与加入 的物质的量关系如图所示。
的物质的量关系如图所示。
①
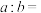
②P点处溶液中
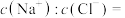
③若Q点时溶液体积为5L,则溶液中
 的浓度为
的浓度为④“M→N”过程中发生反应的离子方程式是
您最近一年使用:0次
名校
3 . 钠的化合物存在广泛,下列说法错误的是
A.溶解度(室温,g/100 g水):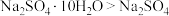 |
B.热稳定性: |
C.水解平衡常数 (同温): (同温):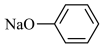 > >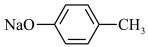 |
D.化学键中的离子键百分数: |
您最近一年使用:0次
2024-03-05更新
|
952次组卷
|
5卷引用:2024届辽宁省名校联盟(东北三省联考)高三下学期模拟预测化学试题
2024届辽宁省名校联盟(东北三省联考)高三下学期模拟预测化学试题(已下线)选择题1-5(已下线)化学(辽宁卷02)-2024年高考押题预测卷(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024年山东省潍坊市高三下学期高考模拟训练调研试题(二)
4 . 化学与人类生产、生活密切相关,下列说法中错误的是
| A.歼-20上采用的氮化镓涂层,属于新型金属材料 |
| B.液晶既有液体的流动性,又有类似晶体的各向异性 |
| C.氯化钠不能使蛋白质变性,但可用作食品防腐剂 |
| D.碳酸氢铵、碳酸氢钠可用于制作面包等食品的膨松剂 |
您最近一年使用:0次
2024-01-13更新
|
1383次组卷
|
8卷引用:辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题
辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题2024届辽宁省沈阳市高三教学质量检测(一模)化学试题辽宁省沈阳市2024届高三一模化学试题(已下线)选择题1-5(已下线)热点01 化学与STSE、化学与传统文化(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)选择题6-10(已下线)选择题1-6
名校
5 . 下列说法正确的是
A. 为强电解质,液态氯化氢可导电 为强电解质,液态氯化氢可导电 |
| B.做面条时可添加适量碳酸氢钠增强口感与韧性 |
C.向饱和食盐水中通入过量 ,能得到 ,能得到 晶体 晶体 |
| D.硫酸钡难溶于水,属于强电解质 |
您最近一年使用:0次
6 . 钠及其化合物广泛应用于生产生活中,回答下列关于钠及其化合物的问题。
(1)实验室需要配制450mL0.1mol/LNaOH溶液,下列仪器一定不需要的是___________ (填仪器名称)。
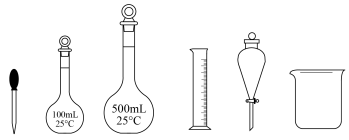
(2)计算需要用托盘天平称量的NaOH固体的质量为___________ g。
(3)配制过程中,下列操作将导致溶液浓度偏大的是___________(填字母)。
(4)由于操作失误,配制的NaOH溶液浓度不准确,为了测定NaOH溶液的准确浓度并探究相关化学反应,取两份上述100mLNaOH溶液,分别向其中通入不同体积的 气体,充分反应后溶液中的溶质组成不可能是___________(填字母)。
气体,充分反应后溶液中的溶质组成不可能是___________(填字母)。
(5)向(4)得到的两份溶液中滴加0.1mol/L盐酸,产生气体的体积与加入盐酸的体积关系如图所示。
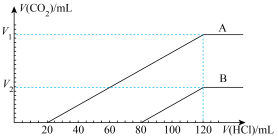
①由图可得,曲线A对应的溶液通入 过程的总反应的离子方程式为
过程的总反应的离子方程式为___________ 。
②曲线B对应的溶液加入盐酸后共产生 气体
气体___________ mL(标准状况)。
③通入 前NaOH溶液浓度为
前NaOH溶液浓度为___________ mol/L。
(6)我国化学家侯德榜先生提出的“联合制碱法”是以氯化钠、二氧化碳、氨和水为原料制取纯碱,并产生副产品氯化铵的过程,其中生成 的反应原理为
的反应原理为___________ (用离子方程式表示),下列有关说法正确的是___________ (填字母)。
A.“联合制碱法”中 来自煅烧石灰石
来自煅烧石灰石
B.母液吸氨可使 转化为
转化为 ,提高析出氯化铵的纯度
,提高析出氯化铵的纯度
C.“联合制碱法”的工艺过程中应用了物质溶解度的差异
D.生成的氯化铵可用于氮肥,提高原料利用率
(1)实验室需要配制450mL0.1mol/LNaOH溶液,下列仪器一定不需要的是

(2)计算需要用托盘天平称量的NaOH固体的质量为
(3)配制过程中,下列操作将导致溶液浓度偏大的是___________(填字母)。
| A.溶解后的溶液未经冷却就转移到容量瓶中 |
| B.容量瓶曾经盛装过0.1mol/LNaOH溶液,未经清洗就直接使用 |
| C.称量NaOH固体时间过长,发生潮解 |
| D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯和玻璃棒 |
(4)由于操作失误,配制的NaOH溶液浓度不准确,为了测定NaOH溶液的准确浓度并探究相关化学反应,取两份上述100mLNaOH溶液,分别向其中通入不同体积的
 气体,充分反应后溶液中的溶质组成不可能是___________(填字母)。
气体,充分反应后溶液中的溶质组成不可能是___________(填字母)。A. 和 和 | B. 和 和 |
C. 、 、 和 和 | D. |
(5)向(4)得到的两份溶液中滴加0.1mol/L盐酸,产生气体的体积与加入盐酸的体积关系如图所示。

①由图可得,曲线A对应的溶液通入
 过程的总反应的离子方程式为
过程的总反应的离子方程式为②曲线B对应的溶液加入盐酸后共产生
 气体
气体③通入
 前NaOH溶液浓度为
前NaOH溶液浓度为(6)我国化学家侯德榜先生提出的“联合制碱法”是以氯化钠、二氧化碳、氨和水为原料制取纯碱,并产生副产品氯化铵的过程,其中生成
 的反应原理为
的反应原理为A.“联合制碱法”中
 来自煅烧石灰石
来自煅烧石灰石B.母液吸氨可使
 转化为
转化为 ,提高析出氯化铵的纯度
,提高析出氯化铵的纯度C.“联合制碱法”的工艺过程中应用了物质溶解度的差异
D.生成的氯化铵可用于氮肥,提高原料利用率
您最近一年使用:0次
2023-12-12更新
|
225次组卷
|
3卷引用:辽宁省部分学校2023-2024学年高一上学期12月月考化学试题
7 . 钠是一种活泼金属,其化合物在生产生活中具有广泛应用.
(1)下列有关钠及其化合物的说法正确的是___________.
(2)将一小块钠迅速投入到热坩埚中,发生反应的化学方程式为___________ .
(3)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液紫色褪去,说明
粉末,观察到溶液紫色褪去,说明 具有一定的
具有一定的___________ (填“氧化性”、“还原性”或“漂白性”).
(4)下列试剂可以鉴别 溶液和
溶液和 溶液的是
溶液的是___________ .
A. 溶液 B.
溶液 B. 溶液 C.稀盐酸
溶液 C.稀盐酸
(5)在标准状况下,将 的
的 通入到
通入到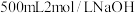 溶液中.
溶液中.
其中 的质量为
的质量为___________ 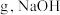 的物质的量为
的物质的量为___________  ,反应的离子方程式为
,反应的离子方程式为___________ .
(1)下列有关钠及其化合物的说法正确的是___________.
| A.钠元素在自然界中都以化合物的形式存在 | B.在实验室中少量钠保存在煤油中 |
C. 常用来治疗胃酸过多 常用来治疗胃酸过多 | D.热稳定性: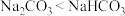 |
(3)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液紫色褪去,说明
粉末,观察到溶液紫色褪去,说明 具有一定的
具有一定的(4)下列试剂可以鉴别
 溶液和
溶液和 溶液的是
溶液的是A.
 溶液 B.
溶液 B. 溶液 C.稀盐酸
溶液 C.稀盐酸(5)在标准状况下,将
 的
的 通入到
通入到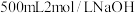 溶液中.
溶液中.其中
 的质量为
的质量为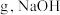 的物质的量为
的物质的量为 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。联合制碱法的工艺流程简化为如图所示流程。

(1)流程中“方框”内的物质属于电解质的有___________ 种。
(2)实验室完成操作Ⅰ所需要的玻璃仪器有___________ ,反应Ⅱ的化学方程式为___________ 。
(3)设计实验检验 样品中含有
样品中含有 ;取样品加水溶解,
;取样品加水溶解,___________ ,样品中含有 。
。
(4)某小组同学采用如下实验探究碳酸钠和碳酸氢钠的性质。
①取两支试管分别加入 的碳酸钠和碳酸氢钠固体,再分别加入几滴水振荡试管,用手触摸试管底部,温度较高的是
的碳酸钠和碳酸氢钠固体,再分别加入几滴水振荡试管,用手触摸试管底部,温度较高的是___________ (填化学式,下同);继续向两支试管中分别加入 水,充分振荡,最先溶解完全的是
水,充分振荡,最先溶解完全的是___________ 。
②按如图所示方式进行实验,观察到的现象有开始无气泡,溶液颜色由红色变为浅红色,最后出现大量气泡。

请用离子方程式解释,“开始无气泡”的原因:___________ ,“最后出现大量气泡”的原因:___________ 。

(1)流程中“方框”内的物质属于电解质的有
(2)实验室完成操作Ⅰ所需要的玻璃仪器有
(3)设计实验检验
 样品中含有
样品中含有 ;取样品加水溶解,
;取样品加水溶解, 。
。(4)某小组同学采用如下实验探究碳酸钠和碳酸氢钠的性质。
①取两支试管分别加入
 的碳酸钠和碳酸氢钠固体,再分别加入几滴水振荡试管,用手触摸试管底部,温度较高的是
的碳酸钠和碳酸氢钠固体,再分别加入几滴水振荡试管,用手触摸试管底部,温度较高的是 水,充分振荡,最先溶解完全的是
水,充分振荡,最先溶解完全的是②按如图所示方式进行实验,观察到的现象有开始无气泡,溶液颜色由红色变为浅红色,最后出现大量气泡。

请用离子方程式解释,“开始无气泡”的原因:
您最近一年使用:0次
2023-11-13更新
|
139次组卷
|
2卷引用:辽宁省朝阳市名校联考2023-2024学年高一上学期期中考试化学试题
23-24高三上·江西赣州·期中
9 . 下列各组物质的鉴别方法错误的是
| 选项 | 物质 | 鉴别方法 |
| A | CO(g)和 | 分别通入澄清石灰水 |
| B |  和 和 | 分别取少许试剂加入金属钠 |
| C | 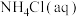 和 和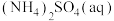 | 分别取少许试剂加入 溶液 溶液 |
| D |  和 和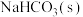 | 分别取少许固体加入盐酸中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-10更新
|
159次组卷
|
3卷引用:选择题1-5
解题方法
10 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,下图为钠的价类二维图,请回答以下问题:
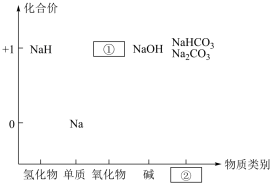
(1)图上中缺失的物质类别②是___________ ,NaH可用作野外生氢剂,反应原理为:NaH+H2O=H2↑+NaOH;则该反应中氧化产物与还原产物的质量之比为___________ 。
(2)下列有关说法正确的是___________。
(3)利用如图实验装置比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ 除加热外,还可用来鉴别NaHCO3溶液和Na2CO3溶液的是___________ 。
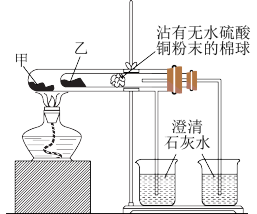
A.Ba(OH)2 B.NaOH溶液 C.稀盐酸
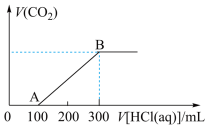
(4)向NaOH溶液中通入CO2后得到溶液M。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入的盐酸的体积V(HCI)的关系如图所示。则溶液M中的溶质为___________ OA段发生反应的离子方程式为___________ 。

(1)图上中缺失的物质类别②是
(2)下列有关说法正确的是___________。
| A.钠与硫酸铜溶液反应,可以置换出单质铜 |
| B.钠的两种常见氧化物都是碱性氧化物 |
| C.工业上主要采用电解饱和食盐水的方法来制取NaOH |
| D.1mol过氧化钠与2mol碳酸氢钠固体混合,在密闭容器中加热充分反应后,排出气体物质冷却,残留的固体物质是Na2CO3和NaOH |
(3)利用如图实验装置比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

A.Ba(OH)2 B.NaOH溶液 C.稀盐酸
(4)向NaOH溶液中通入CO2后得到溶液M。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入的盐酸的体积V(HCI)的关系如图所示。则溶液M中的溶质为

您最近一年使用:0次



