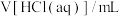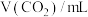名校
1 . 向某NaOH溶液分别通入不同量的 气体,得到A、B、C三种溶液。分别向这三种溶液中滴入
气体,得到A、B、C三种溶液。分别向这三种溶液中滴入 的盐酸,得到的气体变化如图。则:
的盐酸,得到的气体变化如图。则:_____ ;
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:_____ 。
(3)B溶液中原有的NaOH的物质的量为_____ 。
 气体,得到A、B、C三种溶液。分别向这三种溶液中滴入
气体,得到A、B、C三种溶液。分别向这三种溶液中滴入 的盐酸,得到的气体变化如图。则:
的盐酸,得到的气体变化如图。则: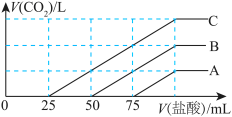
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:
(3)B溶液中原有的NaOH的物质的量为
您最近一年使用:0次
2 . 现有Na2CO3和NaHCO3的混合物共48.6g,加入足量盐酸时放出11.2L(标准状况)CO2,请求出:
(1)产生二氧化碳的物质的量是___________ ;
(2)混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
(1)产生二氧化碳的物质的量是
(2)混合物中Na2CO3和NaHCO3的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . 将Na2CO3和NaHCO3的混合物充分加热,生成的气体(假设无损耗)全部通入足量的石灰水中,得到20.0g白色沉淀,加热后的残留物加入200mL盐酸恰好完全反应,生成5.60LCO2气体(标准状况下)。试回答下列问题:
(1)所加盐酸的物质的量浓度为_______ mol/L。
(2)原混合物中碳酸钠的质量是_______ g。
(1)所加盐酸的物质的量浓度为
(2)原混合物中碳酸钠的质量是
您最近一年使用:0次
名校
解题方法
4 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)存贮时,Na应保存在___________ 中;实验室取用少量金属钠需要用到的实验用品有玻璃片、小刀、___________ 和___________ 等。
(2)工业上采用电解熔融NaCl(熔点为 )制备金属Na,电解反应方程式:
)制备金属Na,电解反应方程式: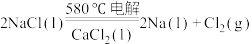 ,加入
,加入 的目的是
的目的是___________ (填序号)。
a.作催化剂,加块电解反应的速率
b.作还原剂,将 还原为
还原为
c.作助熔剂,降低生产过程的能耗
d.作氧化剂,将 氧化为
氧化为
(3)钠能与液氨反应,生成氨基钠(NaNH2)和一种气体单质。将钠投入液氨中,会快速得到深蓝色溶液(生成蓝色的溶剂合电子,如图所示),后慢慢产生气泡。
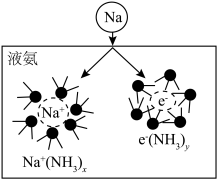
①生成的气体为___________ (填分子式)
②当 钠投入液氨生成
钠投入液氨生成 气体时,Na共失去的电子
气体时,Na共失去的电子___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(4)采用空气和Na为原料可直接制备Na2O2。为防止空气中的某些成分与Na2O2反应,空气与熔融金属Na反应前需依次通过___________ 。(填序号)
a.无水 b.饱和食盐水 c.饱和
b.饱和食盐水 c.饱和 溶液 d.
溶液 d. 溶液 e.
溶液 e. 溶液
溶液
(5)对固体 充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体
充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体 的质量为
的质量为___________ g。
(6)为确定 和
和 混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸
混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸 ,充分反应,产生
,充分反应,产生 的体积(已折算成标准状况下的体积,不考虑
的体积(已折算成标准状况下的体积,不考虑 在水中的溶解)如下表:
在水中的溶解)如下表:
①样品中物质的量之比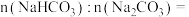
___________ 。
②稀盐酸的物质的量浓度
___________ mol/L。
(1)存贮时,Na应保存在
(2)工业上采用电解熔融NaCl(熔点为
 )制备金属Na,电解反应方程式:
)制备金属Na,电解反应方程式: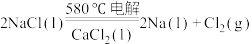 ,加入
,加入 的目的是
的目的是a.作催化剂,加块电解反应的速率
b.作还原剂,将
 还原为
还原为
c.作助熔剂,降低生产过程的能耗
d.作氧化剂,将
 氧化为
氧化为
(3)钠能与液氨反应,生成氨基钠(NaNH2)和一种气体单质。将钠投入液氨中,会快速得到深蓝色溶液(生成蓝色的溶剂合电子,如图所示),后慢慢产生气泡。

①生成的气体为
②当
 钠投入液氨生成
钠投入液氨生成 气体时,Na共失去的电子
气体时,Na共失去的电子 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(4)采用空气和Na为原料可直接制备Na2O2。为防止空气中的某些成分与Na2O2反应,空气与熔融金属Na反应前需依次通过
a.无水
 b.饱和食盐水 c.饱和
b.饱和食盐水 c.饱和 溶液 d.
溶液 d. 溶液 e.
溶液 e. 溶液
溶液(5)对固体
 充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体
充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体 的质量为
的质量为(6)为确定
 和
和 混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸
混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸 ,充分反应,产生
,充分反应,产生 的体积(已折算成标准状况下的体积,不考虑
的体积(已折算成标准状况下的体积,不考虑 在水中的溶解)如下表:
在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积(mL) | 30.0 | 30.0 | 30.0 | 30.0 |
| 样品质量(g) | 2.96 | 3.70 | 5.18 | 6.66 |
 体积(mL) 体积(mL) | 672 | 840 | 896 | 672 |
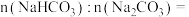
②稀盐酸的物质的量浓度

您最近一年使用:0次
解题方法
5 . Ⅰ.回答下列问题
(1)6.02×1023个CO2与______ mol H2的质量相等。
(2)含0.4 mol Cl-的氯化镁是______ mol,质量是______ g。
(3)4 mol Na2CO3与______ mol Na2SO4所含氧原子数相等。
(4)8 g甲烷(CH4)是______ mol,含______ 个甲烷分子。
(5)相同质量的SO2和SO3的物质的量之比为______ 。
(6)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为______ 。
Ⅱ.向100mLNaOH溶液中通入一定量CO2,充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加2mol·L-1的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
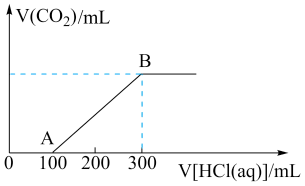
(7)①OA段发生反应的离子方程式为______ 。
②混合溶液中Na2CO3和NaHCO3的物质的量之比为______ 。
(1)6.02×1023个CO2与
(2)含0.4 mol Cl-的氯化镁是
(3)4 mol Na2CO3与
(4)8 g甲烷(CH4)是
(5)相同质量的SO2和SO3的物质的量之比为
(6)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为
Ⅱ.向100mLNaOH溶液中通入一定量CO2,充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加2mol·L-1的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。

(7)①OA段发生反应的离子方程式为
②混合溶液中Na2CO3和NaHCO3的物质的量之比为
您最近一年使用:0次
解题方法
6 . 将一定量的CO2通入20mL未知浓度的NaOH溶液中,在所得的溶液中逐滴加入0.lmol/L稀盐酸至过量,并将溶液加热,产生的气体的体积与加入稀盐酸的体积关系如图所示(忽略气体的溶解和盐酸的挥发)。
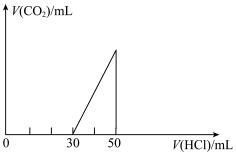
(1)原NaOH溶液的物质的量浓度___________ mol/L。
(2)当30mL<V<50ml时,溶液中发生反应的离子方程式___________ 。
(3)标准状况下,通入CO2的体积为___________ 。

(1)原NaOH溶液的物质的量浓度
(2)当30mL<V<50ml时,溶液中发生反应的离子方程式
(3)标准状况下,通入CO2的体积为
您最近一年使用:0次
7 . 某干燥白色固体可能含有 、
、 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
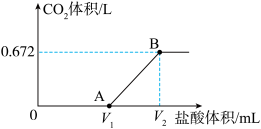
(1)产生的 的物质的量为
的物质的量为______________  ,
, 段反应的离子方程式为
段反应的离子方程式为____________________ 。
(2)若白色固体由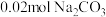 和
和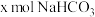 组成,则
组成,则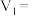
___________ ,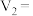
___________ 。
(3)若白色固体由 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为_______________________________ ,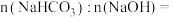
_________________ 。
(4)若白色固体只由 和
和 组成,且
组成,且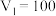 ,
, ,则
,则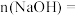
__________  ,原
,原 溶液中的
溶液中的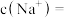
_______________  。
。
(5)另取某 和
和 组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸
组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸 ,充分反应,产生
,充分反应,产生 的体积如下表(标准状况下,且不考虑
的体积如下表(标准状况下,且不考虑 在水中的溶解):
在水中的溶解):
样品中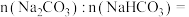
__________________ ,盐酸的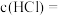
_______________  。
。
 、
、 、
、 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
(1)产生的
 的物质的量为
的物质的量为 ,
, 段反应的离子方程式为
段反应的离子方程式为(2)若白色固体由
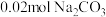 和
和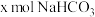 组成,则
组成,则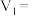
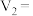
(3)若白色固体由
 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为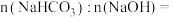
(4)若白色固体只由
 和
和 组成,且
组成,且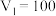 ,
, ,则
,则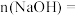
 ,原
,原 溶液中的
溶液中的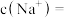
 。
。(5)另取某
 和
和 组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸
组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸 ,充分反应,产生
,充分反应,产生 的体积如下表(标准状况下,且不考虑
的体积如下表(标准状况下,且不考虑 在水中的溶解):
在水中的溶解):实验序号 | ① | ② | ③ |
| 100.0 | 100.0 | 100.0 |
| 3.80 | 7.60 | 11.40 |
| 896 | 1344 | 896 |
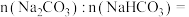
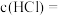
 。
。
您最近一年使用:0次
名校
8 . 将Na2CO3和NaHCO3的混合物3.27 g加热到质量不再减轻时,测得残留固体2.65 g。另取相同质量的此混合物固体,跟 100 mL某浓度的盐酸刚好完全反应生成NaCl,求;
(1)此混合物中NaHCO3与Na2CO3的物质的量之比为______________ ;
(2)所用盐酸的物质的量浓度为______________ ;
(3)生成CO2在标准状况下的体积为______________ 。
(1)此混合物中NaHCO3与Na2CO3的物质的量之比为
(2)所用盐酸的物质的量浓度为
(3)生成CO2在标准状况下的体积为
您最近一年使用:0次
2024-01-10更新
|
106次组卷
|
2卷引用:江苏省常州市溧阳中学2023-2024学年高一上学期阶段性调研测试化学试题
解题方法
9 . 实验室用100mL未知浓度的NaOH溶液捕获 ,充分反应后,再向所得溶液中逐滴加入
,充分反应后,再向所得溶液中逐滴加入 的盐酸,生成
的盐酸,生成 体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的
体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的 气体全部逸出)。
气体全部逸出)。
(1)当 时,溶液中发生的离子方程式:
时,溶液中发生的离子方程式:___________ 。
(2)捕获 的体积为
的体积为_____ L(标准状况)。
(3)原NaOH溶液的物质的量浓度为______  。
。
 ,充分反应后,再向所得溶液中逐滴加入
,充分反应后,再向所得溶液中逐滴加入 的盐酸,生成
的盐酸,生成 体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的
体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的 气体全部逸出)。
气体全部逸出)。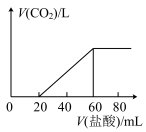
(1)当
 时,溶液中发生的离子方程式:
时,溶液中发生的离子方程式:(2)捕获
 的体积为
的体积为(3)原NaOH溶液的物质的量浓度为
 。
。
您最近一年使用:0次
解题方法
10 . 取5.48g Na2CO3和NaHCO3的固体混合物,分成两等份。
(1)将其中一份固体混合物加水溶解配成100mL溶液。当向溶液中加入300mLBa(OH)2溶液时,恰好使生成白色沉淀的量最多,测得反应后溶液的c(OH-)=0.100 mol∙L-1 (混合溶液体积改变忽略不计)。则原混合物中n(Na2CO3):n(NaHCO3)=___________ 。
(2)将另一份固体混合物充分加热。写出加热时发生反应的化学方程式___________ 。充分加热后的固体溶于水配成100mL溶液,则c(Na+)=___________ mol∙L-1。
(1)将其中一份固体混合物加水溶解配成100mL溶液。当向溶液中加入300mLBa(OH)2溶液时,恰好使生成白色沉淀的量最多,测得反应后溶液的c(OH-)=0.100 mol∙L-1 (混合溶液体积改变忽略不计)。则原混合物中n(Na2CO3):n(NaHCO3)=
(2)将另一份固体混合物充分加热。写出加热时发生反应的化学方程式
您最近一年使用:0次