浙江省“衢温5+1”联盟2023-2024学年高一上学期期中联考化学试题
浙江
高一
期中
2024-01-09
168次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学与STSE
浙江省“衢温5+1”联盟2023-2024学年高一上学期期中联考化学试题
浙江
高一
期中
2024-01-09
168次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学与STSE
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
您最近一年使用:0次
2024-01-06更新
|
100次组卷
|
3卷引用:浙江省“衢温5+1”联盟2023-2024学年高一上学期期中联考化学试题
单选题
|
较易(0.85)
解题方法
3. 下列各项中表达正确的是
| A.漂白液的有效成分是NaClO |
B.硫酸氢钠在水溶液中的电离: |
| C.NaCl是电解质,故NaCl固体能导电 |
D.小苏打的化学式为 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
4. 下列关于胶体的叙述正确的是
| A.胶体是纯净物 |
B.把 饱和溶液滴入到NaOH溶液中,可以制取 饱和溶液滴入到NaOH溶液中,可以制取 胶体 胶体 |
| C.树林中的晨曦,该现象与丁达尔效应有关 |
| D.胶体区别于其他分散系的本质特征是胶体具有丁达尔效应 |
您最近一年使用:0次
2024-01-06更新
|
90次组卷
|
2卷引用:浙江省“衢温5+1”联盟2023-2024学年高一上学期期中联考化学试题
单选题
|
较易(0.85)
6. 下列说法正确的是
| A.若某碱性溶液的焰色呈黄色,则该溶液的溶质一定为NaOH |
| B.钠在氯气中燃烧产生白烟 |
| C.氯气能使鲜花褪色,所以氯气具有漂白性 |
| D.铁与水不发生反应,因此钢水注入模具前,模具不需要干燥处理 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
7. 下列说法不正确 的是
| A.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用 |
| B.碳酸氢钠是发酵粉的主要成分 |
| C.漂白粉可用作游泳池场所的消毒剂 |
| D.食品包装盒中的生石灰或铁粉,均可以起到抗氧化作用 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
8. 下列实验操作不正确 的是
A.NaCl和 的混合物经溶解、过滤、洗涤、干燥,可分离出 的混合物经溶解、过滤、洗涤、干燥,可分离出 |
| B.将新制氯水滴入紫色石蕊溶液中,可以看到石蕊溶液先变红后褪色 |
| C.用同一针筒先后抽取80mL氯气、20mL水,振荡,气体完全溶解,溶液变为黄绿色 |
| D.定容时,因不慎使液面高于容量瓶的刻度线,只能重新配制 |
您最近一年使用:0次
单选题
|
容易(0.94)
9. 设 为阿伏加德罗常数的值,则下列说法正确的是
为阿伏加德罗常数的值,则下列说法正确的是
 为阿伏加德罗常数的值,则下列说法正确的是
为阿伏加德罗常数的值,则下列说法正确的是A. 的 的 溶液中含 溶液中含 数目为 数目为 |
B.常温常压下,22g二氧化碳中含有的原子数目为 |
C.标况下,2.24L水中含有的电子数目为 |
D.在氧化还原反应中,反应掉 时转移电子数目一定为 时转移电子数目一定为 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
10. 下列反应的离子方程式不正确 的是
A.氯气溶于水时发生的反应: |
B.向NaOH稀溶液中通入过量 : : |
C.将 溶于稀HCl溶液中: 溶于稀HCl溶液中: |
D.将 溶于水: 溶于水: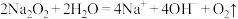 |
【知识点】 离子方程式的正误判断解读 氯气与水的反应解读
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
11. 关于氧化还原反应: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应中 全部作还原剂 全部作还原剂 | B.NaOH是还原产物 |
C.X为 | D.当转移2mol电子时,可生成1molX |
【知识点】 氧化还原反应的几组概念解读 电子转移计算
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
12. 关于阿伏加德罗定律及其推论,下列说法正确的是
| A.同温同压下,相同体积的任何物质都具有相同数目的分子 |
B.不同温度下,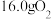 和 和 含有的原子数相等 含有的原子数相等 |
| C.同温同压下,相同质量的二氧化碳与氢气的体积之比为22:1 |
| D.常温下,相同体积、相同质量的氧气与氢气的压强之比为16:1 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
14. 下列实验方案或实验结论不正确 的是
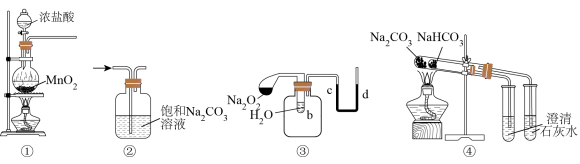

A.装置①可以用于实验室制 |
B.装置②可以用于除去 中混有的少量HCl 中混有的少量HCl |
C.装置③验证 与水反应的热量变化 与水反应的热量变化 |
D.装置④可用于比较 和 和 的热稳定性 的热稳定性 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
15. 印刷电路板(PCB)是用腐蚀液将覆铜板上的部分铜腐蚀掉而制得。电子工业中常用 溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:

下列说法不正确 的是
 溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
下列说法
A.腐蚀后的废液中,主要的金属阳离子有 、 、 、 、 |
B.过程②中发生的主要反应为: 和 和 |
C.若过程④中加入过量的试剂B为酸化的 ,则反应过程中酸性增强 ,则反应过程中酸性增强 |
D.若在10g滤渣中加入足量盐酸,放出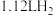 (标准状况),则滤渣中Cu的质量分数是72% (标准状况),则滤渣中Cu的质量分数是72% |
【知识点】 离子方程式的书写解读 有关铁及其化合物转化的流程题型解读
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
16. 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将一小块金属钠投入 溶液,钠会浮在溶液上四处游动,同时会有紫红色固体析出 溶液,钠会浮在溶液上四处游动,同时会有紫红色固体析出 | 钠可以置换出铜 |
| B | 向某溶液中加入稀盐酸产生无色无味气体,将该气体通入澄清石灰水,变浑浊 | 溶液一定含有 |
| C | 室温下,向等浓度、等体积的 和 和 溶液中,分别滴加几滴酚酞, 溶液中,分别滴加几滴酚酞, 溶液红色更深 溶液红色更深 | 说明 溶液碱性比 溶液碱性比 强 强 |
| D | 探究脱氧剂中还原铁粉是否变质,可取少量样品溶于盐酸,再滴加KSCN溶液,溶液未变红 | 说明脱氧剂未变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
较易(0.85)
名校
17. 按要求回答下列问题:
(1)铁红的化学式是___________ 。
(2)固体 的性质:
的性质:___________ (填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
(3)写出工业制漂白粉的化学方程式___________ 。
(4)除去 溶液中少量的
溶液中少量的 选择的试剂
选择的试剂___________ 。
(1)铁红的化学式是
(2)固体
 的性质:
的性质:①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
(3)写出工业制漂白粉的化学方程式
(4)除去
 溶液中少量的
溶液中少量的 选择的试剂
选择的试剂
您最近一年使用:0次
2024-01-06更新
|
68次组卷
|
2卷引用:浙江省“衢温5+1”联盟2023-2024学年高一上学期期中联考化学试题
三、解答题 添加题型下试题
解答题-实验探究题
|
较易(0.85)
解题方法
18. 实验室欲用固体烧碱配制 溶液480mL,请回答以下问题:
溶液480mL,请回答以下问题:
(1)配制过程中,需要用到的主要仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、_____ 。
(2)该实验所需NaOH固体的质量为_____ g。
(3)完成该实验需要如下操作:
①计算所需氢氧化钠固体的质量;②称量氢氧化钠固体;③将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁及玻璃棒2~3次,洗涤液也注入容量瓶中,轻轻的振荡;④用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却至室温;⑤盖好瓶塞,摇匀;⑥继续向容量瓶中加蒸馏水至刻度线1~2cm时,改用胶头滴管滴加蒸馏水至凹液面最低点与刻度线相切。
上述操作步骤的正确顺序为___________ (填序号)。
(4)配制的NaOH溶液过程中,下列说法正确的是___________(填字母)。

 溶液480mL,请回答以下问题:
溶液480mL,请回答以下问题:(1)配制过程中,需要用到的主要仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、
(2)该实验所需NaOH固体的质量为
(3)完成该实验需要如下操作:
①计算所需氢氧化钠固体的质量;②称量氢氧化钠固体;③将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁及玻璃棒2~3次,洗涤液也注入容量瓶中,轻轻的振荡;④用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却至室温;⑤盖好瓶塞,摇匀;⑥继续向容量瓶中加蒸馏水至刻度线1~2cm时,改用胶头滴管滴加蒸馏水至凹液面最低点与刻度线相切。
上述操作步骤的正确顺序为
(4)配制的NaOH溶液过程中,下列说法正确的是___________(填字母)。

| A.容量瓶在检漏和洗净后未干燥,不影响配制溶液的浓度 |
| B.转移和洗涤操作后,应将容量瓶按图方式摇晃初步摇匀,再进行定容 |
| C.定容时仰视容量瓶刻度线,会导致所得溶液浓度偏大 |
D.配制完成的溶液应转移至试剂瓶中贮存,洗净的试剂瓶应先用 溶液润洗2~3次 溶液润洗2~3次 |
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
19.  是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成
是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成 晶体以便储运。亚氯酸钠(
晶体以便储运。亚氯酸钠( )是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成
)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:

已知:① 浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
② 受热易分解
受热易分解
(1)向“反应器”中鼓入空气的作用是___________ 。
(2)“吸收塔”的作用是将产生的 转化为
转化为 ,在此过程中加入的
,在此过程中加入的 是作用
是作用_______ (填“氧化剂”或“还原剂”),当有 参与该反应时,反应转移的电子数为
参与该反应时,反应转移的电子数为_________ 。
(3)“吸收塔”中需要控制温度不超过20℃,其原因是___________ 。
(4) 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl,写出该化学方程式
和NaCl,写出该化学方程式________ 。
(5)写出“反应器”步骤中生成 的离子方程式
的离子方程式___________ 。
(6)为测定所得 (摩尔质量
(摩尔质量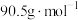 )产品的质量分数,进行如下实验:
)产品的质量分数,进行如下实验:
步骤I:准确称取所得亚氯酸钠样品1.000g于烧杯中,用适量蒸馏水和略过量的KI晶体,再滴加适量的稀硫酸,充分反应。(反应方程式为: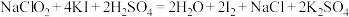 )
)
步骤Ⅱ:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL。(反应方程式为:
溶液22.00mL。(反应方程式为: )
)
计算该产品中 的质量分数
的质量分数_______ (保留小数点后两位)。
 是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成
是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成 晶体以便储运。亚氯酸钠(
晶体以便储运。亚氯酸钠( )是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成
)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:
已知:①
 浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。②
 受热易分解
受热易分解(1)向“反应器”中鼓入空气的作用是
(2)“吸收塔”的作用是将产生的
 转化为
转化为 ,在此过程中加入的
,在此过程中加入的 是作用
是作用 参与该反应时,反应转移的电子数为
参与该反应时,反应转移的电子数为(3)“吸收塔”中需要控制温度不超过20℃,其原因是
(4)
 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl,写出该化学方程式
和NaCl,写出该化学方程式(5)写出“反应器”步骤中生成
 的离子方程式
的离子方程式(6)为测定所得
 (摩尔质量
(摩尔质量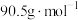 )产品的质量分数,进行如下实验:
)产品的质量分数,进行如下实验:步骤I:准确称取所得亚氯酸钠样品1.000g于烧杯中,用适量蒸馏水和略过量的KI晶体,再滴加适量的稀硫酸,充分反应。(反应方程式为:
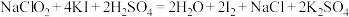 )
)步骤Ⅱ:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用
 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL。(反应方程式为:
溶液22.00mL。(反应方程式为: )
)计算该产品中
 的质量分数
的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
20. 铁是日常生活中最为常见的金属,也是用量最大的金属。某化学兴趣小组想通过如下实验来探究铁及其化合物的某些性质。
探究Ⅰ:利用如图来探究铁与水蒸气反应的产物,试回答下列问题(部分装置和仪器已略去)。

(1)装置B中发生反应的化学方程式为___________ 。
(2)装置A、B加热的先后顺序是________ ;石棉绒的作用是________ 。
(3)反应结束后冷却至室温,取一定量B中残留的固体于试管中,加入足量稀盐酸充分溶解后,再加入几滴KSCN溶液,如果溶液没有变红色,能否说明铁与水蒸气反应生成的固体中一定不含+3价的铁,请说明理由______ 。
(4)关于该实验,下列说法不正确 的是________。
探究Ⅱ:利用如图来探究 的制备,希望较长时间内可以观察到B中有白色沉淀出现。
的制备,希望较长时间内可以观察到B中有白色沉淀出现。
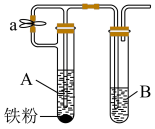
(5)装置A、B中盛放的溶液分别是______ 、________ 。
(6)将B中的白色沉淀置于潮湿的空气中很快就变为红褐色,请用一个化学方程式表示发生该变化的原因______ 。
探究Ⅰ:利用如图来探究铁与水蒸气反应的产物,试回答下列问题(部分装置和仪器已略去)。

(1)装置B中发生反应的化学方程式为
(2)装置A、B加热的先后顺序是
(3)反应结束后冷却至室温,取一定量B中残留的固体于试管中,加入足量稀盐酸充分溶解后,再加入几滴KSCN溶液,如果溶液没有变红色,能否说明铁与水蒸气反应生成的固体中一定不含+3价的铁,请说明理由
(4)关于该实验,下列说法
| A.装置C中盛放的固体可能是碱石灰,起干燥作用 |
B.如果反应后B中残留的固体为黑色纯净物,则该固体可能为 、FeO或 、FeO或 中的一种 中的一种 |
| C.装置D采用向下排空法收集反应产生的气体 |
D.取少许酸性高锰酸钾溶液于试管中,加入(3)中盐酸溶解后的溶液(足量),如果高锰酸钾溶液会褪色,则说明(3)中的溶液一定含有 |
探究Ⅱ:利用如图来探究
 的制备,希望较长时间内可以观察到B中有白色沉淀出现。
的制备,希望较长时间内可以观察到B中有白色沉淀出现。
(5)装置A、B中盛放的溶液分别是
(6)将B中的白色沉淀置于潮湿的空气中很快就变为红褐色,请用一个化学方程式表示发生该变化的原因
您最近一年使用:0次
四、计算题 添加题型下试题
计算题
|
较易(0.85)
解题方法
21. 实验室用100mL未知浓度的NaOH溶液捕获 ,充分反应后,再向所得溶液中逐滴加入
,充分反应后,再向所得溶液中逐滴加入 的盐酸,生成
的盐酸,生成 体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的
体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的 气体全部逸出)。
气体全部逸出)。
(1)当 时,溶液中发生的离子方程式:
时,溶液中发生的离子方程式:___________ 。
(2)捕获 的体积为
的体积为_____ L(标准状况)。
(3)原NaOH溶液的物质的量浓度为______  。
。
 ,充分反应后,再向所得溶液中逐滴加入
,充分反应后,再向所得溶液中逐滴加入 的盐酸,生成
的盐酸,生成 体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的
体积(标准状况)与所加盐酸体积间的关系如下图所示(假设生成的 气体全部逸出)。
气体全部逸出)。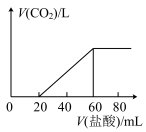
(1)当
 时,溶液中发生的离子方程式:
时,溶液中发生的离子方程式:(2)捕获
 的体积为
的体积为(3)原NaOH溶液的物质的量浓度为
 。
。
【知识点】 碳酸钠、碳酸氢钠混合物的有关求算解读
您最近一年使用:0次
试卷分析
整体难度:较易
考查范围:认识化学科学、化学实验基础、常见无机物及其应用、化学与STSE
试卷题型(共 21题)
题型
数量
单选题
16
填空题
1
解答题
3
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 酸、碱、盐、氧化物 | |
| 2 | 0.94 | 配制一定物质的量浓度的溶液实验的仪器 | |
| 3 | 0.85 | 电解质、非电解质概念 漂白粉和漂粉精的用途 碳酸氢钠的俗称、物理性质及用途 | |
| 4 | 0.94 | 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 5 | 0.94 | 氧化还原反应的几组概念 | |
| 6 | 0.85 | 氯气与金属单质的反应 焰色试验 铁与水蒸气的反应 | |
| 7 | 0.94 | 漂白粉和漂粉精的用途 碳酸氢钠的俗称、物理性质及用途 化学科学对人类文明发展的意义 | |
| 8 | 0.94 | 氯水的性质 配制一定物质的量浓度的溶液的步骤、操作 过滤 | |
| 9 | 0.94 | 阿伏加德罗常数的求算 22.4L/mol适用条件 根据n=m/M的相关计算 氧化还原反应与NA相关推算 | |
| 10 | 0.94 | 离子方程式的正误判断 氯气与水的反应 | |
| 11 | 0.85 | 氧化还原反应的几组概念 电子转移计算 | |
| 12 | 0.94 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 13 | 0.94 | 物质的量浓度与溶质成分有关的计算 | |
| 14 | 0.65 | 氯气的实验室制法 碳酸钠与碳酸氢钠性质的比较 常见气体的制备与收集 综合实验设计与评价 | |
| 15 | 0.94 | 离子方程式的书写 有关铁及其化合物转化的流程题型 | |
| 16 | 0.85 | 钠与盐溶液的反应 Fe3+的检验 物质性质实验方案的设计 | |
| 二、填空题 | |||
| 17 | 0.85 | 非电解质、电解质物质类别判断 漂白粉和漂粉精的制备原理 几种铁的氧化物的物理性质及用途 Fe2+的氧化性 | |
| 三、解答题 | |||
| 18 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 19 | 0.65 | 氧化还原反应有关计算 氧化还原反应方程式的书写与配平 常见无机物的制备 探究物质组成或测量物质的含量 | 工业流程题 |
| 20 | 0.65 | 铁与水蒸气的反应 氢氧化亚铁的制备 Fe3+的检验 物质性质实验方案的设计 | 实验探究题 |
| 四、计算题 | |||
| 21 | 0.85 | 碳酸钠、碳酸氢钠混合物的有关求算 | |





 相等的是
相等的是 溶液与
溶液与 溶液
溶液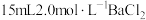 溶液与
溶液与 溶液
溶液 溶液与
溶液与 溶液
溶液 溶液与
溶液与 溶液
溶液

