1 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为碳酸钠,假设杂质分布均匀)。为测其组成,称取3.784克样品溶于水,配成1000mL溶液。取出50mL该溶液,加入0.05mol/LBa(OH)2溶液至44.00mL时沉淀量最大。请计算
(1)0.05mol/LBa(OH)2溶液的c(OH-)=____ 。
(2)样品中n(NaHCO3):n(Na2CO3)=____ 。
(1)0.05mol/LBa(OH)2溶液的c(OH-)=
(2)样品中n(NaHCO3):n(Na2CO3)=
您最近一年使用:0次
2 . 计算
(1)在标准状况下,10.2gH2S 与标况下_______ LNH3含有相同的H原子。
(2)实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取4.420g样品溶于水,配成500mL溶液。取出50.00mL该溶液,加入0. 1000 mol/L Ba(OH)2溶液至50.00mL时沉淀量达到最大。请计算:
①25°C时,0.1000 mol/L Ba(OH)2溶液中的氢氧根离子浓度是_______ mol/L。
②样品中n(NaHCO3):n(Na2CO3)=_______ 。
(1)在标准状况下,10.2gH2S 与标况下
(2)实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取4.420g样品溶于水,配成500mL溶液。取出50.00mL该溶液,加入0. 1000 mol/L Ba(OH)2溶液至50.00mL时沉淀量达到最大。请计算:
①25°C时,0.1000 mol/L Ba(OH)2溶液中的氢氧根离子浓度是
②样品中n(NaHCO3):n(Na2CO3)=
您最近一年使用:0次
解题方法
3 . 实验室中有一瓶碳酸钠固体,已有部分变质(假设杂质只有 ,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加
,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加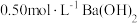 溶液至30.00mL时恰好完全沉淀。
溶液至30.00mL时恰好完全沉淀。
请计算:
(1)加入的 溶液中溶质的物质的量为
溶液中溶质的物质的量为_______ 。
(2)样品中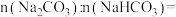
_______ 。
 ,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加
,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加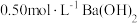 溶液至30.00mL时恰好完全沉淀。
溶液至30.00mL时恰好完全沉淀。请计算:
(1)加入的
 溶液中溶质的物质的量为
溶液中溶质的物质的量为(2)样品中
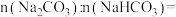
您最近一年使用:0次
20-21高一下·浙江·阶段练习
名校
4 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取1.892g样品溶于水,配成500mL溶液。取出25.00mL该溶液,加入0.050mol·L-1Ba(OH)2溶液至22.00mL时沉淀量达到最大。请计算:
(1)25℃时,0.050mol·L-1Ba(OH)2溶液中的氢氧根离子浓度是_______ mol/L
(2)样品中n(NaHCO3)∶n(Na2CO3)=_______ 。
(1)25℃时,0.050mol·L-1Ba(OH)2溶液中的氢氧根离子浓度是
(2)样品中n(NaHCO3)∶n(Na2CO3)=
您最近一年使用:0次
名校
解题方法
5 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,用分析天平称称取1.7240g样品溶于水,配成500mL溶液。取出25.00mL该溶液,加入一定物质的量浓度的Ba(OH)2溶液至20.00mL时沉淀量达到最大值,过滤、洗涤、干燥,称量沉淀质量为0.1970 g。请计算:
(1)所加Ba(OH)2溶液的物质的量浓度为______ mol·L-1
(2)样品中n(NaHCO3) ∶n(Na2CO3)=___
(1)所加Ba(OH)2溶液的物质的量浓度为
(2)样品中n(NaHCO3) ∶n(Na2CO3)=
您最近一年使用:0次
2020-11-26更新
|
219次组卷
|
6卷引用:浙江省杭州地区(含周边)重点中学2020-2021学年高一上学期期中考试化学试题
浙江省杭州地区(含周边)重点中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】86.(已下线)【浙江新东方】108(已下线)【浙江新东方】在线化学21(已下线)【萧山新东方】萧山试卷解析浙江省瑞安中学2023-2024学年高一上学期12月月考化学试卷
20-21高一·浙江·阶段练习
解题方法
6 . 实验室中有一瓶碳酸氢钾固体,因受热而部分变质(杂质为K2CO3,假设杂质分布均匀)。为测定其组成,称取12.76 g样品溶于水,配成500 mL溶液。取出25.00 mL该溶液,加入0.1000 mol/LBa(OH)2 溶液至60.00mL时沉淀量达到最大。回答下列问题:
(1)写出碳酸氢钾固体受热分解的化学方程式:_______ 。
(2)写出样品溶液与Ba(OH)2溶液反应的离子方程式:_______ 。
(3)12.76g样品中碳酸氢钾物质的量为_______ ,碳酸钾物质的量为_______ 。
(1)写出碳酸氢钾固体受热分解的化学方程式:
(2)写出样品溶液与Ba(OH)2溶液反应的离子方程式:
(3)12.76g样品中碳酸氢钾物质的量为
您最近一年使用:0次
解题方法
7 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为 Na2CO3,假设杂质分布均匀)。为测定其组成,称取1. 892 g 样品溶于水,配成 500 mL 溶液。取出 25. 00 mL 该溶液,加入 0. 050 mol • L-1 Ba(OH)2 溶液至 22. 00 mL 时沉淀量达到最大。
请计算:
(1)25°C时,0. 050mol •L-1Ba (OH)2溶液的pH=__________ 。
(2)样品中 n(NaHCO3):n ( Na2CO3)=__________ 。
请计算:
(1)25°C时,0. 050mol •L-1Ba (OH)2溶液的pH=
(2)样品中 n(NaHCO3):n ( Na2CO3)=
您最近一年使用:0次
10-11高三上·上海浦东新·期末
8 . 已知NaHCO3在潮湿的空气中会缓慢分解。取没有妥善保管已部分变质的NaHCO3样品a g,溶于水配成溶液,慢慢滴入0.200mol/L稀盐酸并不停地搅拌,反应过程中测得溶液中NaHCO3的质量与加入盐酸的体积之间的关系如图所示。
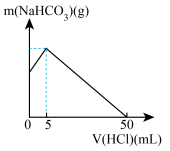
(1)a g样品中含Na2CO3的质量为____________ g。
(2)a g样品未变质前NaHCO3的质量为________ g。
(3)若另取样品b g,充分加热以后得到固体质量为5.300g,则b=_____________ g。

(1)a g样品中含Na2CO3的质量为
(2)a g样品未变质前NaHCO3的质量为
(3)若另取样品b g,充分加热以后得到固体质量为5.300g,则b=
您最近一年使用:0次
名校
9 . NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管已部分变质的一定质量的NaHCO3样品溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不计溶于水的CO2气体)

试求:
(1)该盐酸溶液的物质的量浓度为_______ mol·L-1。
(2)未变质前NaHCO3的物质的量为________ mol。

试求:
(1)该盐酸溶液的物质的量浓度为
(2)未变质前NaHCO3的物质的量为
您最近一年使用:0次
解题方法
10 . 某天然碱可以看作是CO2 和 NaOH 反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
ⅰ称取 3.98 g 天然碱样品,加入 50mL 稀盐酸(足量),产生 CO2 896mL(标准状况)。
ⅱ称取 3.98g 天然碱样品,加热至分解完全,产生 CO2 224mL(标准状况)和 0.36g 水。
①该稀盐酸的物质的量浓度最小是_____________ 。
②天然碱的化学式是_____________ 。
ⅰ称取 3.98 g 天然碱样品,加入 50mL 稀盐酸(足量),产生 CO2 896mL(标准状况)。
ⅱ称取 3.98g 天然碱样品,加热至分解完全,产生 CO2 224mL(标准状况)和 0.36g 水。
①该稀盐酸的物质的量浓度最小是
②天然碱的化学式是
您最近一年使用:0次



