名校
1 . A、B、C、D、E五种物质的焰色试验都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有可燃性,B与水反应放出的气体具有助燃性,同时都生成C的溶液,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D。
(1)写出A+H2O→C的化学方程式:___________ 。
(2)写出B+H2O→C的化学方程式:___________ 。
(3)写出E→D的化学方程式:___________ 。
(4)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式___________ ,___________ 。
(5)某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为___________ (假设漂白粉中的其它成份不与硝酸反应)。
(6)将14gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12L,所得溶液的体积为400mL。试计算:原混合物中Na2O的质量为___________ g,所得溶液的物质的量浓度为___________ mol·L-1。
(1)写出A+H2O→C的化学方程式:
(2)写出B+H2O→C的化学方程式:
(3)写出E→D的化学方程式:
(4)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式
(5)某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为
(6)将14gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12L,所得溶液的体积为400mL。试计算:原混合物中Na2O的质量为
您最近半年使用:0次
2 . 过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠经常因为保存不当容易吸收空气中CO2而变质。
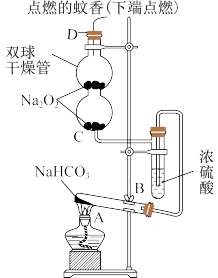
Ⅰ.某课外小组欲用以下装置探究过氧化钠与CO2反应后的产物。试回答下列问题:
(1)写出A中反应的化学方程式_____ 。
(2)B装置的作用是_____ 。
(3)观察到的实验现象:双球干燥管内淡黄色粉末逐渐转变为白色,点燃的蚊香燃烧更加剧烈。请根据实验现象写出C装置的化学方程式:_____ 。
Ⅱ.
(4)该课外小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入_____ 溶液,充分振荡后有白色沉淀,证明 已经变质。
已经变质。
Ⅲ.
(5)超氧化钾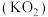 与过氧化钠一样能吸收
与过氧化钠一样能吸收 生成碳酸盐及
生成碳酸盐及 ,写出该反应的化学方程式
,写出该反应的化学方程式_____ 。

Ⅰ.某课外小组欲用以下装置探究过氧化钠与CO2反应后的产物。试回答下列问题:
(1)写出A中反应的化学方程式
(2)B装置的作用是
(3)观察到的实验现象:双球干燥管内淡黄色粉末逐渐转变为白色,点燃的蚊香燃烧更加剧烈。请根据实验现象写出C装置的化学方程式:
Ⅱ.
(4)该课外小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
 已经变质。
已经变质。Ⅲ.
(5)超氧化钾
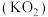 与过氧化钠一样能吸收
与过氧化钠一样能吸收 生成碳酸盐及
生成碳酸盐及 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近半年使用:0次
名校
解题方法
3 . 下列实验过程能达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 配制0.4000mol·L−1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250mL容量瓶中定容 |
| B | 鉴别NaHCO3溶液与Na2CO3溶液 | 用小试管分别取少量待测溶液,然后滴加澄清石灰水 |
| C | 检验Na2SO3样品未变质 | 用取样于试管加入水溶解,滴加几滴硝酸,再加少量BaCl2溶液,观察现象 |
| D | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 下列操作、现象和结论都正确的是
| 选项 | 操作及现象 | 结论 |
| A | 在FeCl₂溶液中滴加KSCN溶液,溶液变红色 | FeCl₂已变质 |
| B | 在碳酸氢钠溶液中滴加澄清石灰水,产生白色沉淀 | NaHCO₃样品中含有Na₂CO₃ |
| C | 在高锰酸钾粉末中加入浓盐酸,产生黄绿色气体 | 氧化性:KMnO₄<Cl2 |
| D | 在AlCl₃溶液中滴加过量的氨水,产生白色沉淀 | Al(OH)₃不与NH₃·H₂O反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取4.86 g样品溶于水,配成500 mL溶液。加入0.50 mol/L Ba(OH)2溶液至100.00 mL时沉淀量达到最大。请计算:
(1)25℃时0.50 mol/L Ba(OH)2溶液中的氢氧根离子浓度是_______ mol/L。
(2)样品中n(NaHCO3)∶n(Na2CO3)=_______ 。
(1)25℃时0.50 mol/L Ba(OH)2溶液中的氢氧根离子浓度是
(2)样品中n(NaHCO3)∶n(Na2CO3)=
您最近半年使用:0次
解题方法
6 . 某变质小苏打样品中含Na2CO3,取m克样品用如图装置测定Na2CO3含量,下列说法不正确的是
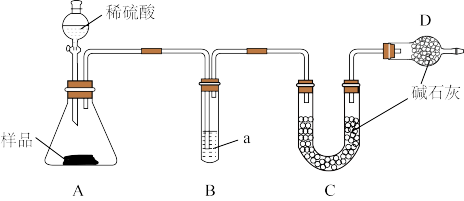

| A.装置B所装试剂a是浓硫酸,其作用是干燥CO2 |
| B.装置D的作用是防止空气中的H2O、CO₂进入装置C |
| C.反应后称量装置C的质量为n克,用数据m、n可求得Na2CO3含量 |
| D.上述装置的不足之处是没有在A装置前接一个赶气装置 |
您最近半年使用:0次
名校
解题方法
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验溶液中是否含Cl- | 先向某溶液中加入稀盐酸酸化,再加入AgNO3溶液 | 若有白色沉淀,说明含有Cl- |
| B | 鉴别NaHCO3与Na2CO3 | 取少许两种物质,加入几滴水,插入温度计,测温 | 温度降低的是Na2CO3 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2-3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| D | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-11-02更新
|
227次组卷
|
3卷引用:浙江省余姚中学2022-2023学年高一上学期10月月考化学试题
解题方法
8 .  常作漂白剂、杀菌剂、消毒剂。
常作漂白剂、杀菌剂、消毒剂。 保存不当易吸收空气中的
保存不当易吸收空气中的 而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
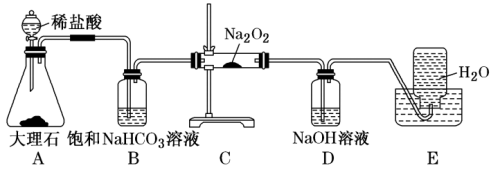
(1)盛稀盐酸的仪器名称为_______ ,A装置为 的发生装置,该反应的化学方程式为
的发生装置,该反应的化学方程式为_______________________________ 。
(2)B中 溶液可除去
溶液可除去 中的
中的 ,则B中反应的化学方程式为
,则B中反应的化学方程式为_______ 。
(3)C装置为 的发生装置,写出
的发生装置,写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(4)D中 溶液的作用是
溶液的作用是_______ 。
(5)E装置为排水法收集 的装置,检验所收集的气体为
的装置,检验所收集的气体为 的方法为
的方法为_______ 。
 常作漂白剂、杀菌剂、消毒剂。
常作漂白剂、杀菌剂、消毒剂。 保存不当易吸收空气中的
保存不当易吸收空气中的 而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
(1)盛稀盐酸的仪器名称为
 的发生装置,该反应的化学方程式为
的发生装置,该反应的化学方程式为(2)B中
 溶液可除去
溶液可除去 中的
中的 ,则B中反应的化学方程式为
,则B中反应的化学方程式为(3)C装置为
 的发生装置,写出
的发生装置,写出 与
与 反应的化学方程式
反应的化学方程式(4)D中
 溶液的作用是
溶液的作用是(5)E装置为排水法收集
 的装置,检验所收集的气体为
的装置,检验所收集的气体为 的方法为
的方法为
您最近半年使用:0次
解题方法
9 . 实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定该瓶样品中氢氧化钠的质量分数,现取17.3g该样品溶于足量的水中(固体完全溶解),向所得溶液中逐滴加入200g一定溶质质量分数的稀盐酸,实验过程如图所示(不考虑碳酸钠的分步反应)。
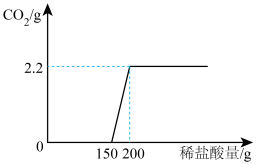
(1)经分析,该氢氧化钠固体_______ (填“部分”或“完全”)变质,恰好完全反应时,产生气体的质量为_______ g。
(2)计算样品中氢氧化钠的质量_______ (写出计算过程)。

(1)经分析,该氢氧化钠固体
(2)计算样品中氢氧化钠的质量
您最近半年使用:0次
10 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为碳酸钠,假设杂质分布均匀)。为测其组成,称取3.784克样品溶于水,配成1000mL溶液。取出50mL该溶液,加入0.05mol/LBa(OH)2溶液至44.00mL时沉淀量最大。请计算
(1)0.05mol/LBa(OH)2溶液的c(OH-)=____ 。
(2)样品中n(NaHCO3):n(Na2CO3)=____ 。
(1)0.05mol/LBa(OH)2溶液的c(OH-)=
(2)样品中n(NaHCO3):n(Na2CO3)=
您最近半年使用:0次



