1 . 含氯、含钠化合物在生活、生产中随处可见。回答下列问题:
(1)某同学查询资料,发现用氯气消毒的自来水不能直接用于浇灌植物、养鱼等。
①不能直接用于浇灌植物、养鱼的原因是氯的水溶液具有较强的___________ (填“氧化性”或“还原性”)
②可以采取___________ 方式快速除水中的氯,再用于浇灌植物。
A.阳光下暴晒 B.烧开后冷却 C.加入过量 固体
固体
(2) 不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为
不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为___________ 。
(3)碱性条件下, 氧化
氧化 可制备绿色消毒剂
可制备绿色消毒剂 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)为了使以面粉为原料制作的面包松软可口,通常用碳酸氢钠作发泡剂,发泡时发生的化学方程式为___________ 。
(1)某同学查询资料,发现用氯气消毒的自来水不能直接用于浇灌植物、养鱼等。
①不能直接用于浇灌植物、养鱼的原因是氯的水溶液具有较强的
②可以采取
A.阳光下暴晒 B.烧开后冷却 C.加入过量
 固体
固体(2)
 不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为
不方便运输,储存,通常将其制备为次氯酸盐。如工业上可用氯气与冷的石灰乳反应制备漂白粉,发生反应的化学方程式为(3)碱性条件下,
 氧化
氧化 可制备绿色消毒剂
可制备绿色消毒剂 ,该反应的离子方程式为
,该反应的离子方程式为(4)为了使以面粉为原料制作的面包松软可口,通常用碳酸氢钠作发泡剂,发泡时发生的化学方程式为
您最近半年使用:0次
解题方法
2 . 化学是人类进步的阶梯.了解物质的组成和性质,并合理使用会在一定程度上改善我们的生活.通过对下列几种生活中常见物质的分析,回答下列问题:
①纯碱;②铁红;③“84”消毒液;④小苏打;⑤食盐;⑥烧碱.
(1)上述物质中属于碱的是______ (填序号).
(2)上述物质能漂白有色鲜花的是______ (填序号),利用了该物质的______ (填“氧化性”“还原性”“酸性”或“碱性”).
(3)铁红与稀盐酸反应的离子方程式为______ .
(4)工业上可利用电解NaCl溶液的方法制备 ,同时生成NaOH和
,同时生成NaOH和 ,该反应的化学方程式为
,该反应的化学方程式为______ ;利用该方法每制备71g ,理论上转移电子的物质的量为
,理论上转移电子的物质的量为______ .
(5)请设计实验,鉴别固体①和④:______ .
①纯碱;②铁红;③“84”消毒液;④小苏打;⑤食盐;⑥烧碱.
(1)上述物质中属于碱的是
(2)上述物质能漂白有色鲜花的是
(3)铁红与稀盐酸反应的离子方程式为
(4)工业上可利用电解NaCl溶液的方法制备
 ,同时生成NaOH和
,同时生成NaOH和 ,该反应的化学方程式为
,该反应的化学方程式为 ,理论上转移电子的物质的量为
,理论上转移电子的物质的量为(5)请设计实验,鉴别固体①和④:
您最近半年使用:0次
2023-12-21更新
|
36次组卷
|
2卷引用:河南省(驻马店)青桐鸣联考2023-2024学年高一上学期12月月考化学试题
名校
3 . 钠的一系列化合物在生活与生产中有非常重要的作用,某学习小组开展了相关研究活动:
(1)甲同学欲配制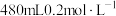 的
的 溶液,需要使用的玻璃仪器有
溶液,需要使用的玻璃仪器有____________ 、烧杯和胶头滴管;下列操作会使所配溶液浓度偏小的是______ 。
a.用托盘天平称量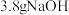 固体进行配制溶液
固体进行配制溶液
b.定容时俯视刻度线
c.未待溶解的 浓溶液冷却即转移至相应容器进行后继操作
浓溶液冷却即转移至相应容器进行后继操作
d.定容摇匀后发现液面低于刻度线,再次加入蒸馏水至刻度线
(2)乙同学欲比较 固体和
固体和 固体的热稳定性,设计实验装置如下图:
固体的热稳定性,设计实验装置如下图:
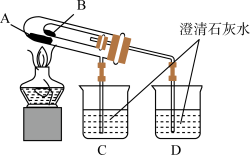
① 烧杯中的现象是
烧杯中的现象是____________
② 处应放置的药品是
处应放置的药品是____________
③热稳定性:
______  (大于、小于)
(大于、小于)
(3)丙同学为探究 的强氧化性,某设计了下图实验装置。
的强氧化性,某设计了下图实验装置。
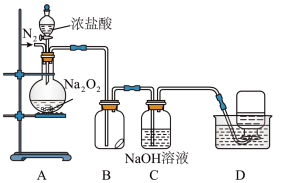
实验步骤及现象如下:
Ⅰ.检查装置气密性后,装入药品并连接仪器。
Ⅱ.缓慢通入一定量的 后,封闭
后,封闭 气体通路,将装置
气体通路,将装置 连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,
连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸, 中剧烈反应,有黄绿色气体产生。
中剧烈反应,有黄绿色气体产生。
Ⅱ.待产生连续气泡后,将装置 中的导管末端伸入集气瓶中,收集到无色气体。
中的导管末端伸入集气瓶中,收集到无色气体。
①. 中气体能使带火星的木条复燃,丙同学分析该气体不可能由
中气体能使带火星的木条复燃,丙同学分析该气体不可能由 还原
还原 所得,从氧化还原角度说明理由:
所得,从氧化还原角度说明理由:______ 。
②.资料显示, 也能与干燥
也能与干燥 反应产生
反应产生 ,写出反应的化学方程式
,写出反应的化学方程式______
(1)甲同学欲配制
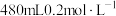 的
的 溶液,需要使用的玻璃仪器有
溶液,需要使用的玻璃仪器有a.用托盘天平称量
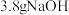 固体进行配制溶液
固体进行配制溶液b.定容时俯视刻度线
c.未待溶解的
 浓溶液冷却即转移至相应容器进行后继操作
浓溶液冷却即转移至相应容器进行后继操作d.定容摇匀后发现液面低于刻度线,再次加入蒸馏水至刻度线
(2)乙同学欲比较
 固体和
固体和 固体的热稳定性,设计实验装置如下图:
固体的热稳定性,设计实验装置如下图:
①
 烧杯中的现象是
烧杯中的现象是②
 处应放置的药品是
处应放置的药品是③热稳定性:

 (大于、小于)
(大于、小于)(3)丙同学为探究
 的强氧化性,某设计了下图实验装置。
的强氧化性,某设计了下图实验装置。
实验步骤及现象如下:
Ⅰ.检查装置气密性后,装入药品并连接仪器。
Ⅱ.缓慢通入一定量的
 后,封闭
后,封闭 气体通路,将装置
气体通路,将装置 连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,
连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸, 中剧烈反应,有黄绿色气体产生。
中剧烈反应,有黄绿色气体产生。Ⅱ.待产生连续气泡后,将装置
 中的导管末端伸入集气瓶中,收集到无色气体。
中的导管末端伸入集气瓶中,收集到无色气体。①.
 中气体能使带火星的木条复燃,丙同学分析该气体不可能由
中气体能使带火星的木条复燃,丙同学分析该气体不可能由 还原
还原 所得,从氧化还原角度说明理由:
所得,从氧化还原角度说明理由:②.资料显示,
 也能与干燥
也能与干燥 反应产生
反应产生 ,写出反应的化学方程式
,写出反应的化学方程式
您最近半年使用:0次
名校
4 . 海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如ClO2、Na2O2、NaClO等。下列物质性质与用途具有对应关系的是
| A.Na2CO3溶液显碱性,可用作抗酸药物 |
| B.ClO2气体呈黄绿色,可用作自来水消毒剂 |
| C.Na2O2具有还原性,可用作供氧剂 |
| D.NaClO具有强氧化性,可用作漂白液 |
您最近半年使用:0次
2024-01-21更新
|
154次组卷
|
2卷引用:江苏省泰州中学、宿迁中学、宜兴中学2023-2024学年高三上学期12月调研测试化学试卷
5 . 物质的性质决定用途,下列两者对应关系不正确的是
| A.碳酸钠溶液显碱性,可用作食用碱或工业用碱 |
| B.小苏打受热易分解,可用作治疗胃酸过多的一种药剂 |
| C.次氯酸有强氧化性,可用作棉、麻和纸张的漂白剂 |
| D.钠有较强还原性,可用作冶炼钛、锆、铌等金属 |
您最近半年使用:0次
名校
解题方法
6 . 某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
(1)KClO4中氯元素的化合价是___________ ,具有___________ (填“还原性”或“氧化性”)。
(2)Fe2O3可处理产生的Na,反应为6Na + Fe2O3 = 3Na2O + 2Fe,反应中Na做___________ (填“还原剂”或“氧化剂”)。
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是___________ 。若不用Fe2O3处理产生的Na,Na可与NaHCO3分解产生的水反应,写出Na与水反应的离子方程式___________ 。
(4)按如图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是___________ 。

(5)下列关于Na2CO3和NaHCO3的说法中,正确的是___________ (填字母)。
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
(1)KClO4中氯元素的化合价是
(2)Fe2O3可处理产生的Na,反应为6Na + Fe2O3 = 3Na2O + 2Fe,反应中Na做
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是
(4)按如图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是

(5)下列关于Na2CO3和NaHCO3的说法中,正确的是
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
您最近半年使用:0次
名校
7 . 下列物质的性质与应用有对应关系的是
| A.氨气沸点低,工业上常用液氨作制冷剂 |
| B.HNO3有强氧化性,可用于溶解银 |
| C.Na2CO3溶液显碱性,可以用来治疗胃酸过多 |
| D.ClO2具有还原性,可用于自来水的杀菌消毒 |
您最近半年使用:0次
8 . 物质的性质决定物质的用途,下列说法不正确的是
| A.过氧化钠有强氧化性,可用于饮用水杀菌消毒 |
| B.碳酸钠溶液显碱性,可用作食用碱或工业用碱 |
| C.不锈钢具有很强的抗腐蚀能力,常用于制造餐具 |
| D.铁粉具有还原性,可用作食品抗氧化剂 |
您最近半年使用:0次
19-20高一·浙江·期中
解题方法
9 . 某校化学社团活动小组同学在学习完钠、氯及其化合物后设计了如下两组探究实验。
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。
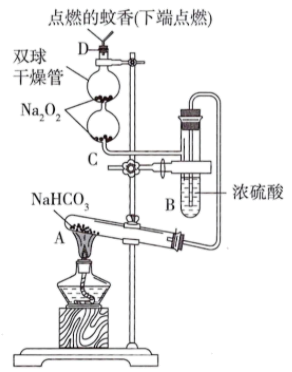
(1)Na2O2的物质类别是___ 。
(2)试管A中发生反应的化学方程式为___ 。
(3)双球干燥管内及D处观察到的实验现象是___ 。
实验二:对新教材中Cl2的实验室制法进行改进,验证Cl2的部分性质并收集一瓶干燥的Cl2。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(4)按气流方向,装置的连接顺序为___ (填仪器接口的小写字母,装置不可重复使用)。
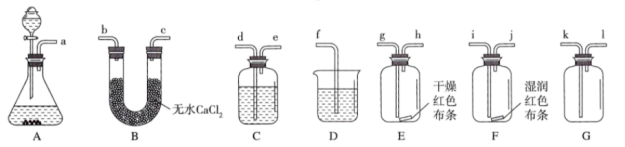
(5)实验时,装置C中所盛装的试剂名称是___ 。
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。

(1)Na2O2的物质类别是
(2)试管A中发生反应的化学方程式为
(3)双球干燥管内及D处观察到的实验现象是
实验二:对新教材中Cl2的实验室制法进行改进,验证Cl2的部分性质并收集一瓶干燥的Cl2。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(4)按气流方向,装置的连接顺序为

(5)实验时,装置C中所盛装的试剂名称是
您最近半年使用:0次
名校
10 . 海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解方法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如 、
、 、
、 等。下列物质性质与用途具有对应关系的是
等。下列物质性质与用途具有对应关系的是
 、
、 、
、 等。下列物质性质与用途具有对应关系的是
等。下列物质性质与用途具有对应关系的是A. 溶液显碱性,可用作除油污剂 溶液显碱性,可用作除油污剂 | B. 受热易分解,可用作抗酸药物 受热易分解,可用作抗酸药物 |
C. 具有还原性,可用作供氧剂 具有还原性,可用作供氧剂 | D. 具有强氧化性,可用作混凝剂 具有强氧化性,可用作混凝剂 |
您最近半年使用:0次
2023-11-15更新
|
233次组卷
|
2卷引用:江苏省泰州市2023-2024学年高三上学期期中考试化学试题



