名校
1 . 海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如ClO2、Na2O2、NaClO等。下列物质性质与用途具有对应关系的是
| A.Na2CO3溶液显碱性,可用作抗酸药物 |
| B.ClO2气体呈黄绿色,可用作自来水消毒剂 |
| C.Na2O2具有还原性,可用作供氧剂 |
| D.NaClO具有强氧化性,可用作漂白液 |
您最近一年使用:0次
2024-01-21更新
|
169次组卷
|
2卷引用:江苏省泰州中学、宿迁中学、宜兴中学2023-2024学年高三上学期12月调研测试化学试卷
名校
2 . 劳动创造美好生活。下列与劳动项目相关的解释正确的是
| 选项 | 劳动项目 | 解释 |
| A | 工人向食品中添加少许维生素C防止食品变质 | 维生素C有较强还原性 |
| B | 医护人员利用酒精消毒 | 乙醇具有强氧化性 |
| C | 科学家用硅材料制作各种电脑芯片 | SiO2可以传导光信号 |
| D | 面包师用小苏打作发泡剂烘焙面包 | NaHCO3溶液显碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-22更新
|
328次组卷
|
4卷引用:广东省广州市天河区2023-2024学年高三上学期10月份调研化学试题
19-20高一·浙江·期中
解题方法
3 . 某校化学社团活动小组同学在学习完钠、氯及其化合物后设计了如下两组探究实验。
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。
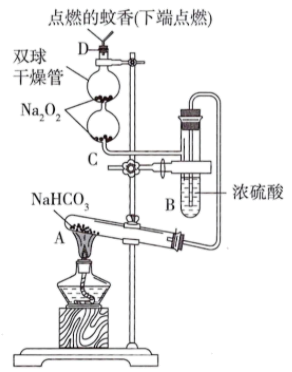
(1)Na2O2的物质类别是___ 。
(2)试管A中发生反应的化学方程式为___ 。
(3)双球干燥管内及D处观察到的实验现象是___ 。
实验二:对新教材中Cl2的实验室制法进行改进,验证Cl2的部分性质并收集一瓶干燥的Cl2。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(4)按气流方向,装置的连接顺序为___ (填仪器接口的小写字母,装置不可重复使用)。
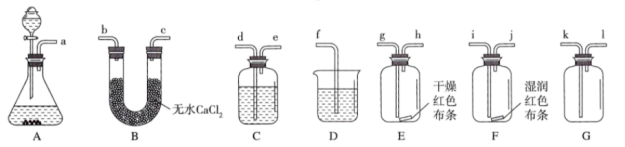
(5)实验时,装置C中所盛装的试剂名称是___ 。
实验一:探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。

(1)Na2O2的物质类别是
(2)试管A中发生反应的化学方程式为
(3)双球干燥管内及D处观察到的实验现象是
实验二:对新教材中Cl2的实验室制法进行改进,验证Cl2的部分性质并收集一瓶干燥的Cl2。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(4)按气流方向,装置的连接顺序为

(5)实验时,装置C中所盛装的试剂名称是
您最近一年使用:0次
4 . 物质的性质决定物质的用途,下列说法不正确的是
| A.过氧化钠有强氧化性,可用于饮用水杀菌消毒 |
| B.碳酸钠溶液显碱性,可用作食用碱或工业用碱 |
| C.不锈钢具有很强的抗腐蚀能力,常用于制造餐具 |
| D.铁粉具有还原性,可用作食品抗氧化剂 |
您最近一年使用:0次
解题方法
5 . 下列物质的性质和用途之间的对应关系正确的是
A. 沸点低,工业上常用液氨作制冷剂 沸点低,工业上常用液氨作制冷剂 |
B. 有强氧化性,可用于溶解银 有强氧化性,可用于溶解银 |
C. 溶液显碱性,常作烘焙糕点的膨松剂 溶液显碱性,常作烘焙糕点的膨松剂 |
D. 具有还原性,可用于除去废水中的 具有还原性,可用于除去废水中的 |
您最近一年使用:0次
2023-02-22更新
|
0次组卷
|
4卷引用:山东省潍坊市2023届高三下学期一模考试化学试题
山东省潍坊市2023届高三下学期一模考试化学试题山东省单县第二中学2023届高三下学期第1次 阶段性质量检测化学试题(已下线)专题05 元素化合物及其性质(已下线)2023年高考山东卷化学真题变式题(选择题1-5)
解题方法
6 . 化学与生活紧密相关,下列与化学知识有关的描述正确的是
| A.小苏打可用作食品膨松剂,利用其水溶液呈碱性 |
B. 可用于饮用水消毒,利用了其强氧化性 可用于饮用水消毒,利用了其强氧化性 |
C. 用于制作光导纤维,利用了其半导体的特性 用于制作光导纤维,利用了其半导体的特性 |
| D.镁铝合金用于制作航天器外壳,利用了其强还原性 |
您最近一年使用:0次
名校
7 . 下列有关物质的性质与用途具有对应关系的是
A. 具有强氧化性,可用于制备硝酸铵 具有强氧化性,可用于制备硝酸铵 |
B. 具有还原性,可用于纸浆漂白 具有还原性,可用于纸浆漂白 |
C. 具有两性,可用于电解冶炼铝 具有两性,可用于电解冶炼铝 |
D. 溶液显碱性,可用于制胃酸中和剂 溶液显碱性,可用于制胃酸中和剂 |
您最近一年使用:0次
2022-09-03更新
|
342次组卷
|
3卷引用:江苏省海安市2022-2023学年高三上学期期初学业质量监测化学试题
8 . 金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为___________ ,采用空气和Na为原料可直接制备Na2O2.空气与熔融的金属Na反应前需依次通过的试剂为___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)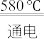 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是___________ 。
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
①配平上述离子方程式___________ 。
②该反应说明Na2O2具有___________ (选填“氧化性”“还原性"或“漂白性”)。
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为___________ 。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
A.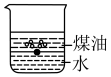 | B.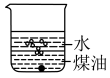 |
C. | D. |
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)
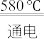 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O①配平上述离子方程式
②该反应说明Na2O2具有
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为
您最近一年使用:0次
名校
解题方法
9 . 钠是一种活泼金属,其化合物在生产生活中具有广泛应用。
(1)下列有关钠及其化合物的说法正确的是___________。
(2)下列试剂可以鉴别NaHCO3溶液和Na2CO3溶液的是___________。
(3)Na2O2因能与 CO2反应可作潜水艇的供氧剂,涉及的反应方程式为___________ 。
(4)向酸性KMnO4液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:MnO +Na2O2+____=_______Mn2++______Na++________+__________,全方程式并配平
+Na2O2+____=_______Mn2++______Na++________+__________,全方程式并配平________ ,该反应说明Na2O2粉末具有___________ 填“氧化性”“还原性”或“漂白性”)。该反应中被还原的元素是___________ (填元素名称)。
(5)将过氧化钠粉末投入到氯化亚铁溶液中,有关现象说法正确的是___________。
(6)向 100mLNaOH 溶液中通入一定量CO2充分反应后,向所得溶液中,逐滴滴加盐酸,所得气体的体积与所加盐酸体积的关系如图所示。

①由图分析,NaOH 溶液中通入一定量(CO2充分反应后所得溶液的溶质为___________ 。
②滴加盐酸时,OA段发生反应的离子方程式为___________ 。
(1)下列有关钠及其化合物的说法正确的是___________。
| A.少量钠保存在酒精中 | B.Na2O2是白色固体,性质不稳定 |
| C.热稳定性:NaHCO3<Na2CO3 | D.NaOH常用来治疗胃酸过多 |
(2)下列试剂可以鉴别NaHCO3溶液和Na2CO3溶液的是___________。
| A.Ba(OH)2 | B.NaOH 溶液 | C.CaCl2溶液 | D.稀盐酸 |
(3)Na2O2因能与 CO2反应可作潜水艇的供氧剂,涉及的反应方程式为
(4)向酸性KMnO4液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:MnO
 +Na2O2+____=_______Mn2++______Na++________+__________,全方程式并配平
+Na2O2+____=_______Mn2++______Na++________+__________,全方程式并配平(5)将过氧化钠粉末投入到氯化亚铁溶液中,有关现象说法正确的是___________。
| A.生成红褐色沉淀 | B.没有气体产生 | C.生成白色沉淀 | D.有无色气体产生 |
(6)向 100mLNaOH 溶液中通入一定量CO2充分反应后,向所得溶液中,逐滴滴加盐酸,所得气体的体积与所加盐酸体积的关系如图所示。

①由图分析,NaOH 溶液中通入一定量(CO2充分反应后所得溶液的溶质为
②滴加盐酸时,OA段发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题
(1)呼吸面具中的供氧剂与二氧化碳反应的化学方程式_______ ,该反应与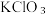 分解反应相比较,产生等分子数的气体,转移电子数目之比为
分解反应相比较,产生等分子数的气体,转移电子数目之比为_______ 。
(2) 溶于水,书写电离方程式
溶于水,书写电离方程式_______ ;检验该溶液中是否含有  ,所需试剂
,所需试剂_______ (填化学式),离子方程式_______ ;除去该溶液中的 杂质,涉及的离子方程式
杂质,涉及的离子方程式_______ ;检验 溶液中是否含有
溶液中是否含有 ,实验操作名称为
,实验操作名称为_______ 。
(3)分别取含等质量溶质的氢氧化钠溶液各 100mL,再分别通入一定量的 ,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
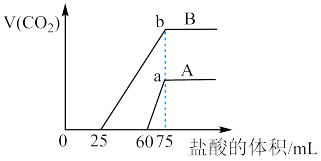
①在A情况下,加入盐酸0-60mL过程中,发生反应的离子方程式依次为_______ 、_______ 。
②图中a、b两点所示的溶液(加入盐酸均为75mL时)溶质分别为_______ 、_______ (生成的 全部逸出),所含溶质的质量大小关系
全部逸出),所含溶质的质量大小关系_______
A. 相等 B. b点质量大 C. a 点质量大
(4) (O为-l价)性质与
(O为-l价)性质与 类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性
类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性 溶液、酸化的KI溶液与
溶液、酸化的KI溶液与 溶液反应验证其性质。(已知:淀粉遇
溶液反应验证其性质。(已知:淀粉遇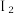 变蓝)
变蓝)

实验①利用了酸性高锰酸钾的_______ 性质,该实验中,证明 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有_______ 。
实验②是为了验证 的
的_______ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式_______ 。
(1)呼吸面具中的供氧剂与二氧化碳反应的化学方程式
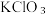 分解反应相比较,产生等分子数的气体,转移电子数目之比为
分解反应相比较,产生等分子数的气体,转移电子数目之比为(2)
 溶于水,书写电离方程式
溶于水,书写电离方程式 ,所需试剂
,所需试剂 杂质,涉及的离子方程式
杂质,涉及的离子方程式 溶液中是否含有
溶液中是否含有 ,实验操作名称为
,实验操作名称为(3)分别取含等质量溶质的氢氧化钠溶液各 100mL,再分别通入一定量的
 ,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
①在A情况下,加入盐酸0-60mL过程中,发生反应的离子方程式依次为
②图中a、b两点所示的溶液(加入盐酸均为75mL时)溶质分别为
 全部逸出),所含溶质的质量大小关系
全部逸出),所含溶质的质量大小关系A. 相等 B. b点质量大 C. a 点质量大
(4)
 (O为-l价)性质与
(O为-l价)性质与 类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性
类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性 溶液、酸化的KI溶液与
溶液、酸化的KI溶液与 溶液反应验证其性质。(已知:淀粉遇
溶液反应验证其性质。(已知:淀粉遇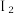 变蓝)
变蓝)
实验①利用了酸性高锰酸钾的
 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有实验②是为了验证
 的
的
您最近一年使用:0次



