解题方法
1 . 实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定该瓶样品中氢氧化钠的质量分数,现取17.3g该样品溶于足量的水中(固体完全溶解),向所得溶液中逐滴加入200g一定溶质质量分数的稀盐酸,实验过程如图所示(不考虑碳酸钠的分步反应)。
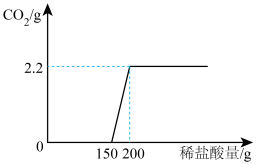
(1)经分析,该氢氧化钠固体_______ (填“部分”或“完全”)变质,恰好完全反应时,产生气体的质量为_______ g。
(2)计算样品中氢氧化钠的质量_______ (写出计算过程)。

(1)经分析,该氢氧化钠固体
(2)计算样品中氢氧化钠的质量
您最近一年使用:0次
解题方法
2 .  常作漂白剂、杀菌剂、消毒剂。
常作漂白剂、杀菌剂、消毒剂。 保存不当易吸收空气中的
保存不当易吸收空气中的 而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
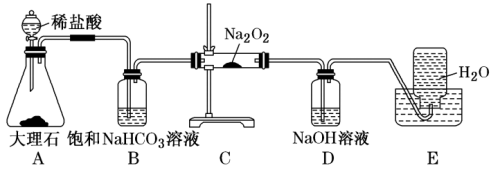
(1)盛稀盐酸的仪器名称为_______ ,A装置为 的发生装置,该反应的化学方程式为
的发生装置,该反应的化学方程式为_______________________________ 。
(2)B中 溶液可除去
溶液可除去 中的
中的 ,则B中反应的化学方程式为
,则B中反应的化学方程式为_______ 。
(3)C装置为 的发生装置,写出
的发生装置,写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(4)D中 溶液的作用是
溶液的作用是_______ 。
(5)E装置为排水法收集 的装置,检验所收集的气体为
的装置,检验所收集的气体为 的方法为
的方法为_______ 。
 常作漂白剂、杀菌剂、消毒剂。
常作漂白剂、杀菌剂、消毒剂。 保存不当易吸收空气中的
保存不当易吸收空气中的 而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
而变质。该小组欲进一步测定其变质的程度,他们称取ag样品,设计用如图组合装置来测定该样品中过氧化钠的质量分数。请回答以下问题:
(1)盛稀盐酸的仪器名称为
 的发生装置,该反应的化学方程式为
的发生装置,该反应的化学方程式为(2)B中
 溶液可除去
溶液可除去 中的
中的 ,则B中反应的化学方程式为
,则B中反应的化学方程式为(3)C装置为
 的发生装置,写出
的发生装置,写出 与
与 反应的化学方程式
反应的化学方程式(4)D中
 溶液的作用是
溶液的作用是(5)E装置为排水法收集
 的装置,检验所收集的气体为
的装置,检验所收集的气体为 的方法为
的方法为
您最近一年使用:0次
解题方法
3 . 某变质小苏打样品中含Na2CO3,取m克样品用如图装置测定Na2CO3含量,下列说法不正确的是
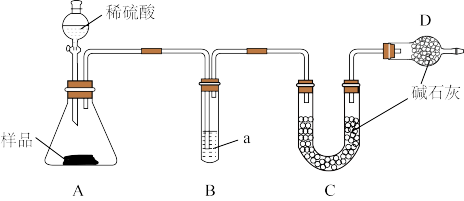

| A.装置B所装试剂a是浓硫酸,其作用是干燥CO2 |
| B.装置D的作用是防止空气中的H2O、CO₂进入装置C |
| C.反应后称量装置C的质量为n克,用数据m、n可求得Na2CO3含量 |
| D.上述装置的不足之处是没有在A装置前接一个赶气装置 |
您最近一年使用:0次
名校
解题方法
4 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验溶液中是否含Cl- | 先向某溶液中加入稀盐酸酸化,再加入AgNO3溶液 | 若有白色沉淀,说明含有Cl- |
| B | 鉴别NaHCO3与Na2CO3 | 取少许两种物质,加入几滴水,插入温度计,测温 | 温度降低的是Na2CO3 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2-3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| D | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-02更新
|
228次组卷
|
3卷引用:浙江省余姚中学2022-2023学年高一上学期10月月考化学试题
名校
解题方法
5 . 钠和钠的化合物是实验室中常用药品。
(1)少量的钠应保存在_______________ 中。
(2)化学小组用金属钠和空气制备纯度较高的 (不考虑空气中的
(不考虑空气中的 ),可利用的装置如下。
),可利用的装置如下。
回答下列问题:
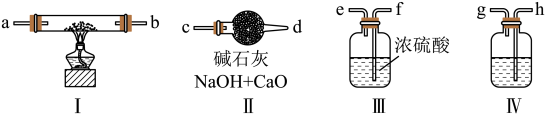
①装置Ⅳ中盛放的药品是__________ 溶液(填化学式),若没有该装置可能导致生成的 中含有杂质,
中含有杂质,  产生该杂质的化学方程式为
产生该杂质的化学方程式为__________ 。
②若规定气流的方向为从左到右,各仪器连接的顺序是:空气进入_______,_______接_______,_______接a,b接c(填字母)。_______
(3)小苏打长期放置在空气中会变质(部分转变为 ),化学小组欲测定某小苏打样品中
),化学小组欲测定某小苏打样品中 的质量分数,设计如下实验方案:
的质量分数,设计如下实验方案:
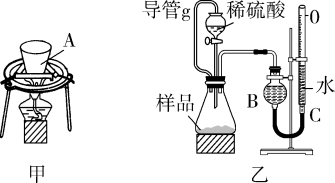
Ⅰ:加热分解法:利用图甲装置,充分加热小苏打样品。
①仪器A的名称为________ 。
②发生反应的化学方程式为_____________________________ 。
Ⅱ:测量气体体积法:利用图乙装置,测定反应生成气体的体积。
①组装好仪器,检查装置气密性,添加药品。为了减小实验误差,B、C中最好用________ 溶液代替水。
②若所取样品的质量为mg,反应前滴定管C的读数为 mL,反应结束后滴定管C的读数为
mL,反应结束后滴定管C的读数为 mL,(滴定管的0刻度在上方)则样品中
mL,(滴定管的0刻度在上方)则样品中 和
和 的物质的量之和为
的物质的量之和为________ (气体体积均已换算为标准状况下的体积)。
(1)少量的钠应保存在
(2)化学小组用金属钠和空气制备纯度较高的
 (不考虑空气中的
(不考虑空气中的 ),可利用的装置如下。
),可利用的装置如下。回答下列问题:

①装置Ⅳ中盛放的药品是
 中含有杂质,
中含有杂质,  产生该杂质的化学方程式为
产生该杂质的化学方程式为②若规定气流的方向为从左到右,各仪器连接的顺序是:空气进入_______,_______接_______,_______接a,b接c(填字母)。
(3)小苏打长期放置在空气中会变质(部分转变为
 ),化学小组欲测定某小苏打样品中
),化学小组欲测定某小苏打样品中 的质量分数,设计如下实验方案:
的质量分数,设计如下实验方案:
Ⅰ:加热分解法:利用图甲装置,充分加热小苏打样品。
①仪器A的名称为
②发生反应的化学方程式为
Ⅱ:测量气体体积法:利用图乙装置,测定反应生成气体的体积。
①组装好仪器,检查装置气密性,添加药品。为了减小实验误差,B、C中最好用
②若所取样品的质量为mg,反应前滴定管C的读数为
 mL,反应结束后滴定管C的读数为
mL,反应结束后滴定管C的读数为 mL,(滴定管的0刻度在上方)则样品中
mL,(滴定管的0刻度在上方)则样品中 和
和 的物质的量之和为
的物质的量之和为
您最近一年使用:0次
6 . 关于下列实验操作、现象和相应结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用CCl4萃取碘水后,先从下口放出下层溶液,再向另一个烧杯中从下口放出上层液体 | 下层溶液为紫色,上层为无色 | CCl4的密度比水大且碘在CCl4中溶解度比在水中的大 |
| B | 向过氧化钠样品中滴加过量的盐酸,将生成的气体通入CaCl2溶液 | 无白色沉淀产生 | 样品未变质 |
| C | 鉴别碳酸钠、碳酸氢钠溶液,向装有两溶液的两支试管中滴加氢氧化钡溶液 | 一支试管无明显现象,一支试管中产生白色沉淀 | 产生白色沉淀的溶液是碳酸钠 |
| D | 向NaBr溶液中加入少量苯,通入适量Cl2后,充分振荡、静置 | 有机层变为橙红色 | Cl2的氧化性强于Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 以下实验设计能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 除去碳酸氢钠固体中的碳酸铵 | 将固体加热至恒重 |
| B | 制备无水氯化铝 | 蒸干铝与稀盐酸反应后的溶液 |
| C | 证明Na2O2没有变质 | 取Na2O2粉末样品,向其中滴加过量的盐酸 |
| D | 鉴别碳酸钠和碳酸氢钠 | 分别向待检样品溶液滴加稀硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列有关实验的描述正确的是
| A.向碘化钠稀溶液中加入新制氯水立即生成大量紫黑色固体 |
| B.中和热测定时环形玻璃搅拌棒要不断顺时针搅拌,目的是为了混合均匀,充分反应 |
| C.将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,变红,说明样品变质 |
| D.向分别装有1g Na2CO3和NaHCO3固体的试管中滴入几滴水,温度高的为Na2CO3 |
您最近一年使用:0次
名校
解题方法
9 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,用分析天平称称取1.7240g样品溶于水,配成500mL溶液。取出25.00mL该溶液,加入一定物质的量浓度的Ba(OH)2溶液至20.00mL时沉淀量达到最大值,过滤、洗涤、干燥,称量沉淀质量为0.1970 g。请计算:
(1)所加Ba(OH)2溶液的物质的量浓度为______ mol·L-1
(2)样品中n(NaHCO3) ∶n(Na2CO3)=___
(1)所加Ba(OH)2溶液的物质的量浓度为
(2)样品中n(NaHCO3) ∶n(Na2CO3)=
您最近一年使用:0次
2020-11-26更新
|
219次组卷
|
6卷引用:浙江省杭州地区(含周边)重点中学2020-2021学年高一上学期期中考试化学试题
浙江省杭州地区(含周边)重点中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】86.(已下线)【浙江新东方】108(已下线)【浙江新东方】在线化学21(已下线)【萧山新东方】萧山试卷解析浙江省瑞安中学2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
10 . 小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组欲测定某小苏打样品中NaHCO3的质量分数,设计如图实验方案:
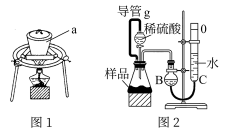
Ⅰ.加热分解法:利用图1装置,充分加热小苏打样品。
将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:

(1)仪器a的名称为______ 。在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是______ (填字母)。
a.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
b.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
(2)操作Ⅲ的方法为______ 、______ 、______ 。
(3)所得晶体中碳酸氢钠的纯度为_____ 。
Ⅱ.测量气体体积法:利用图2装置,测定反应生成气体的体积。
(4)组装好仪器后,首先进行的操作为______ 。
(5)导管g的作用为______ 。
(6)为了减小实验误差,B、C中最好用______ 溶液代替水。
(7)待反应结束,气体冷却至室温后,利用图示装置读取气体体积时,应注意的事项如下:①_____ 。②_____ 。
(8)若所取样品的质量为m g,反应前量气管C的读数为V1 mL,反应结束后量气管C的读数为V2 mL,则样品中NaHCO3和Na2CO3的物质的量之和为__ (气体体积均为标准况)。

Ⅰ.加热分解法:利用图1装置,充分加热小苏打样品。
将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:

(1)仪器a的名称为
a.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
b.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
(2)操作Ⅲ的方法为
(3)所得晶体中碳酸氢钠的纯度为
Ⅱ.测量气体体积法:利用图2装置,测定反应生成气体的体积。
(4)组装好仪器后,首先进行的操作为
(5)导管g的作用为
(6)为了减小实验误差,B、C中最好用
(7)待反应结束,气体冷却至室温后,利用图示装置读取气体体积时,应注意的事项如下:①
(8)若所取样品的质量为m g,反应前量气管C的读数为V1 mL,反应结束后量气管C的读数为V2 mL,则样品中NaHCO3和Na2CO3的物质的量之和为
您最近一年使用:0次



