解题方法
1 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
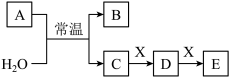
(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__ 。证明D已经氧化变质的方法是:取少量D固体溶于水中,__ 。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为__ ,则X可能为__ (填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为__ 。若X为一种最常见的造成温室效应的气体。若鉴别等浓度的D、E两种溶液,可选择的试剂为__ (填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为__ ,E是__ (填化学式)。

(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为
您最近一年使用:0次
3 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
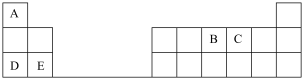
完成下列填空(填元素符号或化学式):
(1)元素C在元素周期表中的位置是__________ ,B、C、E三种元素原子半径从大到小的顺序是__________ ;
(2)D简单离子的结构示意图为______________ ,D的金属性________ E的金属性(填“大于”“小于”“等于”)。D单质在空气中燃烧可生成淡黄色粉末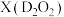 ,
, 的电子式为
的电子式为___________ ,D的最高价氧化物对应的水化物中含有的化学键类型有_________ 。
(3)将 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
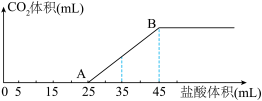
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
①AB段发生反应的离子方程式为____________ 。
②原固体混合物中 与
与 的物质的量之比为
的物质的量之比为____________ 。

完成下列填空(填元素符号或化学式):
(1)元素C在元素周期表中的位置是
(2)D简单离子的结构示意图为
 ,
, 的电子式为
的电子式为(3)将
 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
①AB段发生反应的离子方程式为
②原固体混合物中
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
4 . A、B、C、D、E、F、G六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;A、D同主族,D的焰色反应为黄色;E的简单阳离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C、G两种元素的原子最外层共有13个电子。则
(1)F在元素周期表中的位置为_______________ 。
(2)用电子式表示D2F的形成过程_____________ 。
(3)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为__________________________ 。
(4)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________ 。
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________ 。
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
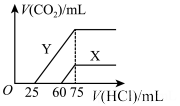
则曲线Y表明M中的溶质为________ ;原NaOH溶液的物质的量浓度为_______ ;由曲线X、Y可知,两次实验通入的CO2的体积比为_________ 。
(1)F在元素周期表中的位置为
(2)用电子式表示D2F的形成过程
(3)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为
(4)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
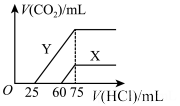
则曲线Y表明M中的溶质为
您最近一年使用:0次
名校
5 . A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。用化学用语回答下列问题:
(1)F在元素周期表中的位置为__ 。
(2)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。H的电子式为___ ,写出在空气中长期放置生成H的化学反应方程式为:__ 。
(3)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
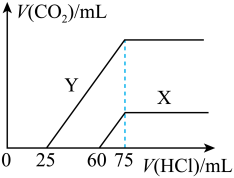
则曲线Y表明M中的溶质为___ ;原NaOH溶液的物质的量浓度为__ ;由曲线X、Y可知,两次实验通入的CO2的体积比为__ 。
(1)F在元素周期表中的位置为
(2)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。H的电子式为
(3)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。

则曲线Y表明M中的溶质为
您最近一年使用:0次
解题方法
6 . X、Y、Z、M、W为原子序数依次增大的短周期元素。已知:
①化合物MaYbXc中a、b、c均为整数,三者之和为13。
②取0.1 mol上述化合物与过量的水反应产生4.8 g气体A,同时生成0.1 mol白色胶状沉淀B,B既能溶于NaOH溶液,又能溶于盐酸。
③A是最简单的有机物,可导致地球表面温室效应不断增加。
④C、D、E、F、G五种物质均含有W元素,C为单质,E和F均为二元化合物且相对分子质量相差16。它们之间有如下转化关系。

⑤Z与W族序数相差5。
回答下列问题:
(1)Y和Z的名称分别为________ 、_______ 。W在周期表中的位置为______ 。
(2)B、F的化学式分别为_____ 、____ 。Y与W形成的二元化合物电子式为_____ 。
(3)MaYbXc与水反应的化学方程式为________________ 。
(4)在④中,D→E化学方程式为_______________ 。
(5)若C、D、E、F、G五种物质均含有Z元素,且发生如上图所示的转化关系。C为淡黄色固体,惰性电极电解F的水溶液可生成D和两种气体单质,则F→G的化学方程式为__________ 。
①化合物MaYbXc中a、b、c均为整数,三者之和为13。
②取0.1 mol上述化合物与过量的水反应产生4.8 g气体A,同时生成0.1 mol白色胶状沉淀B,B既能溶于NaOH溶液,又能溶于盐酸。
③A是最简单的有机物,可导致地球表面温室效应不断增加。
④C、D、E、F、G五种物质均含有W元素,C为单质,E和F均为二元化合物且相对分子质量相差16。它们之间有如下转化关系。

⑤Z与W族序数相差5。
回答下列问题:
(1)Y和Z的名称分别为
(2)B、F的化学式分别为
(3)MaYbXc与水反应的化学方程式为
(4)在④中,D→E化学方程式为
(5)若C、D、E、F、G五种物质均含有Z元素,且发生如上图所示的转化关系。C为淡黄色固体,惰性电极电解F的水溶液可生成D和两种气体单质,则F→G的化学方程式为
您最近一年使用:0次
7 . 非金属及其化合物在生产、生活中应用广泛。
Ⅰ.CO2的有效利用可以缓解温室效应和能源短缺问题,CO2的分子结构决定了其性质和用途。
(1) CO2的电子式是_______ ,包含的化学键类型为_______ 共价键(填“非极性”或“极性”)。
(2) 在温度高于31.26 ℃、压强高于7.29×106 Pa时,CO2处于超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有_______ (答出一点即可)。
Ⅱ.某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。
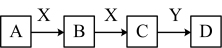
(3)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
①组成A的元素在周期表中的位置是_______ 。
②下列说法正确的是______ (填字母)。
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(4)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是________ 。
② A用于呼吸面具或潜水艇中氧气的来源,若A和X反应生成1 mol B时,转移电子数为______ 。
③ C与Y反应生成X的离子方程式_________ 。
Ⅰ.CO2的有效利用可以缓解温室效应和能源短缺问题,CO2的分子结构决定了其性质和用途。
(1) CO2的电子式是
(2) 在温度高于31.26 ℃、压强高于7.29×106 Pa时,CO2处于超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有
Ⅱ.某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。

(3)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
①组成A的元素在周期表中的位置是
②下列说法正确的是
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(4)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是
② A用于呼吸面具或潜水艇中氧气的来源,若A和X反应生成1 mol B时,转移电子数为
③ C与Y反应生成X的离子方程式
您最近一年使用:0次
名校
解题方法
8 . 下表是元素周期表的一部分,表中的每个字母代表一种元素,请根据要求回答问题。
(1)元素g在元素周期表的位置为____________________ 。
(2)b和g两种元素的原子半径大小关系:b______ g(填“>”或“<”).
(3)由原子个数比为1:1:1的a、b、c三种元素组成的共价化合物X,共形成4对共用电子对,则X的结构式为______________ 。
(4)f的最高价氧化物与e的最高价氧化物对应的水化物在溶液中反应的离子方程式为_________________________ 。
(5)A、B、D、E是由上述部分元素组成的化合物,它们之间的转化关系如图所示(部分产物已略去)。A、B、D的焰色反应均呈黄色,水溶液均为碱性。请回答:

①E的电子式为_______________ ,B的化学式为____________________ 。
②A中的化学键类型为____________________
③自然界中存在B、D和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5mo/L。若取相同质量的固体加热至质量不再发生变化,剩余固体的质量为___________ g。
| 族 周期 | ⅠA | 0 | |||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | b | c | d | ||||||
| 3 | e | f | g |
(2)b和g两种元素的原子半径大小关系:b
(3)由原子个数比为1:1:1的a、b、c三种元素组成的共价化合物X,共形成4对共用电子对,则X的结构式为
(4)f的最高价氧化物与e的最高价氧化物对应的水化物在溶液中反应的离子方程式为
(5)A、B、D、E是由上述部分元素组成的化合物,它们之间的转化关系如图所示(部分产物已略去)。A、B、D的焰色反应均呈黄色,水溶液均为碱性。请回答:

①E的电子式为
②A中的化学键类型为
③自然界中存在B、D和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5mo/L。若取相同质量的固体加热至质量不再发生变化,剩余固体的质量为
您最近一年使用:0次



