名校
1 . 下列物质性质与用途对应关系错误的是
| 选项 | 化学性质 | 用途 |
| A | HClO具有强氧化性 | 用于杀菌消毒 |
| B | 铁粉具有还原性 | 用作食品抗氧化剂 |
| C | NaHCO3受热易分解 | 用于治疗胃酸过多症 |
| D | Na2O2可与CO2、H2O反应产生O2 | 用作潜艇中的供氧剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-08更新
|
206次组卷
|
4卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期期末考试化学试题
解题方法
2 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:______ 。
(2)D单质与C单质在加热条件下反应产物的电子式________ ,该物质与A2C反应的离子方程式______ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为______ 。
(4)用电子式写出A2C的形成过程________ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)用电子式写出A2C的形成过程
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E五种物质的焰色反应都呈黄色,A、B分别与水反应都有气体放出,同时都生成C溶液,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,C与适量的F气体反应生成D,F是导致温室效应的主要气体,D溶液与F气体反应生成E,E加热能够生成D和F气体。
根据以上叙述回答下列问题:
(1)写出下列物质的化学式:
A________ 、B________ 、C________ 、D________ 、E________ 。
(2)B是否为碱性氧化物_________ (填“是”或“否”),B通常用作__________ (写一种用途),现有7.8g B与水反应得到200ml溶液,所得溶液的物质的量浓度为___________ mol/L。
(3)按要求完成方程式:
①写出E加热生成D和F的化学方程式_______________________ ;
②写出B与F反应的化学方程式__________________________ 。
根据以上叙述回答下列问题:
(1)写出下列物质的化学式:
A
(2)B是否为碱性氧化物
(3)按要求完成方程式:
①写出E加热生成D和F的化学方程式
②写出B与F反应的化学方程式
您最近一年使用:0次
名校
4 . 下列有关物质的性质与用途具有对应关系的是
A. 受热易分解,可用于治疗胃酸过多症 受热易分解,可用于治疗胃酸过多症 |
B. 溶液显酸性,可用于蚀刻铜制的电路板 溶液显酸性,可用于蚀刻铜制的电路板 |
C. 具有强氧化性,可用作自来水消毒剂 具有强氧化性,可用作自来水消毒剂 |
D. 密度比空气大,可用作镁着火时的灭火剂 密度比空气大,可用作镁着火时的灭火剂 |
您最近一年使用:0次
2023-01-07更新
|
347次组卷
|
4卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一下学期开学考试化学试题
5 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱。
I.先以NaCl、NH3、CO2和水等为原料,用如图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。
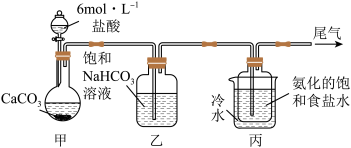
(1)装置丙中反应的化学方程式为_______ 。
(2)装置乙的作用是_____ ;装置丙中冷水的作用是_____ 。
(3)用装置丙中产生的NaHCO3可制取Na2CO3,其反应的化学方程式为_____ 。
II.为进一步探究Na2CO3和NaHCO3的性质,实验小组利用传感器继续做如图实验:
(查阅资料)溶液pH越小,OH-的浓度越小,溶液碱性越弱。
(4)实验I中,溶解时吸收热量的物质是_____ (填化学式)。
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为______ ,说明OH-未参与该反应的实验证据是______ 。
(6)实验II中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,原因是滴加NaHCO3溶液的烧杯中______ 参与了反应。
I.先以NaCl、NH3、CO2和水等为原料,用如图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。

(1)装置丙中反应的化学方程式为
(2)装置乙的作用是
(3)用装置丙中产生的NaHCO3可制取Na2CO3,其反应的化学方程式为
II.为进一步探究Na2CO3和NaHCO3的性质,实验小组利用传感器继续做如图实验:
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下面实验过程中温度的变化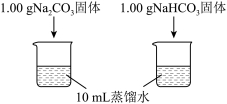 |  |
| 实验II | 测量下面实验过程中溶液pH的变化 注:Na2CO3溶液和NaHCO3溶液的浓度相等 | 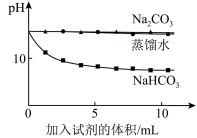 |
(4)实验I中,溶解时吸收热量的物质是
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(6)实验II中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,原因是滴加NaHCO3溶液的烧杯中
您最近一年使用:0次
名校
解题方法
6 . 化学是一门以实验为基础的学科,研究小组需要经常做实验。
(1)某研究小组甲模仿侯德榜制备纯碱,反应原理如下:
 即向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳,析出溶解度
即向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳,析出溶解度______ (填“较小”或“较大”)的碳酸氢钠。欲得到纯碱,该研究小组将固体过滤、洗涤后,还需进行的操作是______ (选装置),反应的化学方程式______ 。
A. B.
B.  C.
C.  D.
D.
(2)某研究小组乙在探究 的性质实验时,发现
的性质实验时,发现 样品与过量水反应,待完全反应不再产生氧气后,得溶液M。溶液M可使酸性
样品与过量水反应,待完全反应不再产生氧气后,得溶液M。溶液M可使酸性 溶液褪色,同时放出氧气。小组成员查阅资料表明,
溶液褪色,同时放出氧气。小组成员查阅资料表明, 与水反应还可生成
与水反应还可生成 。
。
① 与水反应生成
与水反应生成 的反应是否属于氧化还原反应
的反应是否属于氧化还原反应______ (填“是”或“否”)。
②写出 与水反应的离子反应方程式
与水反应的离子反应方程式______ 。
(1)某研究小组甲模仿侯德榜制备纯碱,反应原理如下:

 即向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳,析出溶解度
即向饱和食盐水中通入足量氨气至饱和,然后通入过量二氧化碳,析出溶解度A.
 B.
B.  C.
C.  D.
D.
(2)某研究小组乙在探究
 的性质实验时,发现
的性质实验时,发现 样品与过量水反应,待完全反应不再产生氧气后,得溶液M。溶液M可使酸性
样品与过量水反应,待完全反应不再产生氧气后,得溶液M。溶液M可使酸性 溶液褪色,同时放出氧气。小组成员查阅资料表明,
溶液褪色,同时放出氧气。小组成员查阅资料表明, 与水反应还可生成
与水反应还可生成 。
。①
 与水反应生成
与水反应生成 的反应是否属于氧化还原反应
的反应是否属于氧化还原反应②写出
 与水反应的离子反应方程式
与水反应的离子反应方程式
您最近一年使用:0次
7 . 下列陈述I与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述I | 陈述Ⅱ |
| A |  的氧化性强于 的氧化性强于 |  与 与 在暗处会发生爆炸; 在暗处会发生爆炸; 与 与 加热时会缓慢反应 加热时会缓慢反应 |
| B | 过氧化钠是碱性氧化物 | 过氧化钠能与酸反应 |
| C | 苏打受热易分解 | 苏打常用作食品膨松剂 |
| D | D与T的质子数和核外电子数均相同 | D与T的性质完全相同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 教材中的实验有助于理论知识的学习,下列说法不正确的是
| A | B | C | D |
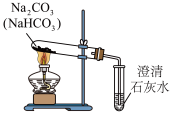 | 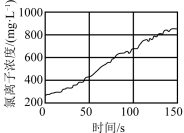 | 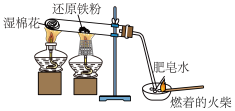 | 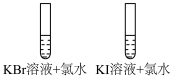 |
| 加热碳酸钠或碳酸氢钠 | 光照过程中氯水中氯离子的浓度变化 | 还原铁粉与水的反应 | 分别向 溶液和 溶液和 溶液中加入氯水 溶液中加入氯水 |
| 可以比较二者的热稳定性 | 氯离子浓度升高的原因是 分解 分解 | 用肥皂水和燃着的火柴检验氢气的生成 | 说明卤素单质的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-04更新
|
210次组卷
|
3卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期开学考试化学试题
9 . 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 小苏打可用于治疗胃酸过多 | NaHCO3可与盐酸反应 | Ⅰ对,Ⅱ对,无 |
| B | 向Na2O2的水溶液中滴入酚酞变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | 过氧化钠用于航天员的供氧剂 | Na2O2能和CO2、H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . “生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_____ (填序号,下同);属于盐类的是______ ;相互间能发生反应的是________ 。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是_______________ ,该变化称为______ 反应。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是__________________ 。
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:____________________________________________ 。
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是_____________________________________ ;苏打饼干可以适当缓解人体胃酸(主要成分盐酸)过多症状,该反应的离子方程式是__________________________________________ 。
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:______________ 。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(4)家庭中常用“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。
“消毒液”与“洁厕灵”同时使用会产生有毒的氯气,写出该反应的离子方程式:
(5)纯碱(Na2CO3)、小苏打(NaHCO3)广泛应用在食品加工。苏打饼干原料中含有小苏打,在烘焙受热过程中,小苏打发生分解反应,该反应的化学方程式是
(6)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
您最近一年使用:0次



