名校
解题方法
1 . 如图所示实验装置不能达到实验目的的是
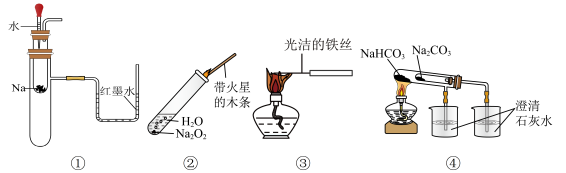
| A.利用装置①验证Na和水反应为放热反应 |
| B.利用装置②检验Na2O2与H2O反应有O2生成 |
| C.利用装置③观察纯碱的焰色试验的现象 |
| D.利用装置④比较Na2CO3和NaHCO3的热稳定性 |
您最近一年使用:0次
2024-01-05更新
|
146次组卷
|
3卷引用:甘肃省兰州新区贺阳高级中学2023-2024学年高一上学期期末考试化学试卷
名校
2 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。
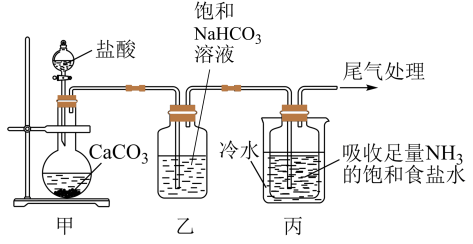
(1)装置乙的作用是_______ ,反应的化学方程式为_______ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为____ 。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、_______ ,最后一步发生反应的化学方程式为_______ 。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:
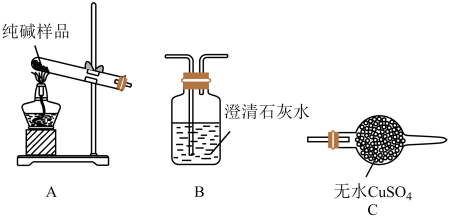
(5)测定该纯碱样品的纯度:称取m1g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为m2g。则该纯碱样品的纯度为_______ 。请另设计一个实验方案,测定纯碱样品的纯度(样品中只含有NaHCO3杂质)_______ 。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。

(1)装置乙的作用是
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

| 选择的装置(填编号) | 实验现象 | 实验结论 |
| 样品中含NaHCO3 |
您最近一年使用:0次
2022-08-21更新
|
474次组卷
|
2卷引用:甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷
名校
解题方法
3 . 按要求填空(每空2分,共20分)
(1)2Fe+3Cl2 2FeCl3,氧化剂是
2FeCl3,氧化剂是_______ ,发生氧化反应的是_______ 。
(2)将小块钠投入到硫酸铜的稀溶液中,观察到的现象是:①钠浮于液面上 ②熔化成小球 ③发出“嘶嘶”的响声,放出气体 ④有蓝色沉淀产生,用化学方程式解释实验现象:_______ 。
(3)某化学兴趣小组用如图装置制备家用消毒液。

①装置A中的溶液是_______ ,长玻璃导管的作用是_______ ,图中装置的连接顺序是B→_______ 。
②居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是_______ 。
(4)如图所示实验为“套管实验”,小试管内塞有沾有白色无水硫酸铜粉末的棉花球。

①点燃酒精灯加热,能观察到的实验现象是小试管中棉花_______ ,B烧杯中_______ 。
②实验结论:Na2CO3的热稳定性比NaHCO3_______ 。(填“强”或“弱”)
(1)2Fe+3Cl2
 2FeCl3,氧化剂是
2FeCl3,氧化剂是(2)将小块钠投入到硫酸铜的稀溶液中,观察到的现象是:①钠浮于液面上 ②熔化成小球 ③发出“嘶嘶”的响声,放出气体 ④有蓝色沉淀产生,用化学方程式解释实验现象:
(3)某化学兴趣小组用如图装置制备家用消毒液。

①装置A中的溶液是
②居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是
(4)如图所示实验为“套管实验”,小试管内塞有沾有白色无水硫酸铜粉末的棉花球。

①点燃酒精灯加热,能观察到的实验现象是小试管中棉花
②实验结论:Na2CO3的热稳定性比NaHCO3
您最近一年使用:0次
名校
4 . 用下列装置或操作进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 目的 | 等质量固体与足量盐酸反应,乙产生气泡快,反应后甲气球大 | 比较 、 、 的稳定性 的稳定性 | 探究氧化性: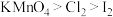 | 用铁丝蘸取碳酸钾溶液进行焰色试验 |
| 装置或操作 | 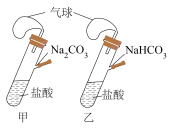 | 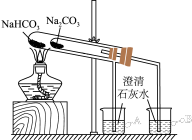 |  | 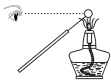 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列利用实验装置进行的实验不能达到实验目的的是
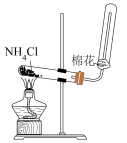 |  | 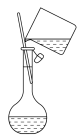 |  |
| A.制备并收集氨气 | B.探究 和 和 的稳定性强弱 的稳定性强弱 | C.配制1 氢氧化钠溶液 氢氧化钠溶液 | D.净化氯气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-24更新
|
158次组卷
|
4卷引用:广东省东莞市部分名校高三上(9月联考)-化学试题
名校
6 . 下列实验装置能达到实验目的的是
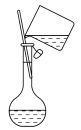 | 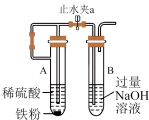 |
| A.配制0.10mol/L的食盐水 | B.制备少量Fe(OH)2 |
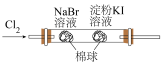 | 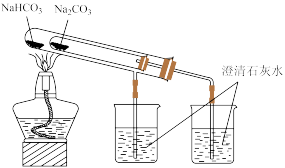 |
| C.证明氧化性Cl2>Br2>I2 | D.验证NaHCO3和Na2CO3的热稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-23更新
|
666次组卷
|
10卷引用:甘肃省张掖市高台县第一中学2023-2024学年高三上学期9月月考化学试题
甘肃省张掖市高台县第一中学2023-2024学年高三上学期9月月考化学试题河北省部分学校2023-2024学年高三一轮复习联考(一)化学试题湖南省百校联盟2023-2024学年高三上学期9月一轮复习联考化学试题河南省部分学校2023-2024学年高三上学期一轮复习联考(一)化学试题 山东省部分学校2023-2024学年高三上学期一轮复习联考(一)化学试题重庆市部分学校2023-2024学年高三一轮复习联考(一)化学试题安徽省灵璧中学2024届高三上学期一轮复习联考(一)化学试题江西省名校协作体2023-2024学年高三上学期11月期中化学试题 安徽省合肥市第一中学2023-2024学年高一上学期素质拓展训练(三)化学试题 广东省深圳市南山为明学校2023-2024学年高一上学期12月月考化学试题
名校
7 . 实验室用下列装置模拟侯氏制碱法制取少量NaHCO3固体。不能达到实验目的的是
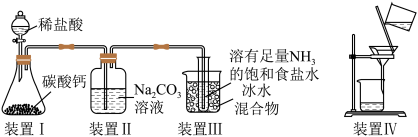

| A.装置Ⅰ制取CO2 |
| B.装置Ⅱ中Na2CO3溶液可除去CO2中的少量HCl |
| C.装置Ⅲ中冰水浴有利于析出NaHCO3固体 |
| D.装置Ⅳ可获得少量NaHCO3固体 |
您最近一年使用:0次
2022-05-15更新
|
2228次组卷
|
12卷引用:甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题
甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题江苏省前黄中学,溧阳中学2022届高三下学期4月份联考化学试题.(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)四川省成都市第七中学2021-2022学年高一下学期期末考试化学试题江苏省响水中学2022-2023学年高三上学期开学测试化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题江苏省南京师范大学附属中学秦淮科技高中2021-2022学年高一下学期期末测试化学试题江苏省南京市六校联合体2022-2023学年高一下学期期末联合调研化学试题(已下线)第1讲 钠及其重要化合物江苏省扬州中学2023-2024学年高三上学期10月月考化学试题江苏省马坝高级中学2023-2024学年高三上学期10月学情调研测试化学试题河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题
8 . 已知钠在较高温度下能与二氧化碳反应,该反应后含碳产物是什么?不同的同学提出如下五种猜想:甲认为是C,乙认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO3,为确定该反应的含碳产物,五位同学用下图装置进行实验探究。
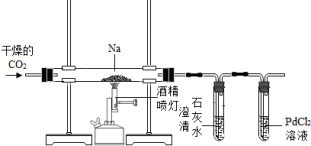
已知:CO能与PdCl2产生黑色的Pd,可利用该反应检测CO是否存在。请回答下列问题:
(1)不用实验就可知道戊的猜想是错误的,判断理由是_______ 。
(2)实验室制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应选用的装置是_______ (选填如图中“I”、“II”或“III”)。
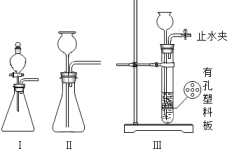
(3)实验时,在加热硬质玻璃管之前需要进行的实验操作是_______ 。
(4)澄清石灰水中发生反应的离子方程式为_______ 。
(5)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直管中的固体全部溶解于水。取所得溶液并加入澄清石灰水,观察到浑浊现象。据此可知,该反应后的含碳产物是_______ 。

已知:CO能与PdCl2产生黑色的Pd,可利用该反应检测CO是否存在。请回答下列问题:
(1)不用实验就可知道戊的猜想是错误的,判断理由是
(2)实验室制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应选用的装置是

(3)实验时,在加热硬质玻璃管之前需要进行的实验操作是
(4)澄清石灰水中发生反应的离子方程式为
(5)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直管中的固体全部溶解于水。取所得溶液并加入澄清石灰水,观察到浑浊现象。据此可知,该反应后的含碳产物是
您最近一年使用:0次
解题方法
9 . 化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性良好)。请回答:
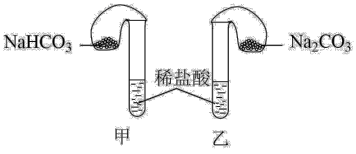
(1)各组反应开始时,____________ (甲、乙)装置中的气球体积先变大,该装置中反应的化学反应方程式是_____________ 。
(2)当试管中不再有气体生成时,三组实验出现不同现象,试分析原因并填写下表的空格。

(1)各组反应开始时,
(2)当试管中不再有气体生成时,三组实验出现不同现象,试分析原因并填写下表的空格。
| 试剂用量 | 实验现象 (气球体积变化) | 分析原因 | |
| 第①组 | 0.42gNaHCO3 0.53gNa2CO3 3mL 4mol·L-1盐酸 | 甲中气球与乙中气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)= n(Na2CO3) V甲(CO2)= V乙(CO2) |
| 第②组 | 0.3gNaHCO3 0.3gNa2CO3 3mL 4 mol·L-1盐酸 | 甲中气球比乙中气球的体积大 | A: |
| 第③组 | 0.6gNaHCO3 0.6gNa2CO3 3mL 2 mol·L-1盐酸 | 甲中气球比乙中气球的体积大 | B: |
| 片刻后,乙中气球又缩小,甲中气球的体积基本不变 | (用化学方程式表示) C: |
您最近一年使用:0次



