1 . 回答下列问题
(1)碳酸钠是白色粉末,俗称________ ,常温下溶解度________ (填大于、小于或等于)碳酸氢钠,水溶液呈________ (填酸性、碱性或中性);电离方程式为________ 。
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:________ 。
②受热分解:________ 。
③与 反应:
反应:________ 。
(3)焰色试验:若要观察钾元素的焰色,需要透过________ 观察火焰颜色。
(1)碳酸钠是白色粉末,俗称
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:
②受热分解:
③与
 反应:
反应:(3)焰色试验:若要观察钾元素的焰色,需要透过
您最近一年使用:0次
2 . 海洋是一个巨大的化学资源宝库,其中钠元素是海洋中含量较高的元素。
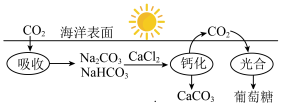
(1)已知在太阳光作用下,绿色植物体内的叶绿素能将水、CO2转化为葡萄糖。海水吸收CO2并进行碳循环的原理示意图如下:
(2)某同学欲用碳酸钠晶体(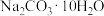 )配制220mL1mol/L的Na2CO3溶液。
)配制220mL1mol/L的Na2CO3溶液。
①所需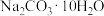 的质量为
的质量为___________ g。
②实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有___________ 。
③配制溶液时正确的操作顺序是:_________ (填字母,下同)
计算→称量→___________→___________→___________→___________→___________→装瓶贴标签。
a.转移 b.定容 c.摇匀 d.洗涤 e.溶解
④下列实验操作会使配制溶液浓度偏高的是___________ 。
A.容量瓶清洗后,未经过干燥处理
B.定容时,俯视刻度线
C.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水至刻度线
D.所用碳酸钠晶体失去结晶水
(1)已知在太阳光作用下,绿色植物体内的叶绿素能将水、CO2转化为葡萄糖。海水吸收CO2并进行碳循环的原理示意图如下:
| A.CO2是碱性氧化物 |
| B.等质量的NaHCO3和Na2CO3分别与足量的盐酸反应,前者产生的二氧化碳气体较多 |
C.碳酸氢钠的电离方程式为 |
| D.该循环过程中未涉及氧化还原反应 |
(2)某同学欲用碳酸钠晶体(
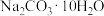 )配制220mL1mol/L的Na2CO3溶液。
)配制220mL1mol/L的Na2CO3溶液。①所需
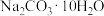 的质量为
的质量为②实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有
③配制溶液时正确的操作顺序是:
计算→称量→___________→___________→___________→___________→___________→装瓶贴标签。
a.转移 b.定容 c.摇匀 d.洗涤 e.溶解
④下列实验操作会使配制溶液浓度偏高的是
A.容量瓶清洗后,未经过干燥处理
B.定容时,俯视刻度线
C.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水至刻度线
D.所用碳酸钠晶体失去结晶水
您最近一年使用:0次
2024-01-25更新
|
59次组卷
|
2卷引用:陕西省汉中市汉台区2023-2024学年高一上学期1月期末化学试题
名校
解题方法
3 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
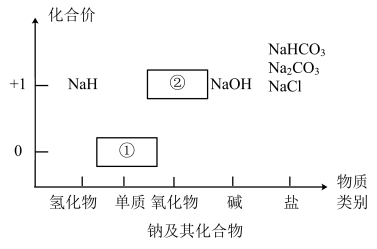
(1)物质①与水反应的离子方程式为_________ ,所以通常将其保存在_________ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目_________ 。
(3)从核心元素价态的视角看,NaH中H元素的化合价为_________ ,从H元素的价态分析,NaH常用作_________ (填“氧化剂”或“还原剂”)。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
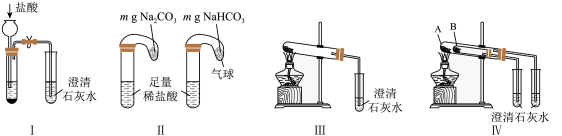
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是_________ (填装置序号)。
②图Ⅲ、Ⅳ中_________ 能更好说明二者的稳定性(填装置序号),写出Ⅳ中使澄清石灰水变浑浊的离子方程式_________ 。

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目
(3)从核心元素价态的视角看,NaH中H元素的化合价为
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②图Ⅲ、Ⅳ中
您最近一年使用:0次



