名校
1 . 某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
(1)KClO4中氯元素的化合价是___________ 。
(2)Fe2O3可处理产生的Na,反应为6Na+Fe2O3=3Na2O+ 2Fe,反应中Na做___________ (填“还原剂”或“氧化剂”)。
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是___________ 。
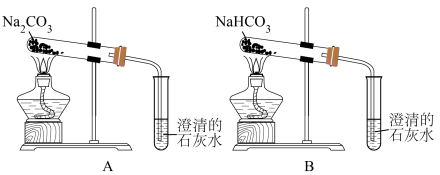
(4)按如图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是___________ 。
(1)KClO4中氯元素的化合价是
(2)Fe2O3可处理产生的Na,反应为6Na+Fe2O3=3Na2O+ 2Fe,反应中Na做
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是
(4)按如图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是

您最近一年使用:0次
名校
解题方法
2 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。图是钠的价类二维图:

请回答以下问题:
(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因_______ (用化学方程式表示,写一个即可)
(2)写出 的电离方程式
的电离方程式_______ ; 溶液常因温度过高而分解含有少量
溶液常因温度过高而分解含有少量 ,除去杂质
,除去杂质 的方法为
的方法为_______ (用离子方程式表示)。
(3)向300 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2(忽略溶液体积的变化),充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加1 mol·L-1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:

①AB段发生反应的离子方程式_______ 。
②B点时,反应所得溶液中溶质的物质的量是_______ 。
(4)实验室可以用稀盐酸鉴别Na2CO3和NaHCO3,除了这种方法,请你再举出一例鉴别Na2CO3和NaHCO3溶液的方法:_______ 。

请回答以下问题:
(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因
(2)写出
 的电离方程式
的电离方程式 溶液常因温度过高而分解含有少量
溶液常因温度过高而分解含有少量 ,除去杂质
,除去杂质 的方法为
的方法为(3)向300 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2(忽略溶液体积的变化),充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加1 mol·L-1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:

①AB段发生反应的离子方程式
②B点时,反应所得溶液中溶质的物质的量是
(4)实验室可以用稀盐酸鉴别Na2CO3和NaHCO3,除了这种方法,请你再举出一例鉴别Na2CO3和NaHCO3溶液的方法:
您最近一年使用:0次
名校
3 . 除去下列物质中所混有少量的杂质,指明应加入的试剂,写出有关的离子反应方程式。
(1)Mg粉(Al粉):试剂_______ 离子方程式 ____________________________________ ;
(2)NaHCO3溶液(Na2CO3):试剂________ 离子方程式 ___________________________ 。
(1)Mg粉(Al粉):试剂
(2)NaHCO3溶液(Na2CO3):试剂
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)若金属钠等活泼金属着火时,应该用_______________ 来灭火。将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是________ 。
a.有气体生成 b.钠熔化成小球并在液面上游动
c.烧杯底部有银白色的金属钙生成 d.溶液变浑浊
(2)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3性质的说法中,正确的是______________ 。
a.常温下,Na2CO3在水中的溶解度比NaHCO3小
b.相同质量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2前者多
c.可用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
d. NaHCO3溶液中混有少量Na2CO3杂质可通入足量CO2除杂
(3)过氧化钠、过氧化镁都是重要的过氧化物。过氧化镁不溶于水,但易溶于稀酸,广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式:_____________ 。
(4)某无色稀溶液X中,可能含有Al3+、Cl-、Fe3+、Mg2+、NH4+中的某几种,向其中加入NaOH溶液时产生沉淀的物质的量(n)与加入NaOH溶液体积(V)的关系如下图所示。

则X中一定含有的阳离子是_________ ,bc段反应的离子方程式为________ 。
(5)在1L某酸性溶液中离子浓度的分析结果如下表
向该溶液中逐滴加入0.5 mol•L-1NaOH溶液至沉淀恰好不再溶解时,消耗NaOH体积为_____ mL。
(1)若金属钠等活泼金属着火时,应该用
a.有气体生成 b.钠熔化成小球并在液面上游动
c.烧杯底部有银白色的金属钙生成 d.溶液变浑浊
(2)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3性质的说法中,正确的是
a.常温下,Na2CO3在水中的溶解度比NaHCO3小
b.相同质量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2前者多
c.可用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
d. NaHCO3溶液中混有少量Na2CO3杂质可通入足量CO2除杂
(3)过氧化钠、过氧化镁都是重要的过氧化物。过氧化镁不溶于水,但易溶于稀酸,广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式:
(4)某无色稀溶液X中,可能含有Al3+、Cl-、Fe3+、Mg2+、NH4+中的某几种,向其中加入NaOH溶液时产生沉淀的物质的量(n)与加入NaOH溶液体积(V)的关系如下图所示。

则X中一定含有的阳离子是
(5)在1L某酸性溶液中离子浓度的分析结果如下表
| 离子 | Mg2+ | Al3+ | SO42− | Cl− |
| c/(mol/L) | 0.5×10−2 | 1.0×10−2 | 0.5×10−2 | 3.0×10−2 |
您最近一年使用:0次
2018-12-07更新
|
166次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题
名校
解题方法
5 . 碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式是___________ ,俗称____________ ,其水溶液显_______ 性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为_____________ 。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者_________ 后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为__________________________ 。
(1)碳酸氢钠的化学式是
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为
您最近一年使用:0次
2016-12-08更新
|
778次组卷
|
7卷引用:宁夏青铜峡市高级中学2020-2021学年高一下学期开学考试化学试题
宁夏青铜峡市高级中学2020-2021学年高一下学期开学考试化学试题(已下线)2011-2012学年黑龙江省绥棱县第一中学高一上学期期末考试化学试卷(已下线)2011-2012学年北京市四中高一上学期期末考试化学试卷2015-2016学年湖北省老河口一中高一上学期期末考试化学试卷2015-2016学年河北省保定市望都中学高一上学期期末化学试卷北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题甘肃省镇原县第二中学2020-2021学年高一上学期期末考试化学试题



