1 . 某小组同学对比Na2CO3和NaHCO3的性质,进行了如下实验。
(1)向相同体积、相同浓度的Na2CO3和NaHCO3溶液中分别滴加0.1mol•L-1的盐酸,溶液pH变化如下。
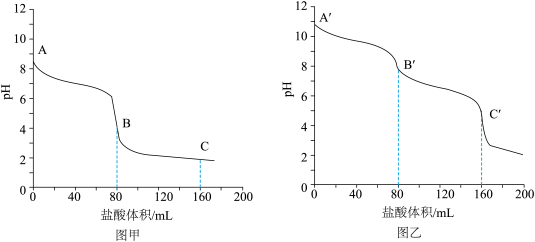
①图____ (填“甲”或“乙”)是NaHCO3的滴定曲线。
②A´—B´发生反应的离子方程式为___________ 。
③下列说法正确的是_________ (填序号)。
a.Na2CO3和NaHCO3溶液中加入饱和石灰水,均有沉淀生成
b.A和A´对应溶液中:c(Na+)+c(H+)=2c( )+c(
)+c( )+c(OH-)
)+c(OH-)
c.B和B´对应溶液中:水的电离程度前者大
d.C和C´对应溶液中:NaCl的物质的量相等
(2)向1mol•L-1的Na2CO3和NaHCO3溶液中分别滴加少量FeCl2溶液,均产生白色沉淀。
查阅资料:i.1mol•L-1的NaHCO3溶液中,c( )=1×10-2mol•L-1,c(OH-)=2×10-6mol•L-1
)=1×10-2mol•L-1,c(OH-)=2×10-6mol•L-1
ii.25℃时,Ksp(FeCO3)=3.2×10-11,Ksp[Fe(OH)2]=5.0×10-17
通过计算判断NaHCO3与FeCl2反应产生的沉淀是FeCO3,还是Fe(OH)2?_______ (要求有计算过程)。
(1)向相同体积、相同浓度的Na2CO3和NaHCO3溶液中分别滴加0.1mol•L-1的盐酸,溶液pH变化如下。

①图
②A´—B´发生反应的离子方程式为
③下列说法正确的是
a.Na2CO3和NaHCO3溶液中加入饱和石灰水,均有沉淀生成
b.A和A´对应溶液中:c(Na+)+c(H+)=2c(
 )+c(
)+c( )+c(OH-)
)+c(OH-)c.B和B´对应溶液中:水的电离程度前者大
d.C和C´对应溶液中:NaCl的物质的量相等
(2)向1mol•L-1的Na2CO3和NaHCO3溶液中分别滴加少量FeCl2溶液,均产生白色沉淀。
查阅资料:i.1mol•L-1的NaHCO3溶液中,c(
 )=1×10-2mol•L-1,c(OH-)=2×10-6mol•L-1
)=1×10-2mol•L-1,c(OH-)=2×10-6mol•L-1ii.25℃时,Ksp(FeCO3)=3.2×10-11,Ksp[Fe(OH)2]=5.0×10-17
通过计算判断NaHCO3与FeCl2反应产生的沉淀是FeCO3,还是Fe(OH)2?
您最近一年使用:0次
2 . 生活离不开化学。家庭厨卫和药品中有许多中学化学常见的物质,括号内为商品的主要成分。
①食盐(NaCl) ②料酒(乙醇) ③白醋(乙酸) ④碱面( ) ⑤发酵粉(
) ⑤发酵粉( 和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl) ⑧雪碧(二氧化碳的水溶液)
和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl) ⑧雪碧(二氧化碳的水溶液)
回答下列问题:
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是___________ 。
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填正确答案标号)。
(3)写出二氧化碳的结构式___________ 。
(4)除去 溶液中混有的少量
溶液中混有的少量 杂质,应采取的方法是
杂质,应采取的方法是___________ ,
(5)相同条件下,等质量的 与
与 分别与足量的盐酸反应产生气体的体积比为
分别与足量的盐酸反应产生气体的体积比为___________ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________
①食盐(NaCl) ②料酒(乙醇) ③白醋(乙酸) ④碱面(
 ) ⑤发酵粉(
) ⑤发酵粉( 和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl) ⑧雪碧(二氧化碳的水溶液)
和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl) ⑧雪碧(二氧化碳的水溶液)回答下列问题:
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填正确答案标号)。
| A.两种物质都是非电解质 | B.两种物质都是电解质 |
| C.两种物质都是含碳化合物 | D.两种物质都是共价化合物 |
(4)除去
 溶液中混有的少量
溶液中混有的少量 杂质,应采取的方法是
杂质,应采取的方法是(5)相同条件下,等质量的
 与
与 分别与足量的盐酸反应产生气体的体积比为
分别与足量的盐酸反应产生气体的体积比为(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
名校
3 .  和
和 在厨房中很常见,回答下列问题:
在厨房中很常见,回答下列问题:
(1) 从其组成的阴离子来看,属于
从其组成的阴离子来看,属于_______ , 的俗称为
的俗称为_______ ,等物质的量的 和
和 固体中所含的离子总数之比为
固体中所含的离子总数之比为_______ 。
(2)厨房去油污选用 溶液而不选用
溶液而不选用 溶液的原因为
溶液的原因为_______ 。
(3)比较 和
和 的热稳定性的示意图如图,一段时间后,观察到烧杯Ⅱ中的溶液变浑浊了,而烧杯Ⅰ中的溶液未变浑浊。
的热稳定性的示意图如图,一段时间后,观察到烧杯Ⅱ中的溶液变浑浊了,而烧杯Ⅰ中的溶液未变浑浊。
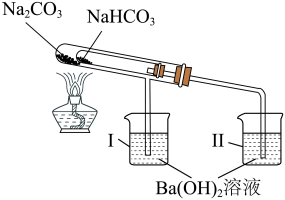
①热稳定性:
_______ (填“>”、“<”或“=”) 。
。
②烧杯Ⅱ中的溶液变浑浊,反应后的产物为_______ (填化学式)。
(4)碳酸氢钠受热分解时转化率与熔烧时间的关系如图。
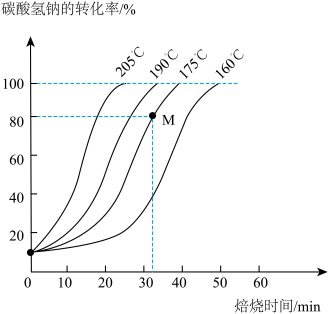
①碳酸氢钠受热分解的化学方程式为_______ 。
②若起始时投入的碳酸氢钠的质量为16.8g(假设不含其他杂质),则M点时产生的二氧化碳气体的体积为_______ L。(气体已换算成标准状况下,转化率 )
)
 和
和 在厨房中很常见,回答下列问题:
在厨房中很常见,回答下列问题:(1)
 从其组成的阴离子来看,属于
从其组成的阴离子来看,属于 的俗称为
的俗称为 和
和 固体中所含的离子总数之比为
固体中所含的离子总数之比为(2)厨房去油污选用
 溶液而不选用
溶液而不选用 溶液的原因为
溶液的原因为(3)比较
 和
和 的热稳定性的示意图如图,一段时间后,观察到烧杯Ⅱ中的溶液变浑浊了,而烧杯Ⅰ中的溶液未变浑浊。
的热稳定性的示意图如图,一段时间后,观察到烧杯Ⅱ中的溶液变浑浊了,而烧杯Ⅰ中的溶液未变浑浊。
①热稳定性:

 。
。②烧杯Ⅱ中的溶液变浑浊,反应后的产物为
(4)碳酸氢钠受热分解时转化率与熔烧时间的关系如图。

①碳酸氢钠受热分解的化学方程式为
②若起始时投入的碳酸氢钠的质量为16.8g(假设不含其他杂质),则M点时产生的二氧化碳气体的体积为
 )
)
您最近一年使用:0次
解题方法
4 . 实验室中的氢氢化钠溶液在空气中放置,因密封不好会变质,有关反应的离子方程式为____ ;为了检测一瓶氢氧化钠溶液是否已变质,可取少量该溶液向其中加入____ ,若有_____ 现象发生,则说明烧碱溶液已经变质。
您最近一年使用:0次
名校
解题方法
5 . (1)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再产生CO2气体为止,在此过程中,溶液中的碳酸氢根离子浓度的变化是___ 。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为___ 。
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有___ 种。若固体混合物A的质量m(A)为定值,生成气体的量为定值,则A的可能组成是(填写化学式):___ 、___ ;___ 、___ 。(可以不填满)
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是___ mol。
A.先变大后变小 B.先变小后变大 C.一直变小 D.保持不变
(2)有含0.2molNa2CO3和含0.3molHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2之比为
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成可能有
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A的总物质的量是
您最近一年使用:0次



