1 . 下列有关实验操作或说法正确的是
A.配制125 mL 1.0 mol⋅L 的氯化钠溶液需要用到130 mL的容量瓶 的氯化钠溶液需要用到130 mL的容量瓶 |
| B.探究碳酸钠和碳酸氢钠热稳定性实验应分别加入碳酸钠与碳酸氢钠 |
| C.制备氢氧化铁胶体的实验中应将氯化铁溶液加入到温水中,继续煮沸至红褐色即可 |
| D.干燥的氯气使湿润的鲜花变色,干燥的氯气具有漂白性 |
您最近一年使用:0次
解题方法
2 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式________ 。
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是__________ 。
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na________ Mg(填“>”“<"或“=”)。
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是__________ 。
(5)其中产物_______ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式__________ 。
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是_________ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因_____ (填“Na2CO3”或*NaHCO3")消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加______ (填“Na2CO3"或“NaHCO3"),继续揉面,上锅蒸后也能蒸出松软的馒头,用化学方程式表示其产气原理_____________ 。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是
(5)其中产物
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加
您最近一年使用:0次
3 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。
I.如图为联合制碱法的主要过程(部分物质已略去):
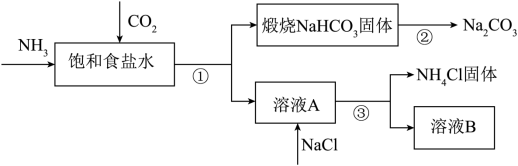
(1)①~③的涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)煅烧NaHCO3固体的化学方程式是___________ 。
(3)上述联合制碱法流程可以循环使用的中一种物质是___________ (填化学式)。
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。
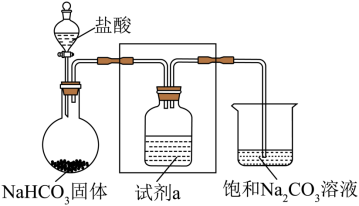
(4)方框中为洗气装置,请将该装置图补充完整___________ 。
(5)试剂a为饱和NaHCO3溶液,其作用是___________ 。
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因___________ 。
(7)下列选项中哪种物质可以鉴别浓度相同的 和
和 ___________。
___________。
I.如图为联合制碱法的主要过程(部分物质已略去):

(1)①~③的涉及的操作方法中,包含过滤的是
(2)煅烧NaHCO3固体的化学方程式是
(3)上述联合制碱法流程可以循环使用的中一种物质是
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。

(4)方框中为洗气装置,请将该装置图补充完整
(5)试剂a为饱和NaHCO3溶液,其作用是
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
(7)下列选项中哪种物质可以鉴别浓度相同的
 和
和 ___________。
___________。| A.澄清石灰水 | B.氢氧化钠溶液 | C.稀盐酸 | D. 溶液 溶液 |
您最近一年使用:0次
解题方法
4 . 下列有关说法正确的是
| A.为了除去Na2CO3溶液中的NaHCO3,可滴加适量的稀盐酸 |
| B.为了除去NaHCO3固体中的Na2CO3,可通过加热除去 |
C.热稳定性: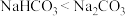 |
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有CO |
您最近一年使用:0次
解题方法
5 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.CO2(HCl):将混合气体通过足量的饱和碳酸钠溶液 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入过量Ca(OH)2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过浓硫酸 |
您最近一年使用:0次
2024-04-07更新
|
70次组卷
|
2卷引用:四川省雅安天立学校腾飞高中2023-2024学年高一上学期11月月考化学试题
6 . 下列实验能够达到相应目的的是
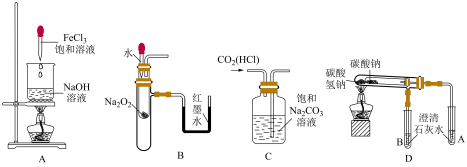
| A.制备氢氧化铁胶体 | B.验证 和水反应是否放热 和水反应是否放热 |
C.除去 中的HCl 中的HCl | D.装置可用于比较碳酸钠和碳酸氢钠的热稳定性 |
您最近一年使用:0次
2024-04-02更新
|
135次组卷
|
2卷引用:广东省深圳市人大附中深圳学校2023-2024学年高一上学期期中考试化学试题
7 . 鉴别K2CO3和NaHCO3两种白色固体的下列方案中,不可行 的是
| A.分别配成溶液,进行焰色试验,观察火焰的颜色 |
| B.分别加热,将可能产生的气体通入澄清石灰水,观察有无浑浊产生 |
| C.分别配成稀溶液,加入澄清石灰水,观察有无白色沉淀产生 |
| D.分别配成浓溶液,滴入稀盐酸,观察有无气泡产生 |
您最近一年使用:0次
2024-03-20更新
|
47次组卷
|
2卷引用:北京市第一五九中学2023-2024学年高一上学期期中考试化学试题
8 . 下列实验操作、现象、结论(或解释)均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将一小块金属钠加入至 | 溶液蓝色褪去,有红色固体出现 | 钠比铜还原性强,钠置换出铜 |
B | 用洁净铂丝蘸取溶液在酒精灯火焰上灼烧并观察 | 火焰呈黄色 | 溶液中的金属元素只有钠元素 |
C | 分别向盛有 | 2支试管中均出现白色沉淀 | 澄清石灰水不适用于鉴别 |
D | 向新制氯水中滴加紫色石蕊试液 | 溶液立即褪色 | 新制氯水具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 金属钠及其化合物在人类社会发展进程中起着重要的作用。请回答:
(1)将一小块金属钠投入盛有水的烧杯中:
①发生反应的离子方程式是_______ 。
②可观察到的实验现象是_______ (填字母)。
a.钠浮于水面 b.钠熔成小球
c.嘶嘶作响 d.小球四处游动
③钠与水反应的现象和钠的下列性质无关的是_______ (填字母)。
a.钠的熔点较低 b.钠的密度小于水
c.钠的硬度较小 d.钠的还原性强
(2)钠在加热条件下与氧气反应,所得产物放置在空气中可能发生反应的化学方程式有_______ 、_______ 。
(3)实验室利用图所示装置进行Na2CO3和NaHCO3热稳定性对比实验:

①加热一段时间后,两试管中石灰水的变化是_______ (填字母)。
a.均变浑浊
b.试管1澄清,试管2变浑浊
c.试管1变浑浊,试管2澄清
②该实验说明二者中稳定性强的物质是_______ (填化学式),另一种物质受热分解的化学方程式是_______ 。
③碳酸氢钠常被用于治疗胃酸(盐酸)过多,反应的离子方程式为:_______ 。
(1)将一小块金属钠投入盛有水的烧杯中:
①发生反应的离子方程式是
②可观察到的实验现象是
a.钠浮于水面 b.钠熔成小球
c.嘶嘶作响 d.小球四处游动
③钠与水反应的现象和钠的下列性质无关的是
a.钠的熔点较低 b.钠的密度小于水
c.钠的硬度较小 d.钠的还原性强
(2)钠在加热条件下与氧气反应,所得产物放置在空气中可能发生反应的化学方程式有
(3)实验室利用图所示装置进行Na2CO3和NaHCO3热稳定性对比实验:

①加热一段时间后,两试管中石灰水的变化是
a.均变浑浊
b.试管1澄清,试管2变浑浊
c.试管1变浑浊,试管2澄清
②该实验说明二者中稳定性强的物质是
③碳酸氢钠常被用于治疗胃酸(盐酸)过多,反应的离子方程式为:
您最近一年使用:0次
10 . 某小组同学进行Na2CO3和NaHCO3性质的探究,实验如下(夹持装置已略去,气密性已检验)。
【实验一】
(1)实验I,能够证明Na2CO3的热稳定性强于NaHCO3的证据是___________ 。
(2)实验II,试剂a为___________ 。
(3)实验II,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:___________ 。
【实验二】
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱。
(4)实验I中,溶解时吸收热量的物质是___________ (写化学式)。
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为___________ ,(OH-未参与该反应的实验证据是___________ 。
(6)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有___________ 。
【实验一】
| 实验I | 实验II |
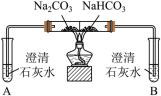 |  |
(2)实验II,试剂a为
(3)实验II,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:
【实验二】
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱。
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化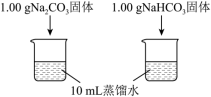 |  |
| 实验操作 | 实验数据 | |
| 实验II | 测量下述实验过程的pH变化 | ②和③中均产生白色沉淀。 各烧杯中pH变化如下图所示 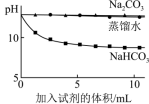 |
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(6)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有
您最近一年使用:0次

 溶液中
溶液中

