名校
1 . 某校学习小组的同学拟用工业废铁屑(主要成分为Fe,还含有少量FeS、Fe3P等)制备FeSO4·7H2O,并探究FeSO4·7H2O高温分解的产物。

I.制备实验步骤如下:
①称取一定量的废铁屑,用热的碳酸钠溶液浸泡,再用蒸馏水洗涤。
②将处理后的废铁屑放入锥形瓶中,加入适量3mol·L-1的硫酸,连接好装置(如图)后水浴加热至反应完全。
③依据现象停止加热,趁热过滤,向滤液中补加少量硫酸。
④将滤液冷却、结晶、过滤、洗涤。
回答下列问题
(1)步骤②中需控制硫酸的用量,使铁粉过量,其目的是_____________________ 。
(2)装置C的作用是__________________________ 。
(3)步骤④中洗涤时所用的洗涤剂最好是______ (填标号)。
A.稀硝酸 B.无水乙醇 C.苯
(4)测定产品的纯度:
称取mg产品,放入锥形瓶中,用经煮沸过且冷却的蒸馏水和稀硫酸溶解,然后用cmol·L-1的KMnO4标准溶液滴定,消耗VmLKMnO4标准溶液。
蒸馏水煮沸的原因:______________ ;产品的纯度为_________________ (列出计算表达式即可)
Ⅱ.探究FeSO4·7H2O高温分解的产物的实验装置及步骤如下,请完成相关填空:

(9)依据实验现象及产物,写出FeSO4·7H2O分解的化学方程式:_________________ 。

I.制备实验步骤如下:
①称取一定量的废铁屑,用热的碳酸钠溶液浸泡,再用蒸馏水洗涤。
②将处理后的废铁屑放入锥形瓶中,加入适量3mol·L-1的硫酸,连接好装置(如图)后水浴加热至反应完全。
③依据现象停止加热,趁热过滤,向滤液中补加少量硫酸。
④将滤液冷却、结晶、过滤、洗涤。
回答下列问题
(1)步骤②中需控制硫酸的用量,使铁粉过量,其目的是
(2)装置C的作用是
(3)步骤④中洗涤时所用的洗涤剂最好是
A.稀硝酸 B.无水乙醇 C.苯
(4)测定产品的纯度:
称取mg产品,放入锥形瓶中,用经煮沸过且冷却的蒸馏水和稀硫酸溶解,然后用cmol·L-1的KMnO4标准溶液滴定,消耗VmLKMnO4标准溶液。
蒸馏水煮沸的原因:
Ⅱ.探究FeSO4·7H2O高温分解的产物的实验装置及步骤如下,请完成相关填空:

| 操作步骤 | 实验现象 | 解释原因 |
| 组装好仪器,先充入氮气,再加热管式炉至700℃一段时间 | 试管E中的白色固体变蓝 | 分解得到的产物中含水蒸气 |
| 气体产物经过试管B时 | 品红溶液褪色 | (5)产物中含有 |
| 气体产物经过试管C时 | 试管C中出现白色沉淀 | (6)C中反应的化学方程式为 |
| 将瓷舟中反应后的固体溶于足量稀硫酸,再滴入几滴KSCN溶液 | (7) | (8)溶液中含有 |
(9)依据实验现象及产物,写出FeSO4·7H2O分解的化学方程式:
您最近一年使用:0次
名校
2 . 下列说法正确的有个
①将铁屑放入稀HNO3中,证明Fe比H2活泼
②FeCl3腐蚀Cu 制印刷电路板是由于铁比铜的金属性强
③检验溶液中是否含有Fe2+,取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN 溶液,观察实验现象
④磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++NO3-==3Fe3++NO↑+3H2O
⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中,制备Fe(OH)3胶体
⑥氢氧化铁与HI溶液反应的离子方程式为: Fe(OH)3+3H+==Fe3++3H2O
⑦铁与水蒸气在高温下的反应产物为Fe2O3 和H2
⑧1mol FeI2与足量氯气反应时转移的电子数为3NA
⑨检验Fe (NO3)2晶体是否氧化变质的方法是将Fe (NO3) 2样品溶于稀H2SO4后,滴加KSCN 溶液,观察溶液是否变红
⑩图示装置能较长时间观察到Fe (OH) 2白色沉淀
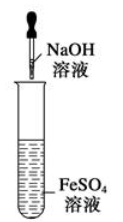
①将铁屑放入稀HNO3中,证明Fe比H2活泼
②FeCl3腐蚀Cu 制印刷电路板是由于铁比铜的金属性强
③检验溶液中是否含有Fe2+,取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN 溶液,观察实验现象
④磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++NO3-==3Fe3++NO↑+3H2O
⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中,制备Fe(OH)3胶体
⑥氢氧化铁与HI溶液反应的离子方程式为: Fe(OH)3+3H+==Fe3++3H2O
⑦铁与水蒸气在高温下的反应产物为Fe2O3 和H2
⑧1mol FeI2与足量氯气反应时转移的电子数为3NA
⑨检验Fe (NO3)2晶体是否氧化变质的方法是将Fe (NO3) 2样品溶于稀H2SO4后,滴加KSCN 溶液,观察溶液是否变红
⑩图示装置能较长时间观察到Fe (OH) 2白色沉淀

| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
解题方法
3 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究化学反应是否可逆 | 向0.5mL0.1mol·L-1KI溶液中滴加1-2滴0.1mol·L-1的Fe(SO4)3溶液,充分反应后,滴入1-2滴0.1mol·L-1的AgNO3溶液,生成黄色沉淀 |
| B | 比较Cu(OH)2、Mg(OH)2的Ksp的相对大小 | 向1mL0.1mol·L-1MgSO4溶液中加入1mL0.3mol·L-1KOH溶液,再滴加5-6滴0.1mol·L-1的CuSO4溶液,观察现象 |
| C | 比较H2O2和Fe3+的氧化性强弱 | 将硫酸酸化过的H2O2滴入Fe(NO3)2的溶液中,溶液变黄 |
| D | 探究浓度对盐类水解平衡的影响 | 向滴有酚酞的碳酸钠溶液中滴加氯化钡溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-10更新
|
182次组卷
|
2卷引用:河南省南阳地区2020-2021学年高二下学期阶段检测考试化学试题



