1 . 探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 往 溶液中加入 溶液中加入 片 片 | 短时间内无明显现象 |  的氧化能力比 的氧化能力比 弱 弱 |
| B | 往 溶液中滴加 溶液中滴加 溶液,再加入少量 溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加 溶液 溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有 价铁 价铁 |
| D | 向沸水中逐滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 再聚集成 再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-11更新
|
10022次组卷
|
19卷引用:2023年1月浙江省普通高校招生选考化学试题
2023年1月浙江省普通高校招生选考化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题11-16)浙江省平阳县万全综合高级中学2022-2023学年高二下学期第一次月考化学试题 (已下线)2023年高考化学真题完全解读(浙江1月)湖南省长沙市雅礼中学2022-2023学年高三下学期4月份第八次月考化学试题湖南省长沙市雅礼中学2022-2023学年高三下学期4月份第八次月考化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题14 化学实验方案的设计与评价(已下线)【知识图鉴】单元讲练测必修第一册第三单元03巩固练(已下线)第6讲 铁及其重要化合物(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题突破卷03?金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型03 离子方程式正误判断 离子共存、检验和推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
2 . 黄色固体X,可能含有漂白粉、 、
、 、
、 、
、 之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
 、
、 、
、 、
、 之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是A.X中含 ,可能含有 ,可能含有 |
B.X中含有漂白粉和 |
C.X中含有 ,Y中含有 ,Y中含有 |
D.用 酸化溶液Z,若有黄绿色气体放出,说明X中含有 酸化溶液Z,若有黄绿色气体放出,说明X中含有 |
您最近一年使用:0次
2020-07-11更新
|
4919次组卷
|
23卷引用:2020年浙江省高考化学试卷(7月选考)
2020年浙江省高考化学试卷(7月选考)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题04.离子反应-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)江西省高安中学2020-2021学年高二上学期第一次段考化学(A)试题广东省深圳外国语学校2021届高三第二次月考化学试题(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)重点7 探究型实验综合题-2021年高考化学专练【热点·重点·难点】(已下线)课时08 离子检验与推断-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 氯及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考点03 离子反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2023年高考化学一轮复习考点微专题(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 氯及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)山东省威海乳山市银滩高级中学2022-2023学年高三9月月考化学试题第一章 化学物质及其变化 第3讲 离子反应的应用(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第3讲 铁盐及其亚铁盐(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
真题
解题方法
3 . 食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:氧化性: >Fe3+>I2;还原性:
>Fe3+>I2;还原性: >I﹣,3I2+6OH﹣=
>I﹣,3I2+6OH﹣= +5I﹣+3H2O;KI+I2⇌KI3
+5I﹣+3H2O;KI+I2⇌KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是____ (用化学式表示);CCl4中显紫红色的物质是_____ (用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为_____ 、_____ 。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下KI与氧气反应的化学方程式:_____ 。将I2溶于KI溶液,在低温条件下,可制得KI3•H2O。该物质作为食盐加碘剂是否合适?_____ (填“是”或“否”),并说明理由_______ 。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是_____ 。
A.Na2S2O3B.AlCl3C.Na2CO3D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂。请设计实验方案,检验该加碘盐中的Fe2+。_____ 。
 >Fe3+>I2;还原性:
>Fe3+>I2;还原性: >I﹣,3I2+6OH﹣=
>I﹣,3I2+6OH﹣= +5I﹣+3H2O;KI+I2⇌KI3
+5I﹣+3H2O;KI+I2⇌KI3(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是
②第二份试液中加入足量KI固体后,反应的离子方程式为
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下KI与氧气反应的化学方程式:
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是
A.Na2S2O3B.AlCl3C.Na2CO3D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂。请设计实验方案,检验该加碘盐中的Fe2+。
您最近一年使用:0次
2019-01-30更新
|
1500次组卷
|
5卷引用:2011年普通高等学校招生全国统一考试化学卷(浙江)
2011年普通高等学校招生全国统一考试化学卷(浙江)(已下线)2014年化学高考总复习课时演练 11-4化学实验方案设计与评价练习卷(已下线)2014年高考化学苏教版总复习 1-4 氧化还原反应练习卷(已下线)2015届河南省顶级名校高三入学定位考试化学试卷2017届河北省邯郸市大名一中高三上学期第一次月考化学试卷
真题
名校
4 . 称取4.00g氧化铜和氧化铁固体混合物,加入50.0mL2.00mol·L-1的硫酸充分溶解,往所得溶液中加入5.60g铁粉,充分反应后,得固体的质量为3.04g。请计算:
(1)加入铁粉充分反应后,溶液中溶质的物质的量_________________ 。
(2)固体混合物中氧化铜的质量_________________ 。
(1)加入铁粉充分反应后,溶液中溶质的物质的量
(2)固体混合物中氧化铜的质量
您最近一年使用:0次
2018-11-09更新
|
2375次组卷
|
11卷引用:浙江省普通高校招生选考科目2018年4月考试化学试题
浙江省普通高校招生选考科目2018年4月考试化学试题浙江省台州市书生中学2018-2019学年高二下学期第一次月考化学试题浙江省金华市武义第三中学2019-2020学年高二上学期期中考试化学试题(已下线)【浙江新东方】在线化学64高一下(已下线)【浙江新东方】高中化学20210513-030【2021】【高一下】(已下线)专题18.化学计算-十年(2012-2021)高考化学真题分项汇编(浙江专用)浙江省杭州市西湖高级中学2021-2022学年高一下学期期中考试化学试题专题3.1 金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 高考帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 高考帮(已下线)考点02 化学用语和常用化学计量-备战2022年高考化学学霸纠错(全国通用)
5 . 为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。

已知:3Fe(s)+4H2O(g)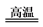 Fe3O4(s)+4H2(g)。 请回答:
Fe3O4(s)+4H2(g)。 请回答:
(1)虚线框处宜选择的装置是_________ (填“甲”或“乙”);实验时应先将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是_______________ 。
(2)实验后,取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由_______ 。

已知:3Fe(s)+4H2O(g)
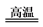 Fe3O4(s)+4H2(g)。 请回答:
Fe3O4(s)+4H2(g)。 请回答:(1)虚线框处宜选择的装置是
(2)实验后,取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由
您最近一年使用:0次
2017-11-06更新
|
2613次组卷
|
6卷引用:浙江省2017年11月普通高校招生选考科目考试化学试题
浙江省2017年11月普通高校招生选考科目考试化学试题2017年11月浙江省普通高校招生选考科目考试化学试题浙江省杭州市富阳区新登中学2018-2019学年高一上学期期末模拟化学试题(已下线)【浙江新东方】在线化学38(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)新疆柯坪县柯坪湖州国庆中学2021-2022学年高三上学期第一次月考化学试题
真题
名校
6 . 某同学将铁铝合金样品溶解后取样25.00mL,分离并测定Fe3+的浓度,实验方案设计如下:

已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5度,微溶于水,在较高的盐酸浓度下,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]而溶于乙醚,当盐酸浓度降低时,该化合物解离。
请回答:
(1)操作A的名称是______________ 。
(2)经操作A后,为判断Fe3+是否有残留,请设计实验方案_____________________ 。
(3)蒸馏装置如下图所示,装置中存在的错误是_______________________________ 。

(4)滴定前,加入的适量溶液B是_________ 。
A.H2SO3—H3PO4 B.H2SO4—H3PO4
C.HNO3—H3PO4 D.HI—H3PO4
(5)滴定达到终点时,消耗0.1000 mol·L-1 K2Cr2O7溶液6.00mL。根据该实验数据,试样X中c(Fe3+)为____________ 。
(6)上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是_______ 。
A.稀释被测试样 B.减少被测试样取量
C.增加平行测定次数 D.降低滴定剂浓度

已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5度,微溶于水,在较高的盐酸浓度下,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]而溶于乙醚,当盐酸浓度降低时,该化合物解离。
请回答:
(1)操作A的名称是
(2)经操作A后,为判断Fe3+是否有残留,请设计实验方案
(3)蒸馏装置如下图所示,装置中存在的错误是

(4)滴定前,加入的适量溶液B是
A.H2SO3—H3PO4 B.H2SO4—H3PO4
C.HNO3—H3PO4 D.HI—H3PO4
(5)滴定达到终点时,消耗0.1000 mol·L-1 K2Cr2O7溶液6.00mL。根据该实验数据,试样X中c(Fe3+)为
(6)上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是
A.稀释被测试样 B.减少被测试样取量
C.增加平行测定次数 D.降低滴定剂浓度
您最近一年使用:0次
2017-11-04更新
|
750次组卷
|
4卷引用:2016年4月浙江省普通高校招生选考科目考试化学试题
2016年4月浙江省普通高校招生选考科目考试化学试题浙江省宁波市北仑中学2019-2020学年高二上学期期中考试化学(1班)试题(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)【优等生百日捷进提升系列】专题10 定量化学实验
真题
7 . FeSO4受热分解的化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
请回答:
将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3。能说明SO2存在的实验现象是_______ ;为测定BaSO4沉淀的质量,后续的操作步骤依次为____ 、洗涤、干燥、称量。
试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)_______ 。
 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑请回答:
将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3。能说明SO2存在的实验现象是

试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)
您最近一年使用:0次
2017-04-14更新
|
1574次组卷
|
6卷引用:2017届浙江省高三4月普通高校招生选考科目考试化学试卷
2017届浙江省高三4月普通高校招生选考科目考试化学试卷浙江省2018版考前特训(2017年10月)压轴特训:3 第28题 基础化学实验题专练浙江省2017届高三新高考选考科目考试化学试题(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)高一必修第一册(鲁科2019)第3章 第2节 硫的转化 高考帮(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物



