1 . 金属铝质轻且具有良好的抗腐蚀性,在日常生活与工业生产中有非常重要的作用。请回答下列问题:
(1)31号元素镓(Ga)与铝同主族。镓的原子结构示意图为___________ ,写出金属镓与盐酸反应的化学方程式:___________ 。铍的单质、化合物与铝的单质、化合物分别具有相似的化学性质,写出 溶液与过量NaOH溶液反应的离子方程式:
溶液与过量NaOH溶液反应的离子方程式:___________ 。
(2)人类最早使用的金属材料的主要成分是铜。下列说法中正确的是___________(填字母)。
(3)向稀 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)
恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)___________ 。
(4)某同学对铝与 发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
①上述置换反应的化学方程式为___________ 。
②该同学推测铝热反应得到的熔融物中还含有 ,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含
,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含 。该同学的实验方案是否合理?
。该同学的实验方案是否合理?___________ (填“合理”或“不合理”)。理由是___________ 。
(1)31号元素镓(Ga)与铝同主族。镓的原子结构示意图为
 溶液与过量NaOH溶液反应的离子方程式:
溶液与过量NaOH溶液反应的离子方程式:(2)人类最早使用的金属材料的主要成分是铜。下列说法中正确的是___________(填字母)。
| A.青铜和黄铜均是合金 | B.铜表面易形成致密的氧化膜 |
C.铜绿[ ]属于碱式盐 ]属于碱式盐 | D.金属铜能与 溶液发生置换反应 溶液发生置换反应 |
 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)
恰好完全沉淀,此时铝元素的存在形式主要为(用化学式表示)(4)某同学对铝与
 发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。
发生铝热反应的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。①上述置换反应的化学方程式为
②该同学推测铝热反应得到的熔融物中还含有
 ,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含
,他设计了如下方案来验证:取一块该熔融物,冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含 。该同学的实验方案是否合理?
。该同学的实验方案是否合理?
您最近一年使用:0次
名校
解题方法
2 . 铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次
3 . 金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。请回答下列问题
(1)31号元素镓(Ga)与铝同族。镓(Ga)在周期表的位置是___________ ;写出镓的氯化物和氨水反应的化学方程式___________ 。铍、铝二者的单质、化合物均具有相似的化学性质,写出BeCl2溶液与Na2BeO2的水溶液混合的化学方程式___________ 。
(2)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,不正确的是___________(填字母)
(3)在稀 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为
恰好完全沉淀,此时铝元素的存在形式主要为___________ (用化学式表示)。
(4)某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入沙中”。由化学手册查阅得有关物质的熔、沸点数据如表。
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,你认为他的解释是否合理___________ (填“合理”或“不合理”)。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所涉及的反应的离子方程式为___________ 。
③另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:取一块该熔融物冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含有Fe2O3.该同学的实验方案是否合理?___________ (填“合理”或“不合理”)。理由:___________ 。
(1)31号元素镓(Ga)与铝同族。镓(Ga)在周期表的位置是
(2)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,不正确的是___________(填字母)
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.铜与O2反应生成黑色的CuO |
| D.CuSO4·5H2O是一种混合物,加热后变为白色固体 |
 溶液中加入适量
溶液中加入适量 溶液至
溶液至 恰好完全沉淀,此时铝元素的存在形式主要为
恰好完全沉淀,此时铝元素的存在形式主要为(4)某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入沙中”。由化学手册查阅得有关物质的熔、沸点数据如表。
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1460 |
| 沸点/℃ | 2467 | 2980 | 2750 |
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,你认为他的解释是否合理
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所涉及的反应的离子方程式为
③另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:取一块该熔融物冷却后投入到少量稀硫酸中,向反应后的混合液中滴加KSCN溶液,观察到溶液颜色未变红,证明该熔融物中不含有Fe2O3.该同学的实验方案是否合理?
您最近一年使用:0次
名校
4 . 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为___________ 。(写出一条即可)

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:
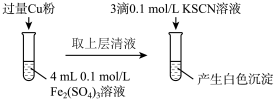
①Fe3+与Cu反应的离子方程式为___________ 。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
Cu2+与SCN-反应的离子方程式为 ___________ 。
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
①方案ⅰ预期现象与实际现象相同,并不能证明补贴口服液中一定含有Fe2+,猜想理由是:___________ 。
②方案ⅱ中实验现象是___________ ,证明补铁口服液中含有Fe2+。
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:

①Fe3+与Cu反应的离子方程式为
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
| 实验方案 | 现象 |
| 步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 无明显现象 |
| 步骤2:取4mL 0.1 mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 产生白色沉淀 |
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
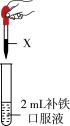 | 方案 | 试剂X |
| 方案ⅰ | 1mL 1mol/L酸性KMnO4溶液 | |
| 方案ⅱ | 依次加入5滴KSCN溶液、1mL新制氯水 |
②方案ⅱ中实验现象是
您最近一年使用:0次
5 . 某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积________ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:_______________ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为______ 色,证明含有Fe3+。
(4)通入氯气的目的是___________________ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:______________________ 。

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:
您最近一年使用:0次
解题方法
6 . 钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是___________ 。
② 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是___________ (填“还原产物”或“氧化产物”)。
(2)铁及其重要化合物之间的部分转化关系如图所示。___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ 。
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为(用化学方程式表达)___________ 。
(1)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是②
 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是(2)铁及其重要化合物之间的部分转化关系如图所示。
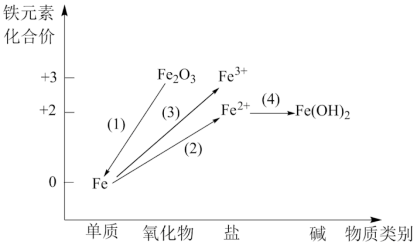
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
7 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
8 . 菠菜营养丰富,素有“蓅菜之王”的美称。菠菜含有丰富的铁(铁元素以草酸亚铁的形式存在)、草酸盐、碳酸盐等,某化学兴趣小组对于生活中流传的“吃菠菜补铁”之说产生兴趣,设计实验进行相关探究。
已知:草酸亚铁是一种淡黄色难溶于水的晶体。
I.菠菜中铁元素含量的测定
(1)取 洗净晾干的新鲜菠菜,切碎后装入煤埚中,放入烘箱烧成灰烬。将灰烬用
洗净晾干的新鲜菠菜,切碎后装入煤埚中,放入烘箱烧成灰烬。将灰烬用 硫酸溶液溶解,加热煮沸
硫酸溶液溶解,加热煮沸 ,过滤后滴加适量
,过滤后滴加适量 溶液并稀释至
溶液并稀释至 ,取出
,取出 并加入5滴
并加入5滴 溶液。
溶液。
①加入 的目的是
的目的是___________ 。
②加入 溶液后,可观察到的现象为
溶液后,可观察到的现象为___________ 。
(2)取不同浓度的___________ [填“ ”或“
”或“ ”]标准溶液各
”]标准溶液各 ,分别滴加5滴KSCN溶液,发现与②中观察到的溶液颜色最接近的标准溶液的浓度为
,分别滴加5滴KSCN溶液,发现与②中观察到的溶液颜色最接近的标准溶液的浓度为 。由此计算可得,每
。由此计算可得,每 新鲜菠菜中含有铁元素的质量约为
新鲜菠菜中含有铁元素的质量约为___________  。
。
II.草酸亚铁晶体 的分解实验
的分解实验

(3)加热反应开始前,需要先通一段时间的N2,目的是___________ 。
(4)实验开始后;装置B中出现浑浊,证明分解产物中存在CO的现象是___________ 。
(5)将充分反应后的固体残余物投入经煮沸的稀硫酸中,固体完全溶解且无气体放出,取反应液,向其中加入KSCN溶液无血红色出现,写出装置A中发生反应的化学方程式:___________ 。
(6)从环保角度考虑,该套实验装置的明显缺陷是___________ 。
已知:草酸亚铁是一种淡黄色难溶于水的晶体。
I.菠菜中铁元素含量的测定
(1)取
 洗净晾干的新鲜菠菜,切碎后装入煤埚中,放入烘箱烧成灰烬。将灰烬用
洗净晾干的新鲜菠菜,切碎后装入煤埚中,放入烘箱烧成灰烬。将灰烬用 硫酸溶液溶解,加热煮沸
硫酸溶液溶解,加热煮沸 ,过滤后滴加适量
,过滤后滴加适量 溶液并稀释至
溶液并稀释至 ,取出
,取出 并加入5滴
并加入5滴 溶液。
溶液。①加入
 的目的是
的目的是②加入
 溶液后,可观察到的现象为
溶液后,可观察到的现象为(2)取不同浓度的
 ”或“
”或“ ”]标准溶液各
”]标准溶液各 ,分别滴加5滴KSCN溶液,发现与②中观察到的溶液颜色最接近的标准溶液的浓度为
,分别滴加5滴KSCN溶液,发现与②中观察到的溶液颜色最接近的标准溶液的浓度为 。由此计算可得,每
。由此计算可得,每 新鲜菠菜中含有铁元素的质量约为
新鲜菠菜中含有铁元素的质量约为 。
。II.草酸亚铁晶体
 的分解实验
的分解实验
(3)加热反应开始前,需要先通一段时间的N2,目的是
(4)实验开始后;装置B中出现浑浊,证明分解产物中存在CO的现象是
(5)将充分反应后的固体残余物投入经煮沸的稀硫酸中,固体完全溶解且无气体放出,取反应液,向其中加入KSCN溶液无血红色出现,写出装置A中发生反应的化学方程式:
(6)从环保角度考虑,该套实验装置的明显缺陷是
您最近一年使用:0次
解题方法
9 . 铁及其重要化合物之间的部分转化关系如图所示。
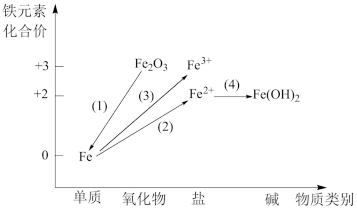
(1)下列金属矿物中用于冶炼金属铁的是___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在加热的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为___________ 色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ ;
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,写出Fe(OH)2被氧化的化学方程式___________ ,请你设计一个防止Fe(OH)2被O2氧化的实验方案 ___________ 。

(1)下列金属矿物中用于冶炼金属铁的是
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在加热的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,写出Fe(OH)2被氧化的化学方程式
您最近一年使用:0次
名校
解题方法
10 . 某小组同学探究菠菜补铁的可行性。
【提出猜想】假设1:菠菜中铁元素以Fe2+形式存在;
假设2:______;
假设3:菠菜中铁元素以Fe2+和Fe3+形式存在。
(1)将假设2补充完整:_______ 。
【设计实验方案】
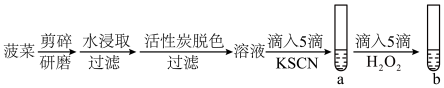
(2)加入KSCN的目的是_______ 。
(3)若观察到_______ ,则证明假设3成立。
(4)经实验,试管a、b中均无明显现象。为探查原因,查阅资料得知:菠菜中的铁元素以草酸亚铁(FeC2O4)的形式存在。FeC2O4难溶于水,高温下可分解产生FeO以及气体产物。
①经检验,气体产物中含有CO2,由此同学们推测气体中应含有CO,理由是______ 。
②实验证明气体产物为CO2和CO,n(CO2):n(CO)=______ 。
【实验反思】
(5)未检测到菠菜中的铁元素,原因可能是_______ 。
【修正实验方案】

(6)①试剂x为______ 。
②取适量滤液于试管中,加入试剂y,即可证明菠菜中含有+2价铁元素。该试剂y为_______ ,现象是______ 。
【可行性分析】
(7)成年人每天所需铁元素的质量为20mg,每100g菠菜中含铁元素约为2mg,铁吸收率约为2%。
①100g菠菜中含FeC2O4的物质的量为______ mol(列出计算式)。
②若要满足成年人对铁元素的需求量,则需要每天食用菠菜______ kg。
【提出猜想】假设1:菠菜中铁元素以Fe2+形式存在;
假设2:______;
假设3:菠菜中铁元素以Fe2+和Fe3+形式存在。
(1)将假设2补充完整:
【设计实验方案】

(2)加入KSCN的目的是
(3)若观察到
(4)经实验,试管a、b中均无明显现象。为探查原因,查阅资料得知:菠菜中的铁元素以草酸亚铁(FeC2O4)的形式存在。FeC2O4难溶于水,高温下可分解产生FeO以及气体产物。
①经检验,气体产物中含有CO2,由此同学们推测气体中应含有CO,理由是
②实验证明气体产物为CO2和CO,n(CO2):n(CO)=
【实验反思】
(5)未检测到菠菜中的铁元素,原因可能是
【修正实验方案】

(6)①试剂x为
②取适量滤液于试管中,加入试剂y,即可证明菠菜中含有+2价铁元素。该试剂y为
【可行性分析】
(7)成年人每天所需铁元素的质量为20mg,每100g菠菜中含铁元素约为2mg,铁吸收率约为2%。
①100g菠菜中含FeC2O4的物质的量为
②若要满足成年人对铁元素的需求量,则需要每天食用菠菜
您最近一年使用:0次



