1 . 实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢 ) 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。
①甲同学认为 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为___________ (选填序号)
A. 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液
②乙同学取 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为___________ 。(保留三位有效数字)。
(2)分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是___________ 。

(3)装置A中试剂的作用是___________ ,反应的离子方程式___________ 。
(4)简述确认气体Y中含有 的实验现象
的实验现象___________ 。
(5)如果气体Y中含有 ,预计实验现象应是
,预计实验现象应是___________ 。
(1)称取铁钉(
 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。①甲同学认为
 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液②乙同学取
 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为(2)分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有
 的实验现象
的实验现象(5)如果气体Y中含有
 ,预计实验现象应是
,预计实验现象应是
您最近一年使用:0次
2021-10-10更新
|
285次组卷
|
5卷引用:2014-2015江西省临川市第一中学高一上学期期末化学试卷
解题方法
2 . FeCl3是重要的化工原料,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解
(1)制备无水氯化铁
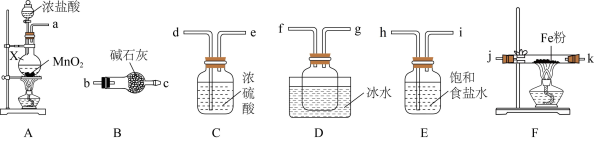
①仪器X的名称为______________ 。
②装置的连接顺序为a→______ → j,k →________ (按气流方向,用小写字母表示)。
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为____ 。
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①____________
④实验结论:反应(i)、(ii)的活化能大小关系是:E(i)____ E(ii)(填“>”、 “<”或“=”,下同),平衡常数大小关系是:K(i)__________ K(ii)。
⑤另取5 mL l mol L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是____ 。
(1)制备无水氯化铁

①仪器X的名称为
②装置的连接顺序为a→
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①
| 步骤 | 现象 | 结论 |
| Ⅰ.取5 mL1 mol⋅L−1 FeCl3溶液于试管中,通入SO2至饱和 | 溶液很快由黄色变为红棕色 | |
| Ⅱ.用激光笔照射步骤Ⅰ中的红棕色溶液 | 溶液中无明显光路 | ②红棕色物质不是 |
| Ⅲ将步骤Ⅰ中的溶液静置 | 1小时后,溶液逐渐变为浅绿色 | |
| IV.向步骤Ⅲ中溶液加入2滴K3[Fe(CN)6]溶液 | ③ | 溶液中含有Fe2+ |
⑤另取5 mL l mol
 L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
您最近一年使用:0次
2020-11-24更新
|
305次组卷
|
2卷引用:江西省九江市浔阳区九江市第七中学2021届高三上学期期中考试化学试题
名校
3 . 无水FeCl3呈棕红色,极易潮解,100 ℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
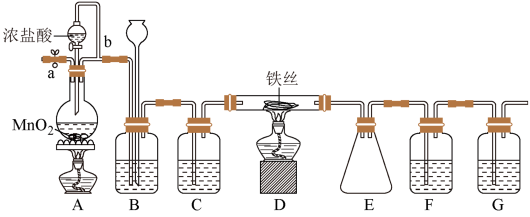
(1)装置A中反应的离子方程式为________________ 。
(2)装置C中所加的试剂为____________ 。
(3)导管b的作用为___________ ;装置G的作用为________ 。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,是因为_____ 。
(5)为检验所得产品为FeCl3,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入____________ ,___________ (填试剂和现象)。

(1)装置A中反应的离子方程式为
(2)装置C中所加的试剂为
(3)导管b的作用为
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,是因为
(5)为检验所得产品为FeCl3,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入
您最近一年使用:0次
2019-10-14更新
|
454次组卷
|
6卷引用:江西省南昌市第十中学2020届高三上学期期中考试化学试题
江西省南昌市第十中学2020届高三上学期期中考试化学试题江西省丰城市第九中学2020届高三上学期期中考试化学试题甘肃省甘谷第一中学2020届高三上学期第一次检测化学试题海南省儋州市第一中学2020届高三上学期第二次月考化学试卷河南省商丘市虞城高中2020届高三11月月考化学试题(已下线)3.1.2 铁及其化合物之间的转化关系练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)
名校
解题方法
4 . 下列关于Fe3+、Fe2+性质实验的说法错误的是( )


| A.用如图装置可以制备Fe(OH)2沉淀 |
| B.配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度 |
| C.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,此现象不能确定溶液中含有Fe2+ |
| D.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化 |
您最近一年使用:0次
2016-12-09更新
|
481次组卷
|
16卷引用:2015-2016学年河北保定一中高二下期末化学试卷
2015-2016学年河北保定一中高二下期末化学试卷【全国百强校】甘肃省静宁县第一中学2019届高三上学期第一次模拟考试化学试题黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题河北省邯郸市大名县第一中学2019-2020学年高二下学期第一次半月考化学试题安徽省滁州市定远县民族中学2020-2021学年高一11月月考化学试题江西省安福中学2021-2022学年高二上学期开学考试化学(理)试题安徽省滁州市定远育才学校2021-2022学年高二上学期开学摸底考试化学试题安徽省滁州市定远县育才学校2021-2022学年高一上学期月考化学试题宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题(已下线)第3讲 铁盐及其亚铁盐陕西省西安市铁一中学2023-2024学年高三上学期9月月考化学试题
5 . Ⅰ.化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有___________
①氢氧化亚铁在空气中最终变为灰绿色; ②淀粉溶液遇碘化钾变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色 ④品红溶液通入过量氯气后褪色
⑤无水硫酸铜吸收水蒸气变成浅绿色; ⑥新制氯水久置后变为无色;
Ⅱ.某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
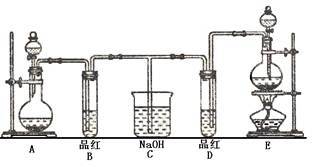
(1) 实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中_________ 装置(填装置序号)制Cl2。在制Cl2的反应中MnO2表现出的性质是_____________ 。
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___________ ,D:______________ 。
(3) 装置C的作用是_____________________________________________________ 。
(4) 甲乙两同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:____________ 。

②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:_________ ,并写出其相应的离子方程式:___________ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是:__________ 。
①氢氧化亚铁在空气中最终变为灰绿色; ②淀粉溶液遇碘化钾变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色 ④品红溶液通入过量氯气后褪色
⑤无水硫酸铜吸收水蒸气变成浅绿色; ⑥新制氯水久置后变为无色;
Ⅱ.某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。

(1) 实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:
(3) 装置C的作用是
(4) 甲乙两同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:

②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是:
您最近一年使用:0次
6 . 科学的实验方法为我们探索物质世界提供了一把金钥匙。下列实验能达到目的的是( )
| 选项 | 实验目的 | 实验步骤及现象 |
| A | 探究铁与水在高温下发生反应 | 将水蒸气通过灼热的铁粉,观察粉末变为红褐色 |
| B | 证明溶液中含有Fe3+ | 向溶液中加入KSCN溶液,观察到溶液变红 |
| C | 证明钠与氧气反应会生成过氧化钠 | 切开金属钠,钠表面的银白色会逐渐褪去 |
| D | 证明二氧化硫具有漂白性 | 将SO2通入酸性KMnO4溶液中,溶液褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-11-28更新
|
188次组卷
|
3卷引用:湖北省沙市中学2019-2020学年高二上学期期中考试化学(学考)试题
7 . 用如图中的实验装置进行相应的实验,不能 达到实验目的的是( )




| A.用图甲装置,可快速制取氨气 |
| B.用图乙装置,分离饱和食盐水溶液中的食盐和水 |
| C.用图丙装置操作方法,可检验Fe2+ |
| D.用图丁装置,可说明浓H2SO4具有脱水性和强氧化性,SO2具有漂白性和还原性 |
您最近一年使用:0次
2020-05-30更新
|
181次组卷
|
3卷引用:江西省南昌县莲塘第三中学2019-2020学年高一下学期期末考试化学试题
名校
8 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去Cu中少量CuO | 加入稀硝酸溶解、过滤、洗涤及干燥 |
| B | FeCl3废蚀刻液(含FeCl2、FeCl3、CuCl2、HCl)制备FeCl2溶液 | 废蚀刻液中加入过量铁粉、充分搅拌、过滤 |
| C | 检验碳与浓硫酸反应的气态产物中含SO2和CO2 | 将产生的气体依次通过澄清石灰水和品红溶液 |
| D | 分离苯萃取溴水的水层和有机层 | 先放出水层,然后换一个烧杯再放出有机层 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-11-04更新
|
459次组卷
|
3卷引用:江西省上饶中学2019届高三上学期开学检测化学试题
9 . 下列实验设计不能达到实验目的的是
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 用洁净铂丝蘸取某溶液进行焰色反应 | 检验溶液中是否有钠元素 |
| D | 用铝盐溶液与氨水反应 | 制备氢氧化铝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . Fe3O4呈黑色,有磁性,应用广泛。以Fe3O4为吸附剂去除水中含磷物质是一种新的除磷措施。
(1)检验Fe3O4中铁元素的价态;用盐酸溶解Fe3O4,取少量滴加______________ ,溶液变红;另取少量滴加铁氰化钾溶液,产生蓝色沉淀。
(2)氧化沉淀法制备
I.向稀硫酸中加入过量铁粉,得到FeSO4溶液。加过量铁粉的作用是_________________ 。II.在氮气保护下,向热NaOH溶液中加入FeSO4溶液,搅拌,得到Fe(OH)2浊液。将NaNO3溶液滴入Fe(OH)2浊液中,充分反应得到Fe3O4。
①用红色石蕊试纸检验产物,__________________ (填现象),证明有NH3。
②写出NaNO3溶液与Fe(OH)2反应制备Fe3O4的离子方程式___________________________ 。
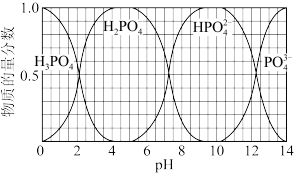
(3)含磷各微粒在溶液中的物质的量分数与pH的关系如图所示:(图中三个交点的对应pH分别为2.2、7.2、12.4)。 下列分析不正确的是________________
A.KH2PO4水溶液中:c(H+)< c(OH-)
B. K2HPO4溶液显碱性,原因是HPO42-的水解程度大于其电离程度
C.磷酸一级电离常数K1=10-2.2
D.想获得较纯的KH2PO4溶液,可将溶液pH控制 在4-5之间
(4)已知:信息①溶液pH对吸附剂Fe3O4表面所带电荷的影响:
pH <6.8,Fe3O4表面带正电荷;
pH=6.8,Fe3O4表面不带电荷;
pH >6.8,Fe3O4表面带负电荷。
信息②吸附剂Fe3O4对含磷微粒的去除率随pH的变化如图所示。现将吸附剂Fe3O4加到KH2PO4溶液中,调节溶液pH。请根据以上信息及图示回答下列问题:
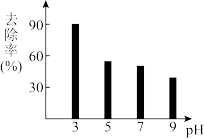
①pH=3时,吸附的主要微粒是__________________ 。
②与pH=5相比,pH=9时的去除率明显下降,原因是_____________________________ 。
(1)检验Fe3O4中铁元素的价态;用盐酸溶解Fe3O4,取少量滴加
(2)氧化沉淀法制备
I.向稀硫酸中加入过量铁粉,得到FeSO4溶液。加过量铁粉的作用是
①用红色石蕊试纸检验产物,
②写出NaNO3溶液与Fe(OH)2反应制备Fe3O4的离子方程式
(3)含磷各微粒在溶液中的物质的量分数与pH的关系如图所示:(图中三个交点的对应pH分别为2.2、7.2、12.4)。 下列分析不正确的是

A.KH2PO4水溶液中:c(H+)< c(OH-)
B. K2HPO4溶液显碱性,原因是HPO42-的水解程度大于其电离程度
C.磷酸一级电离常数K1=10-2.2
D.想获得较纯的KH2PO4溶液,可将溶液pH控制 在4-5之间
(4)已知:信息①溶液pH对吸附剂Fe3O4表面所带电荷的影响:
pH <6.8,Fe3O4表面带正电荷;
pH=6.8,Fe3O4表面不带电荷;
pH >6.8,Fe3O4表面带负电荷。
信息②吸附剂Fe3O4对含磷微粒的去除率随pH的变化如图所示。现将吸附剂Fe3O4加到KH2PO4溶液中,调节溶液pH。请根据以上信息及图示回答下列问题:

①pH=3时,吸附的主要微粒是
②与pH=5相比,pH=9时的去除率明显下降,原因是
您最近一年使用:0次



