解题方法
1 . 某实验小组在实验室进行Fe2+与Fe3+相互转化的实验。
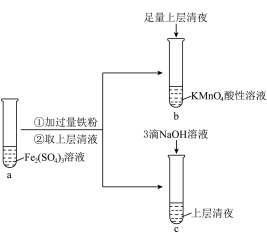
(1)向试管a中加入过量铁粉的离子方程式是___________ 。
(2)试管b中的实验现象是___________ 。
(3)试管c中产生白色沉淀,一段时间后部分沉淀变为红褐色。写出白色沉淀变为红褐色的化学方程式___________ 。
(4)实验小组为探究反应物浓度对Fe(OH)2制备效果的影响,以Fe(OH)2沉淀白色持续时间(t)为指标,t越大,实验效果越好。部分实验数据如下(w表示质量分数):
①实验i、ii、iii的目的是___________ 。
②小组同学通过实验得出结论:其他条件不变时,所用NaOH溶液的浓度越大,实验效果越好,推断的证据是___________ 。

(1)向试管a中加入过量铁粉的离子方程式是
(2)试管b中的实验现象是
(3)试管c中产生白色沉淀,一段时间后部分沉淀变为红褐色。写出白色沉淀变为红褐色的化学方程式
(4)实验小组为探究反应物浓度对Fe(OH)2制备效果的影响,以Fe(OH)2沉淀白色持续时间(t)为指标,t越大,实验效果越好。部分实验数据如下(w表示质量分数):
| 实验 | 序号 | w(FeSO4)/% | w(NaOH)/% | t/s |
 | i | 2.5 | 15 | 149 |
| ii | 5 | 15 | 138 | |
| iii | 10 | 15 | 99 | |
| iv | 5 | 25 | 142 | |
| v | 5 | 35 | 180 |
②小组同学通过实验得出结论:其他条件不变时,所用NaOH溶液的浓度越大,实验效果越好,推断的证据是
您最近一年使用:0次
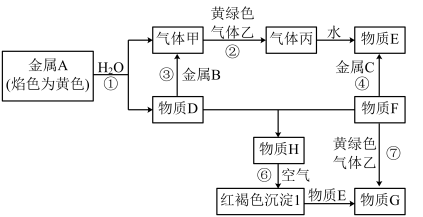
2 . I.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:_______ ;
(2)反应③的离子方程式:_______ ;
(3)反应⑦的离子方程式:_______ ;
(4)反应⑥的化学方程式:_______ 。
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
(5)铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是_______ 的质量分数;当合金熔点最低时,合金中铅与锡的质量比为_______ 。

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
(7)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿[主要成分Cu2(OH)2CO3],从其化学式可知铜绿是铜与_______ (填物质的化学式)长期作用的结果。

请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:
(2)反应③的离子方程式:
(3)反应⑦的离子方程式:
(4)反应⑥的化学方程式:
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
| A.20~40℃ | B.60~80℃ | C.230~250℃ | D.300~320℃ |
您最近一年使用:0次
2022-12-07更新
|
115次组卷
|
2卷引用:9.3.2合金及其应用(课后)-2019苏教版必修2课前课中课后
19-20高一上·湖北武汉·期末
名校
解题方法
3 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。

(1)物质A的化学式为________ ,D的化学式为________ ;
(2)B和R在溶液中反应生成F的离子方程式为________________ ;
(3)请写出两种A的用途:________ ,________ ;
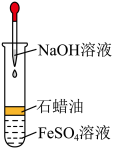
(4)H在潮湿空气中变成M的实验现象是________________ ;
(5)A能氧化E生成M,试写出A恰好氧化E的离子方程式_______________ 。

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)请写出两种A的用途:
(4)H在潮湿空气中变成M的实验现象是
(5)A能氧化E生成M,试写出A恰好氧化E的离子方程式
您最近一年使用:0次



