名校
解题方法
1 . 采用氧化沉淀法可以利用绿矾制取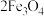 ,其制取流程如图所示:
,其制取流程如图所示:___________ (填写化学式),由溶液 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→___________ →过滤洗涤 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。
(2)某兴趣小组模仿如图流程制取 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取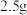 工业绿矾,配制成
工业绿矾,配制成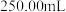 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用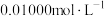 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为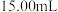 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为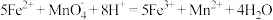 )则绿矾的质量分数为
)则绿矾的质量分数为___________ (计算结果保留三位小数)。
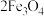 ,其制取流程如图所示:
,其制取流程如图所示:
 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→ 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。(2)某兴趣小组模仿如图流程制取
 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取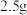 工业绿矾,配制成
工业绿矾,配制成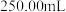 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用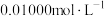 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为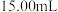 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为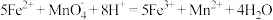 )则绿矾的质量分数为
)则绿矾的质量分数为
您最近半年使用:0次
解题方法
2 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。日常生活中可通过食物摄入铁元素,例如黑木耳中就含有比较丰富的铁元素。某研究性学习小组为测定某地黑木耳中铁的含量,开展了如下研究与实践活动。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质___________ (填“难”或“易”)溶于水。
(2)取少量滤液于试管中,滴入 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、___________ (填离子符号)。
(3)滤液与Fe生成A的离子方程式为___________ 。
(4)由A转化为B可加入的试剂X可以是___________ (填标号)。
a.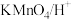 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为___________ 。C转化成D的化学方程式为___________ 。
(6)将 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到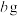 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为___________ (用含a、b、c的代数式表示)。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取
 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。【研究与实践活动二】
研究黑木耳中铁的含量:称取
 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。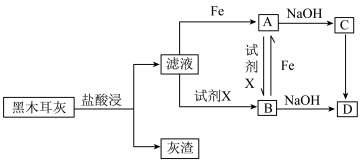
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质
(2)取少量滤液于试管中,滴入
 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、(3)滤液与Fe生成A的离子方程式为
(4)由A转化为B可加入的试剂X可以是
a.
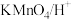 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为
(6)将
 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到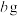 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为
您最近半年使用:0次
名校
3 . 铁黑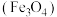 是常见的铁系颜料,:可利用硫铁矿废水为原料进行制备,不仅为硫铁矿废水的处理开辟了新途径,同时也实现了资源利用,生产流程如下:
是常见的铁系颜料,:可利用硫铁矿废水为原料进行制备,不仅为硫铁矿废水的处理开辟了新途径,同时也实现了资源利用,生产流程如下:
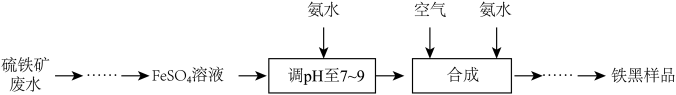
(1)在实验室中,为防止 溶液被氧化变质,需要往试剂瓶中加入
溶液被氧化变质,需要往试剂瓶中加入_______ ,检验 溶液是否变质的常用试剂是
溶液是否变质的常用试剂是_______ 。
(2)加入氨水调 至7~9时,发生反应的离子方程式为
至7~9时,发生反应的离子方程式为_______ ; “合成”步骤中, 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(3)某化学学习小组测定产品中铁的含量,实验步骤如下:
步骤一:取 铁黑样品于锥形瓶中,加入足量盐酸,加热使之完全溶解。
铁黑样品于锥形瓶中,加入足量盐酸,加热使之完全溶解。
步骤二:加入过量的 溶液将
溶液将 还原成
还原成 ,再加入
,再加入 溶液。
溶液。
步骤三:在酸性条件下,加入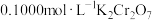 溶液与
溶液与 发生反应:
发生反应:  ,恰好完全反应时,消耗
,恰好完全反应时,消耗 溶液
溶液 。
。
由步骤二得出 的还原性
的还原性_______  的还原性(填“强于”或“弱于”);加入
的还原性(填“强于”或“弱于”);加入 溶液的目的是
溶液的目的是_______ 。样品中 元素的质量分数为
元素的质量分数为_______  。
。
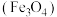 是常见的铁系颜料,:可利用硫铁矿废水为原料进行制备,不仅为硫铁矿废水的处理开辟了新途径,同时也实现了资源利用,生产流程如下:
是常见的铁系颜料,:可利用硫铁矿废水为原料进行制备,不仅为硫铁矿废水的处理开辟了新途径,同时也实现了资源利用,生产流程如下:
(1)在实验室中,为防止
 溶液被氧化变质,需要往试剂瓶中加入
溶液被氧化变质,需要往试剂瓶中加入 溶液是否变质的常用试剂是
溶液是否变质的常用试剂是(2)加入氨水调
 至7~9时,发生反应的离子方程式为
至7~9时,发生反应的离子方程式为 转化为
转化为 的化学方程式为
的化学方程式为(3)某化学学习小组测定产品中铁的含量,实验步骤如下:
步骤一:取
 铁黑样品于锥形瓶中,加入足量盐酸,加热使之完全溶解。
铁黑样品于锥形瓶中,加入足量盐酸,加热使之完全溶解。步骤二:加入过量的
 溶液将
溶液将 还原成
还原成 ,再加入
,再加入 溶液。
溶液。步骤三:在酸性条件下,加入
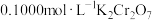 溶液与
溶液与 发生反应:
发生反应:  ,恰好完全反应时,消耗
,恰好完全反应时,消耗 溶液
溶液 。
。由步骤二得出
 的还原性
的还原性 的还原性(填“强于”或“弱于”);加入
的还原性(填“强于”或“弱于”);加入 溶液的目的是
溶液的目的是 元素的质量分数为
元素的质量分数为 。
。
您最近半年使用:0次
2023-04-23更新
|
196次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一上学期教学质量检测(期末)化学试题
名校
4 . 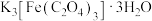 (三草酸合铁酸钾)为亮绿色晶体,易溶于水,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[
(三草酸合铁酸钾)为亮绿色晶体,易溶于水,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[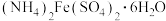 ]制备
]制备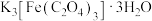 的流程如图所示。
的流程如图所示。
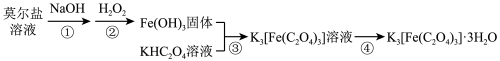
(1)步骤②反应时控制温度为40℃左右,原因是___________ 。
(2)步骤③将 加入到
加入到 溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量
溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量___________ (已知:常温下 溶液的pH约为3.5)。
溶液的pH约为3.5)。
(3)步骤④具体实验操作有___________ 、过滤、洗涤、干燥。
(4)制备的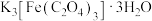 中可能含有
中可能含有 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取m g样品于锥形瓶中,加入稀 溶解,水浴加热至75℃。用cmol/L的
溶解,水浴加热至75℃。用cmol/L的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液V1mL。
溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液V2mL。
溶液V2mL。
①滴定过程中滴加 溶液的操作正确的是
溶液的操作正确的是___________ (填标号)。
a. b.
b.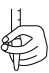 c.
c. d.
d.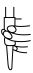
②Ⅱ中用 溶液滴定待测液,滴定至终点的现象是
溶液滴定待测液,滴定至终点的现象是___________ 。
③样品中所含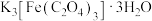 (M=491g/mol)的质量分数表达式为
(M=491g/mol)的质量分数表达式为___________ 。
④若步骤Ⅰ中滴入 溶液不足,则测得样品中Fe元素含量
溶液不足,则测得样品中Fe元素含量___________ (填“偏高”、“偏低”或“不变”)。
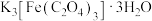 (三草酸合铁酸钾)为亮绿色晶体,易溶于水,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[
(三草酸合铁酸钾)为亮绿色晶体,易溶于水,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[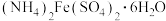 ]制备
]制备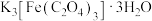 的流程如图所示。
的流程如图所示。
(1)步骤②反应时控制温度为40℃左右,原因是
(2)步骤③将
 加入到
加入到 溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量
溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量 溶液的pH约为3.5)。
溶液的pH约为3.5)。(3)步骤④具体实验操作有
(4)制备的
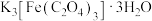 中可能含有
中可能含有 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:Ⅰ.取m g样品于锥形瓶中,加入稀
 溶解,水浴加热至75℃。用cmol/L的
溶解,水浴加热至75℃。用cmol/L的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液V1mL。
溶液V1mL。Ⅱ.向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液V2mL。
溶液V2mL。①滴定过程中滴加
 溶液的操作正确的是
溶液的操作正确的是a.
 b.
b. c.
c. d.
d.
②Ⅱ中用
 溶液滴定待测液,滴定至终点的现象是
溶液滴定待测液,滴定至终点的现象是③样品中所含
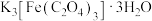 (M=491g/mol)的质量分数表达式为
(M=491g/mol)的质量分数表达式为④若步骤Ⅰ中滴入
 溶液不足,则测得样品中Fe元素含量
溶液不足,则测得样品中Fe元素含量
您最近半年使用:0次
2022-01-24更新
|
323次组卷
|
2卷引用:山东省临沂市2021-2022学年高二上学期期末考试化学试题
5 . 为测定一块铝铁合金中铝的含量,做如下实验:将该合金溶于过量盐酸,然后加入足量的NaOH溶液,待溶液中的沉淀全部变成红褐色时,过滤沉淀物并在空气中灼烧,最后所得红棕色粉末的质量与原来的合金试样质量正好相等。则合金中铝的质量分数为
| A.20% | B.30% | C.50% | D.70% |
您最近半年使用:0次
2022-02-24更新
|
110次组卷
|
2卷引用:河南省濮阳市2021-2022学年高一上学期期末考试化学试题
名校
6 . 铁及其化合物在生产、生活中有着广泛的应用。
I.钢(一种铁碳合金)是用量最大、用途最广的合金。钢中碳的含量范围为_______ 。
a.4.3%~5% b.2%~4.3% c.0.03%~2%
II.FeSO4可作补血剂,用于治疗缺铁性贫血症。用 FeSO4溶液制备 Fe(OH)2的操作是用长滴管吸取不含 O2的 NaOH 溶液,插入 FeSO4溶液液面下,再挤出 NaOH 溶液。这样操作的原因是为了防止 Fe(OH)2被氧化,写出其被氧化的化学反应方程式_______ 。
III.高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液自身发生氧化还原生成Fe3+,并快速产生 O2,在碱性溶液中较稳定。
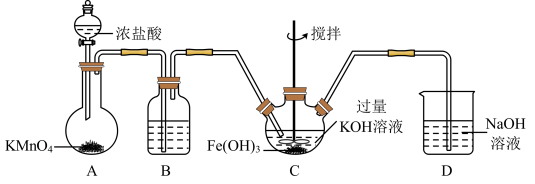
(1)制备K2FeO4
①在装置A中发生的化学反应中 HCl显示出来的性质为_______ 。
②C为制备K2FeO4装置,次氯酸钾与氢氧化铁在碱性环境中反应生成K2FeO4,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)探究K2FeO4的性质
取 C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液 a,经检验气体中含有 Cl2。为证明K2FeO4能否氧化 Cl-而产生 Cl2,设计如下方案:取少量溶液 a,滴加_______ 溶液至过量,溶液呈红色。由方案中溶液变红可知 a中含有 Fe3+,该离子的产生不能判断一定是由 K2FeO4被 Cl-还原而形成的,原因是_______ 。
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
①完成并配平离子方程式:_______
_______FeO +_______H+=_______Fe3++_______O2↑+_______H2O
+_______H+=_______Fe3++_______O2↑+_______H2O
②现取C中洗涤并干燥后的样品10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。(计算结果保留到 0.1%)
I.钢(一种铁碳合金)是用量最大、用途最广的合金。钢中碳的含量范围为
a.4.3%~5% b.2%~4.3% c.0.03%~2%
II.FeSO4可作补血剂,用于治疗缺铁性贫血症。用 FeSO4溶液制备 Fe(OH)2的操作是用长滴管吸取不含 O2的 NaOH 溶液,插入 FeSO4溶液液面下,再挤出 NaOH 溶液。这样操作的原因是为了防止 Fe(OH)2被氧化,写出其被氧化的化学反应方程式
III.高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液自身发生氧化还原生成Fe3+,并快速产生 O2,在碱性溶液中较稳定。

(1)制备K2FeO4
①在装置A中发生的化学反应中 HCl显示出来的性质为
②C为制备K2FeO4装置,次氯酸钾与氢氧化铁在碱性环境中反应生成K2FeO4,该氧化还原反应中氧化剂与还原剂的物质的量之比为
(2)探究K2FeO4的性质
取 C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液 a,经检验气体中含有 Cl2。为证明K2FeO4能否氧化 Cl-而产生 Cl2,设计如下方案:取少量溶液 a,滴加
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
①完成并配平离子方程式:
_______FeO
 +_______H+=_______Fe3++_______O2↑+_______H2O
+_______H+=_______Fe3++_______O2↑+_______H2O②现取C中洗涤并干燥后的样品10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近半年使用:0次
7 . 铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医疗上常用作补血剂。某课外活动小组为测定该补血剂中铁元素的含量,设计如下实验。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为______ mL(保留一位小数)。
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为__________________________ 。
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为_______________________ 。
(4)该补血剂中铁元素的质量分数为____________ ,若步骤③加入氨水的量不足,则实验结果_____ (填“偏大”、“偏小”、“无影响”)
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是_________________ 。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为
(4)该补血剂中铁元素的质量分数为
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是
您最近半年使用:0次
8 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近半年使用:0次
名校
9 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近半年使用:0次
名校
解题方法
10 . 碳酸亚铁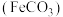 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
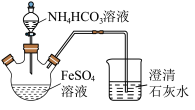
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是___________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3) 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:___________ 。
(4)某 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入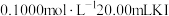 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程___________ 。
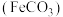 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)
 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:(4)某
 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入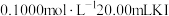 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程
您最近半年使用:0次



