名校
解题方法
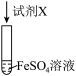
1 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: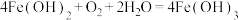 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近半年使用:0次
名校
2 . 关于甲、乙、丙、丁四套装置的说法正确的是
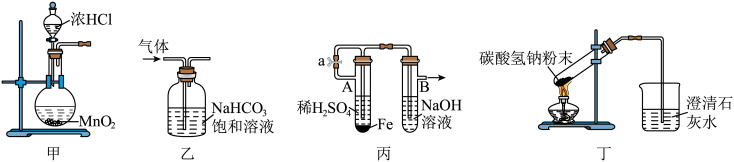

| A.用装置甲制取氯气 | B.用装置乙除去氯气中的少量氯化氢 |
| C.用装置丙制Fe(OH)2 | D.用装置丁证明碳酸氢钠受热易分解 |
您最近半年使用:0次
解题方法
3 . 利用铁元素价类二维图可以从不同角度研究含铁物质的性质及其转化关系,下列说法不正确 的是
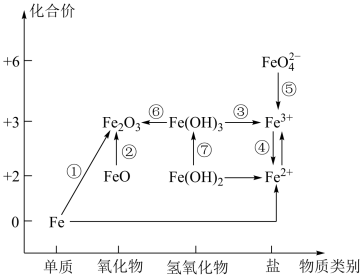

A.由图可预测高铁酸盐( )具有强氧化性 )具有强氧化性 |
| B.从图中可知Fe(OH)2无法一步转化为Fe(OH)3 |
| C.Fe2+→Fe3+的转化过程中铁元素被还原 |
| D.欲证明某溶液中含Fe2+而无Fe3+的最佳方案为:先滴加KSCN溶液,再滴加H2O2溶液 |
您最近半年使用:0次
名校
解题方法
4 . 某实验小组探究NiO能否催化NO和CO反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是


 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
A.从理论上推断, 与 与 生成 生成 和 和 的反应,高温有利于自发进行 的反应,高温有利于自发进行 |
B.在空气中加热 可制备NiO 可制备NiO |
C.打开装置1中气球,通过观察气体是否变为红棕色判断是否生成 |
D.若以上实验证明 能够成功催化该反应,且固体A是 能够成功催化该反应,且固体A是 ,则装置2中的反应方程式为: ,则装置2中的反应方程式为: |
您最近半年使用:0次
2022-11-28更新
|
338次组卷
|
5卷引用:重庆2023届拔尖强基联合11月定时检测化学试题
重庆2023届拔尖强基联合11月定时检测化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)重庆市西南大学附属中学校2022-2023学年高三上学期11月拔尖强基联合定时检测化学试题四川外国语大学附属外国语学校2024届高三上学期10月月考化学试题湖北省荆州中学2023-2024学年高三上学期10月半月考化学试题
解题方法
5 . 下列关于铁及其化合物的说法正确的是
A.将NaOH浓溶液滴加到饱和的 溶液中,制备 溶液中,制备 胶体 胶体 |
B. 溶液常用在印刷电路板将Cu氧化成 溶液常用在印刷电路板将Cu氧化成 , , 被还原为Fe 被还原为Fe |
C.某溶液中加KSCN溶液显红色,证明原溶液中有 ,无 ,无 |
D. 浊液露置于空气中,由白色逐步转变为灰绿色,最后变成红褐色 浊液露置于空气中,由白色逐步转变为灰绿色,最后变成红褐色 |
您最近半年使用:0次
名校
6 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.某溶液中加入 , , 层显紫色,证明原溶液中存在 层显紫色,证明原溶液中存在 |
您最近半年使用:0次
2021-09-16更新
|
423次组卷
|
3卷引用:浙江省宁波市镇海中学2020-2021学年高一上学期期末考试化学试卷
名校
解题方法
7 . 某研究小组欲探究 能否与
能否与 溶液反应。
溶液反应。
【查阅资料】
i. 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。
ii. 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。
【提出猜想】
(1)小组同学经过讨论后,认为 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:___________ 。
【设计实验】
(2)实验I:在试管中加入 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液_____ ,小组同学认为 和
和 溶液反应生成了
溶液反应生成了 。
。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是______ 。
重新设计实验:
实验II:在试管中加入 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。
【获得结论】
(4)过氧化氢___________ (填“能”或者“不能”)氧化 。
。
【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入___________ ,产生___________ 。
【总结反思】
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中,___________ ,证明待测液含有 。
。
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意___________ (至少写出两条)对实验结果的影响。
 能否与
能否与 溶液反应。
溶液反应。【查阅资料】
i.
 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。ii.
 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。【提出猜想】
(1)小组同学经过讨论后,认为
 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:【设计实验】
(2)实验I:在试管中加入
 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液 和
和 溶液反应生成了
溶液反应生成了 。
。(3)甲同学注意到盛放
 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是重新设计实验:
实验II:在试管中加入
 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。【获得结论】
(4)过氧化氢
 。
。【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将
 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。(5)补全实验III的方案:在试管中加入
 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入【总结反思】
(6)小组同学经过讨论后,提出了
 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中, 。
。(7)从上述实验中可以得出结论,在物质性质的检验中,应注意
您最近半年使用:0次
2021-11-07更新
|
1003次组卷
|
4卷引用:北京市一零一中2021-2022学年高一上学期期中考试化学试题
解题方法
8 . 长期放置的FeSO4溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶FeSO4溶液进行了如表实验。
I.分别取2mL新制的FeSO4溶液于两支试管中,进行如图实验。
(1)实验i中,现象a是___________ 。
(2)写出实验ii中酸性双氧水参与反应的的离子方程式:___________ 。
II.久置的FeSO4溶液。
(3)为证明FeSO4溶液部分变质,实验iv操作是___________ 。
(4)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验v。
由实验v能否得出___________ (填“能”或“否”)“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
I.分别取2mL新制的FeSO4溶液于两支试管中,进行如图实验。
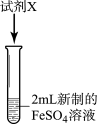 | 实验 | 试剂X | 实验现象 |
| 实验i | 1mL1mol/LNaOH溶液 | 现象a | |
| 实验ii | 依次加入5滴KSCN溶液、5滴酸性双氧水 | 现象b:加入KSCN后无明显现象,加入双氧水后溶液变成红色 |
(1)实验i中,现象a是
(2)写出实验ii中酸性双氧水参与反应的的离子方程式:
II.久置的FeSO4溶液。
| 实验操作 | 实验现象 | 实验结论 | |
| 实验iii | 取少量久置的FeSO4溶液于试管中,向其中滴加5滴KSCN溶液 | 溶液变红 | FeSO4溶液部分变质 |
| 实验iv | |||
(3)为证明FeSO4溶液部分变质,实验iv操作是
(4)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验v。
| 实验操作 | 实验现象 | |
| 实验v | 取一定量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性KMnO4溶液 | 紫色褪去 |
由实验v能否得出
您最近半年使用:0次
9 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近半年使用:0次
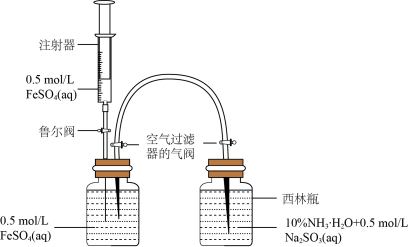
10 . Ⅰ.某小组利用数字化实验模拟制备Fe(OH)2并探究其相关性质。
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是_____ ,Na2SO3的作用是_____ 。
(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化, 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。

对比ab、bc段溶解氧的消耗速率,可以得出什么结论_____ 。
(3)已知:在 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且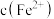 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因_____ ,检验反应后的溶液中是否存在 ,可以选择的试剂是
,可以选择的试剂是_____ 。
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是_____ 。
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是

(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化,
 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。
对比ab、bc段溶解氧的消耗速率,可以得出什么结论
(3)已知:在
 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且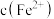 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因 ,可以选择的试剂是
,可以选择的试剂是A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
 |  | 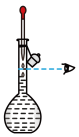 | 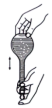 |
| A.称量 | B.转移 | C、定容 | D、摇匀 |
| A.A | B.B | C.C | D.D |
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
您最近半年使用:0次