名校
解题方法
1 . 部分含铁的纯净物的“价-类”关系如图所示。下列叙述错误的是
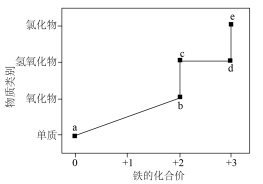
| A.图中相邻物质中c→d在空气里最易转化 | B.在隔绝空气条件下加热 可得到b 可得到b |
C.在高温下a与水蒸气反应生成b和 | D.e溶液中加入铜粉,发生氧化还原反应 |
您最近一年使用:0次
2024-05-18更新
|
168次组卷
|
2卷引用:河北省保定市2024届高三下学期二模化学试题
解题方法
2 . 近日,《国家科学评论》在线发表了南京师范大学陈旭东教授课题组和清华大学李隽教授课题组的合作研究成果,该研究团队完成了具有二十面体结构的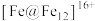 铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
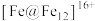 铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
A. 比 比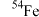 多2个电子 多2个电子 | B.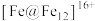 具有还原性 具有还原性 |
| C.Fe位于元素周期表第10纵列 | D.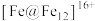 中铁与铁之间存在离子键 中铁与铁之间存在离子键 |
您最近一年使用:0次
3 . Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是___________ 。
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:___________ 。___________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:___________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
①由以上实验可得到的规律是___________ 。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为___________ (填“1.0”“1.5”或“2.0”)mol/L。
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为___________ (任写一条)。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:

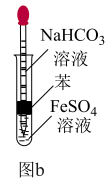
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(NaHCO3)/(mol/L) c(FeSO4)/(mol/L) | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 3.5 min | 9 min | 24 min | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 13 min | 15 min | 22 min | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 | 3 min | 8 min | 30 min | |
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为
您最近一年使用:0次
2024-04-16更新
|
307次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
名校
4 . 下列物质的颜色变化与氧化还原反应无关 的是
| A.浓硝酸久置后,显黄色 |
| B.将SO2通入酸性高锰酸钾溶液中,溶液紫红色褪去 |
| C.新制的白色氢氧化亚铁放置在空气中,最终变为红褐色 |
D.向黄色的铬酸钾(K2CrO4)溶液中加入硫酸,溶液变为橙红色(Cr2O ) ) |
您最近一年使用:0次
2024-02-23更新
|
327次组卷
|
2卷引用:天津市河东区2024年高三下学期一模考试化学试题
解题方法
5 . 过氧化钙 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为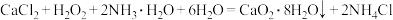 。
。
一、制
I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。
Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制
Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤, 烘干。
烘干。
回答下列问题:
(1)步骤I中使用的主要玻璃仪器有___________ 。
(2)步骤Ⅱ中除去二价铁的相关离子方程式为___________ ;煮沸后需趁热过滤,目的是___________ ;若在该步骤中使用热抽滤漏斗(见下图),比普通过滤的优点是___________ (写两条)。
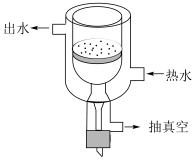
(3)步骤Ⅲ得到的固体主要是___________ (写化学式)。
(4)步骤Ⅳ经“___________ 、过滤、洗涤”,得到纯净固体后加盐酸,如果不进行再次煮沸,可能造成的影响是___________ 。
(5)关于步骤V的操作,下列方案最合理的是___________ (填序号)。
① 溶液
溶液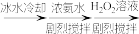
②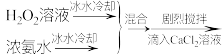
③
 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为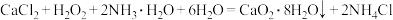 。
。一、制

I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用
 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制

Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤,
 烘干。
烘干。回答下列问题:
(1)步骤I中使用的主要玻璃仪器有
(2)步骤Ⅱ中除去二价铁的相关离子方程式为

(3)步骤Ⅲ得到的固体主要是
(4)步骤Ⅳ经“
(5)关于步骤V的操作,下列方案最合理的是
①
 溶液
溶液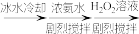
②
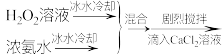
③

您最近一年使用:0次
2024-01-06更新
|
235次组卷
|
2卷引用:2024届四川省成都市高中毕业班第一次诊断性检测理科综合
名校
解题方法
6 . 部分含铁物质及化合价关系如图所示,下列说法错误的是
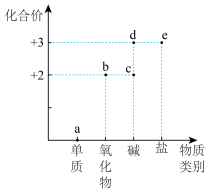

| A.工业上用热还原法冶炼a |
| B.b是黑色固体,在空气中加强热变为红色 |
| C.c可以通过化合反应生成d |
| D.e可以加快H2O2的分解 |
您最近一年使用:0次
2023-06-27更新
|
452次组卷
|
2卷引用:广东省揭阳市普宁市第二中学2020-2021学年高三下学期适应性考试(二)化学试题
解题方法
7 . 如图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系。下列说法正确的是
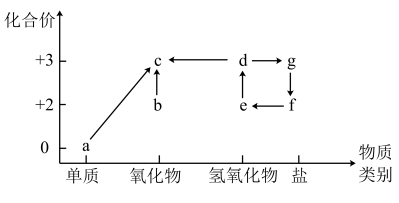

| A.a与水蒸气反应可转化为c |
| B.b是一种黑色粉末,不稳定,在空气中受热,迅速反应转化为c |
| C.e可以通过化合反应制得d |
| D.向g中加强碱溶液可制得胶体 |
您最近一年使用:0次
8 . 下列关于元素及其化合物的性质说法不正确 的是
A.Mg与 反应可生成C 反应可生成C |
B. 与 与 反应可生成 反应可生成 |
C.可通过化合反应制取 |
| D.NaI固体与浓硫酸反应可制取HI |
您最近一年使用:0次
解题方法
9 . 宏观辨识与微观探析是化学学科核心素养之一,下列反应方程式书写错误的是
| A.醋酸除水垢(CaCO3):CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| B.向FeI2溶液中通入少量氯气:2I-+Cl2=2Cl-+I2 |
| C.硫氰化钾检验溶液中是否存在Fe3+:Fe3++3SCN- =Fe(SCN)3↓ |
| D.制备氢氧化亚铁时,白色沉淀会快速变为灰绿色最后变为红褐色的原因:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
您最近一年使用:0次
解题方法
10 . 某固体混合物X可能是由Na2SiO3、Fe、Na2CO3、MgCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计实验方案如图所示(所加试剂均过量)

下列说法不正确的是

下列说法不正确的是
| A.气体A是CO2、H2的混合物 |
| B.沉淀A是H2SiO3 |
| C.根据白色沉淀C是AgCl可知,白色沉淀B一定不是纯净物 |
| D.该固体混合物一定含有Fe、Na2CO3、Na2SiO3 |
您最近一年使用:0次



