1 . 铁及其化合物在生产、生活中有着广泛的应用。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为_______ ,为了将反应后溶液中的Cu2+回收利用,并得到含有一种溶质的溶液,进行的具体操作是_______ 。
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是_______ L(标准状况下)。
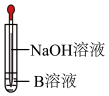
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式_______ 。_______ 。
②酸浸时,Fe3O4与硫酸反应的化学方程式为_______ ;通入O2的目的是_______ 。
③滤渣的成分是_______ (填化学式)。
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量( 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是_______ 。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式
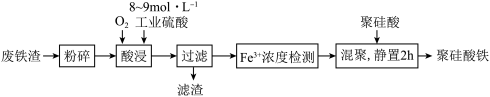
②酸浸时,Fe3O4与硫酸反应的化学方程式为
③滤渣的成分是
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量(
 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
您最近一年使用:0次
名校
解题方法
2 . 高铁酸钾 是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:
是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理: 。
。
(1)胶体分散质粒子的直径范围是_________ 。该反应中 是
是_________ 。
A.还原剂 B.氧化剂 C.被还原 D.被氧化
(2) 能杀灭水中细菌的原因是
能杀灭水中细菌的原因是___________ 。
(3)配平湿法制高铁酸钾的离子反应方程式_________ 。
___________Fe(OH)3+___________ClO-+__________ ___________
___________ +___________
+___________ + ___________。
+ ___________。
 是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:
是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理: 。
。(1)胶体分散质粒子的直径范围是
 是
是A.还原剂 B.氧化剂 C.被还原 D.被氧化
(2)
 能杀灭水中细菌的原因是
能杀灭水中细菌的原因是(3)配平湿法制高铁酸钾的离子反应方程式
___________Fe(OH)3+___________ClO-+__________
 ___________
___________ +___________
+___________ + ___________。
+ ___________。
您最近一年使用:0次
名校
解题方法
3 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价—类”二维图。铁元素的“价—类”二维图如图所示,下列说法正确的是
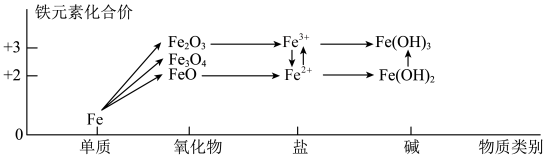
| A.高温条件下Fe和水蒸气反应生成Fe(OH)2和H2,该反应为置换反应 |
| B.FeO在加热的条件下能被氧气氧化成Fe3O4 |
| C.将饱和的FeCl3溶液加热煮沸可制得氢氧化铁胶体 |
| D.Fe(OH)2浊液露置于空气中,由白色立即变为红褐色 |
您最近一年使用:0次
2024-04-26更新
|
99次组卷
|
2卷引用:江西省宜春市丰城中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
4 . 各物质的转化关系如下图所示,请完成下列空白。
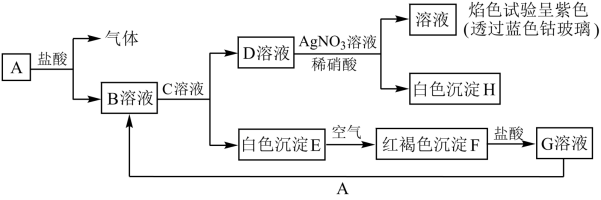
(1)写出B和D 的化学式:B___________ ;D___________ 。
(2)写出E F的化学方程式:
F的化学方程式:___________ 。
(3)向G溶液中加入A,写出反应的离子方程式___________ 。
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子___________ 。

(1)写出B和D 的化学式:B
(2)写出E
 F的化学方程式:
F的化学方程式:(3)向G溶液中加入A,写出反应的离子方程式
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子
您最近一年使用:0次
5 . 下列化合物中不能由化合反应直接制得的是
| A.CuCl2 | B.FeCl2 | C.Fe(OH)2 | D.Fe(OH)3 |
您最近一年使用:0次
6 . 以下流程中涉及的物质均为中学化学常见物质,其中白色固体A为一种常见的钠盐,混合气体C可使澄清石灰水变浑浊,白色固体F在空气中易迅速变为灰绿色,黑色固体H有磁性。

请回答下列问题:
(1)白色固体E的化学式为___________ ;黑色固体H的化学式为___________ ;无色气体I的化学式为___________ 。
(2)无色混合气体C的组成为___________ 。
(3)白色固体A与少量澄清石灰水反应的离子方程式为___________ 。
(4)白色固体F无氧常温条件下分解的化学方程式为___________ 。
(5)请设计实验验证黑色固体H中金属元素的化合价___________ 。

请回答下列问题:
(1)白色固体E的化学式为
(2)无色混合气体C的组成为
(3)白色固体A与少量澄清石灰水反应的离子方程式为
(4)白色固体F无氧常温条件下分解的化学方程式为
(5)请设计实验验证黑色固体H中金属元素的化合价
您最近一年使用:0次
7 . 下列说法正确的是
| A.FeSO4和Fe(OH)3可以通过化合反应生成 |
| B.50mL0.5mol/LKCl溶液中的Cl-浓度小于100mL0.2mol/LMgCl2溶液 |
| C.将Na、Mg各0.2mol分别与含0.1molHCl的盐酸反应,产生气体体积比为1∶1 |
| D.将40gNaOH固体溶于1L水,所得NaOH溶液物质的量浓度为1mol/L |
您最近一年使用:0次
名校
解题方法
8 . 氧化还原反应与四种基本类型的关系如图所示,则下列化学反应属于阴影部分的是


A. |
B.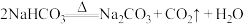 |
C.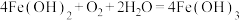 |
D.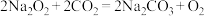 |
您最近一年使用:0次
2024-01-04更新
|
132次组卷
|
23卷引用:广东省普宁市第二中学2021-2022学年高一上学期期中考试化学试题
广东省普宁市第二中学2021-2022学年高一上学期期中考试化学试题湖南省邵阳市第二中学2021-2022学年高一上学期期中考试化学试题(已下线)【2022】【高一上】【期中考】【杭九】【高中化学】【赵优萍收集】广东实验中学附属江门学校2022-2023学年高一上学期期中考试化学试题广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题北京市北京师范大学附属实验中学2021-2022学年高一上学期期中考试化学试题河北省石家庄卓越中学2023-2024学年高一上学期期中考试化学试题广东省珠海市第四中学2023-2024学年高一上学期期中考试化学试卷浙江省金华市云富高级中学2020-2021学年高一上学期第一次月考化学试题浙江省金华市第八中学2021-2022学年高一上学期9月月考卷化学试题河北省张家口市宣化第一中学2021-2022学年高一上学期期初考试化学试题浙江省台州市书生中学2021-2022学年高一上学期第一次月考化学试题甘肃省天水市田家炳中学2021-2022学年高一上学期第一阶段考试化学试卷(已下线)第07练 氧化还原反应-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)(已下线)衔接点11 氧化还原反应概念-2022年初升高化学无忧衔接?(已下线)第一章 物质及其变化(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)四川省绵阳市南山中学2022-2023学年高一上学期12月线上测试化学试题江苏省苏州工业园区星海实验高级中学2023-2024学年高一上学期10月月考化学试题云南会泽县实验高级中学校2023-2024学年高一上学期10月月考化学试题广西钦州市第四中学2023-2024学年高一上学期11月考试化学试卷云南省曲靖市罗平县第一中学2023-2024学年高一上学期9月月考化学试题云南省宣威市东升实验中学2023-2024学年高一上学期11月月考化学试题山东省济宁市微山县第二中学2023-2024学年高一上学期12月月考化学试题
9 . 实验是检验真理的唯一标准。下列叙述正确的是
A. 溶液中滴加 溶液中滴加 溶液,立刻生成红褐色沉淀 溶液,立刻生成红褐色沉淀 |
| B.自由移动离子数目多的溶液导电性一定比数目少的溶液强 |
| C.分别向装有干燥的和潮湿的有色纸条的集气瓶中通入干燥的氯气,有色布条均褪色 |
| D.若容量瓶中有少量蒸馏水,配制一定物质的量浓度的溶液时,对实验无影响 |
您最近一年使用:0次
10 . 化学研究源于实验与理论的结合,得益于科学的推断与探究。
(1)一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
②工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有___________ 性。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为: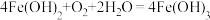 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是___________ 。
(3)某化学兴趣小组用食品脱氧剂( 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。
实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是___________ (写离子符号)。
②检验溶液丙中 的方案是
的方案是___________ 。
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)
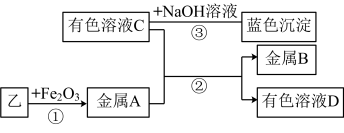
写出反应②的离子方程式___________ ,若反应消耗 金属A,转移电子的数目为
金属A,转移电子的数目为___________ 。
(1)一个体重
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
②工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:
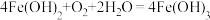 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是(3)某化学兴趣小组用食品脱氧剂(
 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是
②检验溶液丙中
 的方案是
的方案是③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)

写出反应②的离子方程式
 金属A,转移电子的数目为
金属A,转移电子的数目为
您最近一年使用:0次



