名校
1 . 中学化学中的氯水和氨水是非常重要的两种“水”,下列说法正确的是
A.氯水具有漂白性,为增加其漂白效果,可向其中通入少量 |
B.向 溶液中滴加新制氯水,观察产生淡黄色沉淀,可证明非金属性: 溶液中滴加新制氯水,观察产生淡黄色沉淀,可证明非金属性: |
C.氨水是一元弱碱,其中只存在两种分子 和 和 |
| D.可用玻璃棒蘸取浓氨水靠近收集氯化氢的试管口,可看到产生白雾 |
您最近半年使用:0次
名校
解题方法
2 . 下列关于氨水的叙述正确的是
| A.氨水显碱性,是因为氨气是一种弱碱 |
| B.氨水和液氨成分相同 |
| C.氨水中物质的量浓度最大的粒子是NH3(除水外) |
D.1mol•L-1的氨水指在1L溶液中含NH3、NH3•H2O、NH 物质的量之和为1mol 物质的量之和为1mol |
您最近半年使用:0次
2024-03-28更新
|
437次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
解题方法
3 . NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温下,pH=1的硫酸溶液中,含有H+数目为0.1NA |
| B.常温下,1 L 0.5 mol·L-1的AlCl3溶液中,含有Al3+数目为0.5NA |
| C.常温下,1 L pH=12的CH3COONa溶液,由水电离产生的OH-数目为0.01NA |
| D.标准状况下,4.48 L NH3溶于水得到的溶液中,NH3·H2O的总数为0.2NA |
您最近半年使用:0次
解题方法
4 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中含有的中子数为 中含有的中子数为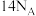 |
B. 与足量的 与足量的 反应,转移电子数为 反应,转移电子数为 |
C. 质量分数为 质量分数为 的 的 溶液中 溶液中 原子数目为 原子数目为 |
D.标准状况下,将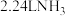 溶于足量水中,溶液中 溶于足量水中,溶液中 与 与 两种微粒数之和等于 两种微粒数之和等于 |
您最近半年使用:0次
名校
解题方法
5 . 分类是科学研究的重要方法,下列物质分类正确的是
| A.化合物:干冰,冰水混合物,碱石灰,小苏打,氨水 |
| B.非电解质:乙醇,二氧化碳,液氯,氨气,葡萄糖 |
| C.碱性氧化物:氧化铁,氧化铝,过氧化钠,生石灰,氧化镁 |
| D.混合物:纯净矿泉水,漂白粉,石灰石,天然气,盐酸 |
您最近半年使用:0次
解题方法
6 . 过氧化钙 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为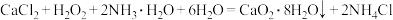 。
。
一、制
I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。
Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制
Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤, 烘干。
烘干。
回答下列问题:
(1)步骤I中使用的主要玻璃仪器有___________ 。
(2)步骤Ⅱ中除去二价铁的相关离子方程式为___________ ;煮沸后需趁热过滤,目的是___________ ;若在该步骤中使用热抽滤漏斗(见下图),比普通过滤的优点是___________ (写两条)。
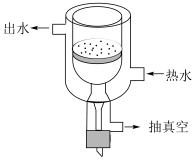
(3)步骤Ⅲ得到的固体主要是___________ (写化学式)。
(4)步骤Ⅳ经“___________ 、过滤、洗涤”,得到纯净固体后加盐酸,如果不进行再次煮沸,可能造成的影响是___________ 。
(5)关于步骤V的操作,下列方案最合理的是___________ (填序号)。
① 溶液
溶液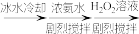
②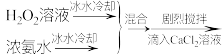
③
 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为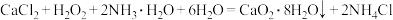 。
。一、制

I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用
 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制

Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤,
 烘干。
烘干。回答下列问题:
(1)步骤I中使用的主要玻璃仪器有
(2)步骤Ⅱ中除去二价铁的相关离子方程式为

(3)步骤Ⅲ得到的固体主要是
(4)步骤Ⅳ经“
(5)关于步骤V的操作,下列方案最合理的是
①
 溶液
溶液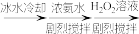
②
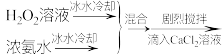
③

您最近半年使用:0次
2024-01-06更新
|
219次组卷
|
2卷引用:2024届四川省成都市高中毕业班第一次诊断性检测理科综合
名校
7 . 下列几组溶液的导电性变化与图像一致的是
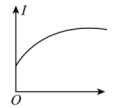

A.向 溶液中加入少量 溶液中加入少量 固体 固体 | B.向 溶液中通入少量 溶液中通入少量 |
C.向氨水中通入 直至过量 直至过量 | D.向 溶液中通入 溶液中通入 至过量 至过量 |
您最近半年使用:0次
8 . 下列关于氨水的说法不正确的是
| A.氨水和液氨不同,氨水是由多种粒子构成的,液氨的组成中只有氨分子 |
| B.氨水中物质的量浓度最大的粒子是NH3·H2O(除水外) |
| C.氨水显弱碱性,故通常保存在金属容器中 |
D.在1 mol·L-1氨水中,NH3·H2O、 、NH3的物质的量浓度之和为1 mol·L-1 、NH3的物质的量浓度之和为1 mol·L-1 |
您最近半年使用:0次
9 . 清代《本草纲目拾遗》中关于“鼻冲水(氨水)”的记载明确指出:“鼻冲水,∙∙∙∙∙∙贮以玻璃瓶,紧塞其口,勿使泄气,则药方不减∙∙∙∙∙∙唯以此水瓶口对鼻吸其气,即遍身麻颤出汗而愈,虚弱者忌之。宜外用,勿服。”下列有关“鼻冲水”的推断不正确的是
| A.鼻冲水是弱碱 |
| B.鼻冲水滴入酚酞溶液中,溶液变红色 |
| C.鼻冲水中含有分子和离子的种类为6种 |
D.存在平衡:NH3+H2O NH3·H2O NH3·H2O  +OH- +OH- |
您最近半年使用:0次
10 . 每年10月23日被誉为“摩尔日”。设NA为阿伏加德罗常数的值,下列说法正确的是
A.将1.7gNH3溶于1L水,形成的溶液中NH3·H2O和 的数目之和为0.1NA 的数目之和为0.1NA |
| B.SiO2与足量的焦炭反应,生成1mol气体时转移的电子数为2NA |
| C.标准状况下,22.4L己烷中含非极性键的数目为5NA |
| D.加热条件下,含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数等于0.1NA |
您最近半年使用:0次



