1 . 人类的生产和生活都离不开金属。
(一)金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图所示:
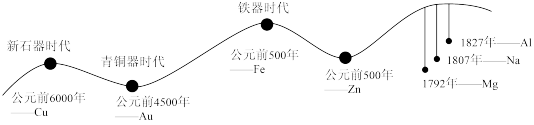
(1)由图可知人类最早使用的合金是___________ ;通过敲打可将金属材料打制成不同的形状,是利用了金属的___________ 性。
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾(硫酸铜晶体),熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是___________ (填序号)
A.“苦泉”的溶质之一——CuSO4
B.“挹其水之”——蒸发溶剂
C.“熬胆矾铁釜,久之亦化为铜”——发生置换反应
(3)铝的利用距今100多年,现在铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是________ (用化学方程式表示)
(二)实验室探究铜的冶炼
已知: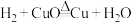 。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
I、设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。

(4)图1中制取氢气的化学反应方程式为____________________________________________ 。
(5)实验开始时,___________ (填序号)
A.先向长颈漏斗中加稀硫酸后点酒精灯 B.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
(6)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到___________ ,证明固体产物有Cu2O。
II、探究反应生成Cu2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。
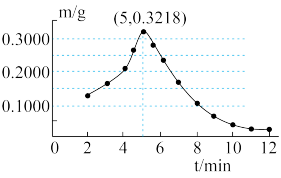
(7)由图2可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是____________ 。
(8)为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是___________ 。
III、探究反应生成Cu2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1:经历 ,
, 两个反应,且在同一条件下两个反应同时进行。
两个反应,且在同一条件下两个反应同时进行。
假设2:依次经历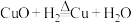 、
、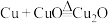 、
、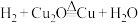 三个反应。
三个反应。
(9)结合探究II的结果,通过计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是___________________ 。(写出合理的推理过程)
(三)用废铜屑生产硫酸铜晶体(CuSO4∙5H2O)的流程如下:
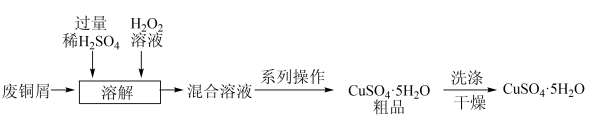
(10)“溶解”时发生的化学反应方程式为___________________ 。
(11)“洗涤、干燥”过程中常用95%的酒精做洗涤剂,优点是_________ 。
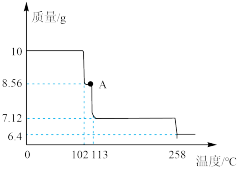
(12)取10g CuSO4∙5H2O,其受热脱水过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示。则晶体CuSO4∙3H2O存在的最高温度约为___________ 。
(一)金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图所示:

(1)由图可知人类最早使用的合金是
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾(硫酸铜晶体),熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是
A.“苦泉”的溶质之一——CuSO4
B.“挹其水之”——蒸发溶剂
C.“熬胆矾铁釜,久之亦化为铜”——发生置换反应
(3)铝的利用距今100多年,现在铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是
(二)实验室探究铜的冶炼
已知:
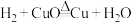 。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。I、设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。

(4)图1中制取氢气的化学反应方程式为
(5)实验开始时,
A.先向长颈漏斗中加稀硫酸后点酒精灯 B.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
(6)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到
II、探究反应生成Cu2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。

(7)由图2可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是
(8)为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是
III、探究反应生成Cu2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1:经历
 ,
, 两个反应,且在同一条件下两个反应同时进行。
两个反应,且在同一条件下两个反应同时进行。假设2:依次经历
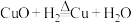 、
、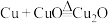 、
、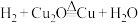 三个反应。
三个反应。(9)结合探究II的结果,通过计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是
(三)用废铜屑生产硫酸铜晶体(CuSO4∙5H2O)的流程如下:

(10)“溶解”时发生的化学反应方程式为
(11)“洗涤、干燥”过程中常用95%的酒精做洗涤剂,优点是
(12)取10g CuSO4∙5H2O,其受热脱水过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示。则晶体CuSO4∙3H2O存在的最高温度约为

您最近一年使用:0次
名校
2 . 柠檬酸因具有酸性和较好的络合性,可用于浸出金属离子并得到柠檬酸浸出液。下图是从柠檬酸浸出液中分离出铜并制备碱式碳酸铜: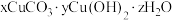 的流程
的流程

实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
则下列说法不正确的是
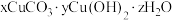 的流程
的流程
实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜
 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。则下列说法不正确的是
A.经过计算碱式碳酸铜的化学式组成为 |
| B.调pH分离铜时,因Cu2+与柠檬酸根形成配合物,则与OH-形成Cu(OH)2减少 |
C.抗坏血酸还原Cu(OH)2的化学反应方程式为: |
| D.温度超过80℃时,因抗坏血酸受热易分解,使浓度降低,还原铜的能力减弱 |
您最近一年使用:0次
名校
解题方法
3 . 取一定量胆矾晶体(CuSO4·5H2O)加热分解,固体残留率( ) 随温度的变化如图所示:
) 随温度的变化如图所示:
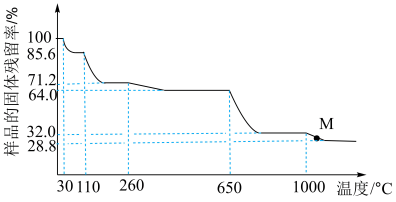
下列说法中不正确的是
 ) 随温度的变化如图所示:
) 随温度的变化如图所示:
下列说法中不正确的是
| A.110°C 时的晶体化学式 CuSO4·3H2O |
B.260°C~ 650°C 过程中的反应方程式为CuSO4·H2O CuSO4+H2O CuSO4+H2O |
| C.已知 650°C 加热至 1000°C ,产物为一种固体与一种气体, 则气体为SO2 |
| D.M 点所得固体是 CuO 与 Cu2O 的混合物 |
您最近一年使用:0次
4 . 宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料,其主要成分为CuCO3•Cu(OH)2,下列说法中错误的是
| A.孔雀石颜料中含有重金属离子,使用时勿入口中 |
| B.孔雀石颜料耐酸和碱腐蚀 |
| C.孔雀石颜料不易被空气氧化 |
| D.保存《千里江山图》需控制温度和湿度 |
您最近一年使用:0次
2022-07-10更新
|
681次组卷
|
6卷引用:2022年江苏卷高考真题变式题1-13
(已下线)2022年江苏卷高考真题变式题1-132020年辽宁省普通高中合格性考试(7月份 ) 化学试题(已下线)易错点02 化学与STSE-备战2023年高考化学考试易错题宁夏六盘山高级中学2022-2023学年高一下学期学业水平合格性考试化学模拟试题(已下线)专题十 金属材料(已下线)合格考真题汇编8金属元素及其化合物二
5 . 化工行业常用硒(Se)作催化剂,该催化剂具有反应条件温和、成本低、环境污染小、用后处理简便等优点。以铜阳极泥(主要成分为Cu2Se、Ag2Se,还含有少量Ag、Au、Pt等)为原料制备纯硒的工艺流程如图。

已知:①“净化除杂”时采用真空蒸馏的方法提纯硒(沸点为685℃);
②焙烧后,Cu、Ag均以硫酸盐形式存在, ;
;
③“浸出液”中溶质的饱和浓度不小于0.01 。
。
下列说法错误的是

已知:①“净化除杂”时采用真空蒸馏的方法提纯硒(沸点为685℃);
②焙烧后,Cu、Ag均以硫酸盐形式存在,
 ;
;③“浸出液”中溶质的饱和浓度不小于0.01
 。
。下列说法错误的是
| A.“加硫酸并焙烧”时使用的硫酸应为浓硫酸 |
| B.“水吸收”过程得到的溶液呈酸性 |
| C.在实验室蒸馏时,需要用到直形冷凝管 |
| D.“浸出液”中的溶质成分不可能含有Ag2SO4 |
您最近一年使用:0次
2021-04-09更新
|
819次组卷
|
4卷引用:江苏省常熟市2021-2022学年高三上学期阶段性抽测二化学试题
名校
解题方法
6 . 工业电解精炼铜的溶液中含有Zn2+、Cu2+等离子,实验室设计分离出Zn2+并制取胆矾的流程如下:
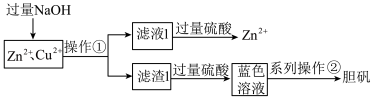
已知:Zn2+与NaOH的反应与Al3+类似。下列说法错误的是

已知:Zn2+与NaOH的反应与Al3+类似。下列说法错误的是
A.滤液1与过量硫酸反应的离子方程式为ZnO +4H+=Zn2++2H2O +4H+=Zn2++2H2O |
| B.操作①和②中用到的玻璃仪器完全相同 |
| C.系列操作②包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| D.可用无水乙醇洗涤胆矾晶体,除去表面的杂质 |
您最近一年使用:0次
2020-11-01更新
|
507次组卷
|
7卷引用:江苏省连云港市赣榆智贤中学2020-2021学年高二3月月考化学试题
江苏省连云港市赣榆智贤中学2020-2021学年高二3月月考化学试题湖南省永州市2021届高三第一次模拟化学试题(已下线)热点5 常见元素及其化合物的性质与应用-2021年高考化学专练【热点·重点·难点】(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)河南省南阳市第一中学校2021-2022学年高三上学期第二次月考化学试题广东省广州市第一中学2021-2022学年高三下学期2月教学质量监测化学试题(已下线)第一部分 二轮专题突破 专题17 典型实验装置及化学实验基本操作
2010·江苏泰州·一模
7 . 已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的10 mol∙L−1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
| A.该反应显示硫酸具有酸性 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.反应中硫酸作氧化剂 |
您最近一年使用:0次
12-13高三上·陕西咸阳·期末
8 . 有一铁粉和氧化铜的混合物6.96g,进行如下实验:
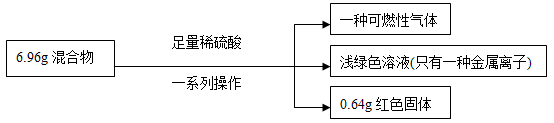
根据实验所得数据,关于混合物相关说法正确的是

根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
您最近一年使用:0次



