名校
1 . 学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
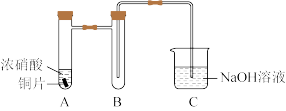
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为______ ,装置B的作用为______ 。
(2)铜与过量 反应的探究如下:
反应的探究如下:

实验②中Cu溶解的离子方程式为______ ;产生的气体为______ 。比较实验①和②,从氧化还原角度说明H⁺的作用是______ 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,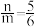 。X的化学式为
。X的化学式为______ 。
(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量______ %。
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为

(2)铜与过量
 反应的探究如下:
反应的探究如下:
实验②中Cu溶解的离子方程式为
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,
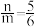 。X的化学式为
。X的化学式为(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L

 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量
您最近一年使用:0次
2 . 碳粉、CO、H2均可作为实验室还原CuO的还原剂,实验小组对CuO的还原反应及还原产物组成进行探究。
查阅资料:
I .CuO还原反应中相关信息如表所示:
II .CuO高温分解生成Cu2O,Cu2O+2H+=Cu+Cu2++H2O;
II .PdCl2溶液能吸收CO,生成黑色Pd沉淀和一种氢化物、一种氧化物。
回答下列问题:
(1)实验室还原CuO适宜选用的还原剂为_______ ,理由为_______ 。
(2)小组同学用如图所示装置探究碳粉与CuO反应的产物。

①仪器a的名称为_______ 。
②试剂X的作用为_______ 。
③若气体产物中含有CO,则观察到的现象为_______ ;其中反应的化学方程式为_______ 。
(3)某小组同学为测定碳粉还原CuO后固体混合物中单质Cu的质量分数,设计如下实验:准确称取反应管中残留固体8.000g,溶于足量稀硝酸,过滤、洗涤、干燥,所得沉淀的质量为0.160 g;将洗涤液与滤液合并,配成500mL溶液;量取所配溶液25.00mL,加入适当过量的KI溶液;以淀粉为指示剂,用0.500 0 mol·L-1 Na2S2O3标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为12.00mL。已知:2Cu2++5I-=2CuI↓+ ,
, +2
+2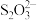 =
=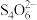 +3I-。
+3I-。
①溶解样品时,不能用稀硫酸代替稀硝酸的原因为_______ .。
②通过计算说明还原产物中是否含有Cu2O:_______ 。
③若CuI吸附部分 ,会导致所测Cu单质的质量分数
,会导致所测Cu单质的质量分数_______ .(填“偏大”“偏小”或“无影响”)。
查阅资料:
I .CuO还原反应中相关信息如表所示:
| 还原剂 | 反应温度/℃ | 产物性状 |
| 碳粉 | >800 | 可能混有砖红色固体或黑色固体 |
| CO | >500 | 可能混有砖红色固体 |
| H2 | 300左右 | 紫红色固体 |
II .PdCl2溶液能吸收CO,生成黑色Pd沉淀和一种氢化物、一种氧化物。
回答下列问题:
(1)实验室还原CuO适宜选用的还原剂为
(2)小组同学用如图所示装置探究碳粉与CuO反应的产物。

①仪器a的名称为
②试剂X的作用为
③若气体产物中含有CO,则观察到的现象为
(3)某小组同学为测定碳粉还原CuO后固体混合物中单质Cu的质量分数,设计如下实验:准确称取反应管中残留固体8.000g,溶于足量稀硝酸,过滤、洗涤、干燥,所得沉淀的质量为0.160 g;将洗涤液与滤液合并,配成500mL溶液;量取所配溶液25.00mL,加入适当过量的KI溶液;以淀粉为指示剂,用0.500 0 mol·L-1 Na2S2O3标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为12.00mL。已知:2Cu2++5I-=2CuI↓+
 ,
, +2
+2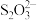 =
=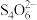 +3I-。
+3I-。①溶解样品时,不能用稀硫酸代替稀硝酸的原因为
②通过计算说明还原产物中是否含有Cu2O:
③若CuI吸附部分
 ,会导致所测Cu单质的质量分数
,会导致所测Cu单质的质量分数
您最近一年使用:0次
3 . 氯化亚铜( )广泛应用于化工、印染、电镀等行业。
)广泛应用于化工、印染、电镀等行业。 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是
难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是 和少量
和少量 )为原料,采用硝酸铵(受热到一定温度时,易分解)氧化分解技术生产
)为原料,采用硝酸铵(受热到一定温度时,易分解)氧化分解技术生产 的工艺过程如图:
的工艺过程如图:
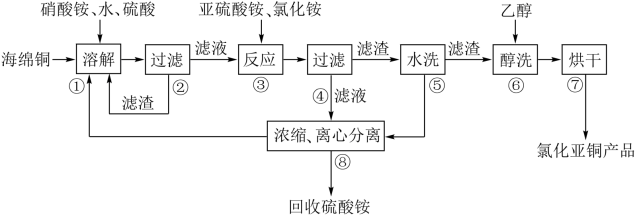
(1)步骤①中主要反应的离子方程式_______ ,步骤③中主要反应的离子方程式_______ ,溶解温度应控制在60-70℃,原因是_______ 。
(2)步骤⑤包括用 的酸洗、水洗两步操作,酸洗应采用的酸及原因是
的酸洗、水洗两步操作,酸洗应采用的酸及原因是_______ 。
(3)工艺流程中,步骤⑥醇洗的目的是_______ 。
(4)准确称取所制备的氯化亚铜样品10.0g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,用0.5
溶液中,待样品完全溶解后,加入适量稀硫酸,用0.5 的
的 溶液滴定到终点,消耗
溶液滴定到终点,消耗 溶液36
溶液36 。滴定时反应的离子方程式为
。滴定时反应的离子方程式为_______ ,样品中 的质量分数为
的质量分数为_______ 。(本题中 的原子量为36,另不考虑
的原子量为36,另不考虑 与
与 的反应)
的反应)
 )广泛应用于化工、印染、电镀等行业。
)广泛应用于化工、印染、电镀等行业。 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是
难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是 和少量
和少量 )为原料,采用硝酸铵(受热到一定温度时,易分解)氧化分解技术生产
)为原料,采用硝酸铵(受热到一定温度时,易分解)氧化分解技术生产 的工艺过程如图:
的工艺过程如图:
(1)步骤①中主要反应的离子方程式
(2)步骤⑤包括用
 的酸洗、水洗两步操作,酸洗应采用的酸及原因是
的酸洗、水洗两步操作,酸洗应采用的酸及原因是(3)工艺流程中,步骤⑥醇洗的目的是
(4)准确称取所制备的氯化亚铜样品10.0g,将其置于过量的
 溶液中,待样品完全溶解后,加入适量稀硫酸,用0.5
溶液中,待样品完全溶解后,加入适量稀硫酸,用0.5 的
的 溶液滴定到终点,消耗
溶液滴定到终点,消耗 溶液36
溶液36 。滴定时反应的离子方程式为
。滴定时反应的离子方程式为 的质量分数为
的质量分数为 的原子量为36,另不考虑
的原子量为36,另不考虑 与
与 的反应)
的反应)
您最近一年使用:0次
4 . 宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。下列说法错误的是
| A.保存《千里江山图》需控制温度和湿度 |
| B.孔雀石、蓝铜矿颜料不易被空气氧化 |
| C.孔雀石、蓝铜矿颜料耐酸耐碱 |
| D.Cu(OH)2·CuCO3中铜的质量分数高于Cu(OH)2·2CuCO3 |
您最近一年使用:0次
2020-07-09更新
|
18233次组卷
|
76卷引用:山东省临沂市莒南第二中学2021届高三10月月考化学试题
山东省临沂市莒南第二中学2021届高三10月月考化学试题山东省泰安市宁阳一中2021届高三上学期模块考试化学试题(已下线)热点2 化学与传统文化-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第01题 化学与STSE、传统文化-备战2021年高考化学临考题号押题(山东卷)山东省青岛莱西市2020-2021学年高二下学期期末考试(第四次考试)化学试题2020年全国统一考试化学试题(新课标Ⅲ)(已下线)专题01 STSE 化学用语-2020年高考真题和模拟题化学分项汇编(已下线)第01章 物质及其变化(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)广东惠州市华罗庚中学2021届高三9月月考化学试题河南省三门峡市第一高级中学2021届高三8月开学考试化学试题四川省绵阳南山中学2020-2021学年高二上学期开学考试化学试题黑龙江省哈尔滨市尚志市尚志中学2021届高三10月月考化学试题福建省厦门实验中学2021届高三上学期十月份月考化学试题(已下线)【南昌新东方】3. 南昌一中 余贞梅(已下线)【浙江新东方】32北京首都师范大学第二附属中学2021届高三9月月考化学试题吉林省汪清县第六中学2021届高三第三次月考模拟化学试题福建省福州市第一中学2021届高三上学期开学质检化学试题河北省尚义县第一中学2021届高三上学期期中考试化学试题湖南省宁乡市第一高级中学2021届高三上学期11月摸底考试化学试题重庆市万州新田中学2020-2021学年高一上学期第二次月考化学试题重庆市第七中学2021届高三上学期期中化学试题河南省洛阳市第一高级中学2020-2021学年高一上学期12月月考化学试题(已下线)热点2 化学与传统文化-2021年高考化学专练【热点·重点·难点】宁夏海原县第一中学2021届高三上学期期末考试化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题(已下线)专题01 物质的组成、性质和分类——备战2021年高考化学纠错笔记(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练广东省梅州市五华县五华中学2021届高三2月测练化学试题(已下线)小题01 化学与传统文化——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第7题 化学与社会生产生活-备战2021年高考化学临考题号押题(课标全国卷)广西桂林市第十八中学2020-2021学年高一下学期期中考试化学试题陕西省西安市庆华中学2020-2021学年高三上学期第二次月考化学试题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省益阳市箴言中学2021-2022学年高一上学期10月月考化学试题 江西省宜春市第九中学2021-2022学年高三上学期10月月考化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高一上学期第一次月考化学试题(已下线)专题讲座(七) STSE与 化学可持续发展(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题01 化学与STSE—2022年高考化学二轮复习讲练测-讲义(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)2020年全国卷Ⅲ化学真题变式题(已下线)卷01 化学与传统文化-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)押全国卷理综第7题 化学与社会生产生活及传统文化-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点01 化学与STSE与传统文化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题01STSE化学用语-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题01STSE化学用语-五年(2018~2022)高考真题汇编(全国卷)(已下线)第01练 化学与科技社会生产生活、传统文化-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)微专题01 “话”中有“化”—化学与传统文化-备战2023年高考化学一轮复习考点微专题(已下线)微专题15 铜及其化合物的性质、制备与实验探究-备战2023年高考化学一轮复习考点微专题(已下线)第10讲 金属材料及金属矿物的开发利用(练)-2023年高考化学一轮复习讲练测(全国通用)陕西省榆林市神木中学、府谷中学和绥德中学2021-2022学年高二下学期期末考试化学试题河南省信阳高级中学2021-2022学年高一下学期期末考试化学试题云南省昆明第一中学2022-2023学年高一上学期入学考试化学试题重庆南开中学2022-2023学年高一上学期入学考试化学试题安徽省安庆市第一中学2022-2023学年高一上学期期中考试化学试题福建省厦门集美中学2022-2023学年高三上学期期中考试化学试题(已下线)专题二 化学与STSE-实战高考·二轮复习核心突破福建省厦门市国祺中学2021-2022学年高三上学期期中考试化学试题甘肃省张掖市2022-2023学年高一上学期适应性模拟考试化学试题(已下线)专题01 物质的组成与分类 传统文化-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题7 化学与传统文化第三章 金属及其化合物 第15讲 金属材料 金属冶炼(已下线)题型37 含铜化合物的性质及其之间的转化流程(已下线)题型1 传统文化-高考必备50个题型(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)宁夏石嘴山市平罗中学2022-2023学年高三上学期11月期中考试化学试题陕西省咸阳市实验中学2023-2024学年高一上学期段性检测(一)化学试题陕西省延安市延川县中学2023-2024学年高一上学期第一次月考化学试题江西省宜春市上高二中2023-2024学年高三上学期第一次月考化学试题上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
名校
解题方法
5 . 氯化亚铜(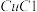 )在化工、印染、电镀等行业应用广泛。
)在化工、印染、电镀等行业应用广泛。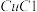 微溶于水,不溶于醇和稀酸,可溶于
微溶于水,不溶于醇和稀酸,可溶于 浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量
浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量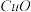 )为原料,采用硝酸铵氧化分解技术生产
)为原料,采用硝酸铵氧化分解技术生产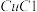 的工艺过程如图。回答下列问题:
的工艺过程如图。回答下列问题:

(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式______________ 。
(2)步骤②中,亚硫酸铵要略保持过量,原因是___________ ,滤液中可循环利用的物质是__________ 。
(3)步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为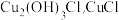 被氧化为
被氧化为 的化学方程式为
的化学方程式为______________________ 。
(4)用 溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品
溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品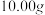 ,将其置于过量的
,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸配成
溶液中,待样品完全溶解后,加入适量稀硫酸配成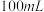 溶液,取溶液
溶液,取溶液 用
用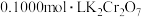 溶液进行滴定,反应中
溶液进行滴定,反应中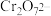 被还原成
被还原成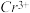 ,相关数据记录如表所示:该样品中
,相关数据记录如表所示:该样品中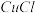 的质量分数
的质量分数__________________ 。
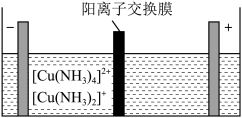
(5)制造印刷电路板产生的废液中含大量 等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到
等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到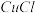 ,电解时阴极的电极反应式为
,电解时阴极的电极反应式为___________ ,生成 的离子方程式为
的离子方程式为________________________________ 。
 )在化工、印染、电镀等行业应用广泛。
)在化工、印染、电镀等行业应用广泛。 微溶于水,不溶于醇和稀酸,可溶于
微溶于水,不溶于醇和稀酸,可溶于 浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量
浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量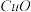 )为原料,采用硝酸铵氧化分解技术生产
)为原料,采用硝酸铵氧化分解技术生产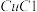 的工艺过程如图。回答下列问题:
的工艺过程如图。回答下列问题:
(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式
(2)步骤②中,亚硫酸铵要略保持过量,原因是
(3)步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为
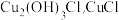 被氧化为
被氧化为 的化学方程式为
的化学方程式为(4)用
 溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品
溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品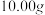 ,将其置于过量的
,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸配成
溶液中,待样品完全溶解后,加入适量稀硫酸配成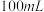 溶液,取溶液
溶液,取溶液 用
用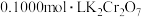 溶液进行滴定,反应中
溶液进行滴定,反应中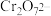 被还原成
被还原成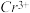 ,相关数据记录如表所示:该样品中
,相关数据记录如表所示:该样品中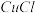 的质量分数
的质量分数| 实验编号 | 1 | 2 | 3 |
消耗 溶液的体积/mL 溶液的体积/mL | 14.98 | 16.03 | 15.02 |
 等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到
等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到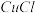 ,电解时阴极的电极反应式为
,电解时阴极的电极反应式为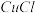 的离子方程式为
的离子方程式为
您最近一年使用:0次
2020-03-28更新
|
353次组卷
|
3卷引用:山东省六地市部分学校2020届高三下学期3月2日线上考试化学试题
山东省六地市部分学校2020届高三下学期3月2日线上考试化学试题山东省实验中学2020届高三线上诊断测试化学试题(已下线)考点17 化工生产诸要素及流程图分析-2020年高考化学命题预测与模拟试题分类精编



