解题方法
1 . 氧化亚铜 可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将
可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将 和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知:
和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知: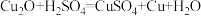 。请计算:
。请计算:
(1)原混合物中 的质量(写出计算过程)
的质量(写出计算过程) _______ 。
(2)在图中画出向20 g 和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据_______ 。

(3)氧化亚铜可用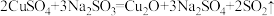 原理制备。
原理制备。
①反应过程中产生 可循环利用,因此应该选用
可循环利用,因此应该选用_______ 溶液来吸收它。
②反应过程中溶液pH将_______ (填“变大”“变小”或“不变”),因此制备过程,要控制溶液的酸碱度,因为如果反应时溶液pH过小,会导致产品下降,原因是_______ 。
 可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将
可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将 和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知:
和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知: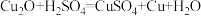 。请计算:
。请计算:(1)原混合物中
 的质量(写出计算过程)
的质量(写出计算过程) (2)在图中画出向20 g
 和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
(3)氧化亚铜可用
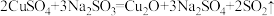 原理制备。
原理制备。①反应过程中产生
 可循环利用,因此应该选用
可循环利用,因此应该选用②反应过程中溶液pH将
您最近半年使用:0次
2 . 铜是重要的工业原料,现有Cu、Cu2O组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g该混合物加入0.5 L 3.6mol/L的稀硝酸中,固体物质完全反应,溶液中铜元素均为Cu2+,且生成4.48 L(标准状况)的NO。向所得溶液中加入a L 2.0 mol/L的NaOH溶液,恰好使溶液中的Cu2+沉淀完全。
(1)Cu与稀硝酸反应的离子方程式为_______ ;
(2)a=_______ L;
(3)求混合物中Cu的质量分数_______ 。
(1)Cu与稀硝酸反应的离子方程式为
(2)a=
(3)求混合物中Cu的质量分数
您最近半年使用:0次
解题方法
3 . 将55g铁片放入硫酸铜溶液片刻,取出洗涤干燥后称重,质量为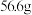 ,求参加反应的铁和生成的铜的质量
,求参加反应的铁和生成的铜的质量___________ 。
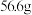 ,求参加反应的铁和生成的铜的质量
,求参加反应的铁和生成的铜的质量
您最近半年使用:0次
名校
解题方法
4 . 把氧化铁、氧化铜和铁粉组成的混合物,投入到3mol·L-1200mL的盐酸中,充分反应后,产生标准状况下的H2896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中c(H+)的浓度为08mol·L-1。求原混合物中各成分的物质的量___ 、___ 、___ 。
您最近半年使用:0次
5 . 向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
(1)Cu与稀HNO3反应的离子方程式为_____ 。
(2)混合物中Cu与Cu2O的物质的量分别为______ 、______ 。(要求写出计算过程)
(1)Cu与稀HNO3反应的离子方程式为
(2)混合物中Cu与Cu2O的物质的量分别为
您最近半年使用:0次
20-21高一下·浙江·开学考试
解题方法
6 . 将CuO和Fe2O3的混合物ag分成两等份,向其中一份混合物中加入2mol/L的硫酸溶液50mL,恰好将固体完全溶解。将另一份混合物在过量的CO气流中加热并充分反应,冷却后得到剩余固体质量为bg。求;
(1)硫酸溶液中的 的物质的量为
的物质的量为_______ mol。
(2)b=_______ g(用a表示)。
(1)硫酸溶液中的
 的物质的量为
的物质的量为(2)b=
您最近半年使用:0次
20-21高一下·浙江绍兴·阶段练习
7 . 称取CuO和Fe2O3的固体混合物4.00 g,加入50.0 mL 2.00 mol/L的H2SO4充分反应,往所得溶液中加入5.60 g Fe粉,充分反应后,得到固体的质量为3.04 g。请计算:
(1)加入Fe粉充分反应后,溶液中溶质的物质的量_______ mol。
(2)固体混合物中CuO的质量分数_______ 。
(1)加入Fe粉充分反应后,溶液中溶质的物质的量
(2)固体混合物中CuO的质量分数
您最近半年使用:0次
8 . X是金属M的碱式碳酸盐,不含结晶水。称取质量相等的样品两份,分别进行处理:一份在H2中充分处理(反应1),收集得0.994g水,剩余残渣为金属M的单质,重2.356g;另一份则在CO中处理(反应2),完全反应后得到1.245LCO2(101.325kPa,0°C),剩余残渣和反应1完全相同。
(1)通过计算,推出X的化学式______ 。
(2)写出X分别和H2、CO反应的方程式______ (要求系数为最简整数比)
(1)通过计算,推出X的化学式
(2)写出X分别和H2、CO反应的方程式
您最近半年使用:0次
9 . 称取8.00 g氧化铜和氧化铁固体混合物,加入100 mL2.00mol/L的硫酸充分溶解,往所得溶液中加11.2g铁粉,充分反应后,得固体的质量为6.08g。请计算:
(1)加入铁粉充分反应后,溶液中溶质的物质的量_______ 。
(2)固体混合物中氧化铜的质量_______ 。
(1)加入铁粉充分反应后,溶液中溶质的物质的量
(2)固体混合物中氧化铜的质量
您最近半年使用:0次
解题方法
10 . 碱式碳酸铜[Cu2(OH)2CO3]用作农药防治小麦黑穗病。实验室用加热法测定某农药中碱式碳酸铜的质量分数(假设杂质受热不参与反应)。充分加热100 g样品,得到固体84.5 g。已知反应的化学方程式为:Cu2(OH)2CO3 2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
试计算:(1)Cu2(OH)2CO3中铜元素与氧元素的质量比___________ 。(最简整数比)
(2)质量分数最大的元素是___________ 。(填元素名称)
(3)样品中碱式碳酸铜的质量分数是多少__________ ?(保留1位小数)
 2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。
2CuO+H2O+CO2↑,Cu2(OH)2CO3的相对分子质量为222。试计算:(1)Cu2(OH)2CO3中铜元素与氧元素的质量比
(2)质量分数最大的元素是
(3)样品中碱式碳酸铜的质量分数是多少
您最近半年使用:0次



