名校
解题方法
1 . 在298K、101kPa时,已知:



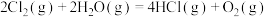

则 与
与 和
和 间的关系正确的是
间的关系正确的是




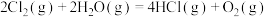

则
 与
与 和
和 间的关系正确的是
间的关系正确的是A.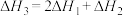 | B. |
C.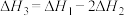 | D.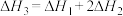 |
您最近一年使用:0次
2023-12-11更新
|
270次组卷
|
11卷引用:陕西省延安市富县高级中学2021-2022学年高一下学期期中考试化学试题
陕西省延安市富县高级中学2021-2022学年高一下学期期中考试化学试题天津市第二南开学校2022-2023学年度高二上学期期中质量调查化学试题广东省江门市鹤山市第一中学2022-2023学年高二上学期第二阶段考试化学试题宁夏吴忠市盐池高级中学2019-2020学年高二上学期期末检测化学试题广东省普宁市第二中学2021-2022学年高二上学期期中考试化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题贵州省黔西南布依族苗族自治州2022-2023学年高二上学期期末考试化学试题北京市第五十中学2023-2024学年高二上学期期中考试化学试题广东省广州市第三中学、第四中学、培正中学2023-2024学年高二上学期期中考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第二次月考化学试题福建省龙岩市永定区城关中学2023-2024学年高二上学期期中考试化学试题
2 . 下列关于反应热的说法正确的是
A.可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的ΔH小于0,说明此反应为吸热反应 CO2(g)+H2(g)”中的ΔH小于0,说明此反应为吸热反应 |
| B.已知S(s)+3/2O2(g)=SO3(g)的反应热为-385.5kJ/mol,说明硫的燃烧热为385.5 kJ·mol-1 |
| C.一个化学反应的反应热等于反应物的总能量减去生成物的总能量 |
| D.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
您最近一年使用:0次
2022-10-08更新
|
244次组卷
|
2卷引用:黑龙江省佳木斯市第八中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
3 . 下列关于盖斯定律的说法错误的是
| A.盖斯定律遵守能量守恒定律 |
| B.不管反应是一步完成还是分几步完成,其反应热都相同 |
| C.有些反应的反应热不能直接测得,可通过盖斯定律间接计算得到 |
| D.化学反应的反应热不仅与反应体系的始态和终态有关,还与反应的途径有关 |
您最近一年使用:0次
名校
解题方法
4 . 将氯化氢直接氧化转化为氯气的技术成为科学研究的热点,直接氧化法可按下列催化过程进行:
①CuCl2(s)=CuCl(s)+ Cl2(g) ΔH1=+83 kJ·mol- 1
Cl2(g) ΔH1=+83 kJ·mol- 1
②CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=- 20 kJ·mol- 1
Cl2(g) ΔH2=- 20 kJ·mol- 1
③CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=- 121 kJ·mol- 1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH等于
①CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=+83 kJ·mol- 1
Cl2(g) ΔH1=+83 kJ·mol- 1②CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=- 20 kJ·mol- 1
Cl2(g) ΔH2=- 20 kJ·mol- 1③CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=- 121 kJ·mol- 1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH等于
| A.-141 kJ·mol-1 | B.+101 kJ·mol-1 | C.+63 kJ·mol-1 | D.-116 kJ·mol-1 |
您最近一年使用:0次
名校
解题方法
5 . 如图是金属镁和卤素单质X2反应的能量变化示意图。下列说法正确的是
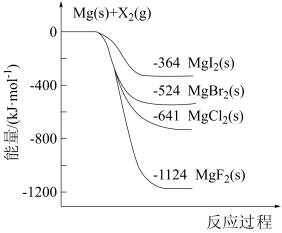

| A.由MgCl2制取Mg是放热过程 |
| B.热稳定性: MgI2 > MgBr2 > MgCl2 > MgF2 |
| C.金属镁和卤素单质X2的反应都是放热反应 |
| D.由图可知,此温度下MgBr2 (s) 与Cl2 (g) 反应的热化学方程式为MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(g) ∆H=+117kJ/mol |
您最近一年使用:0次
2022-03-10更新
|
1214次组卷
|
14卷引用:辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题
辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题(已下线)化学反应的热效应——进阶学习新疆维吾尔自治区喀什第二中学2022-2023学年高二上学期第一次月考化学试题贵州省贵州铜仁伟才学校2022-2023学年高二上学期12月月考化学试题湖南省长沙市芙蓉高级中学2022-2023学年高二上学期期中考试化学试题广东省佛山市三水中学2022-2023学年高二上学期10月第一次统测化学试题山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题山东省实验中学2019-2020学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 专题1 焓变知识的综合应用高中必刷题高二选择性必修1第一章 化学反应的热效应 专题1 反应热知识的综合应用宁夏银川一中2020-2021学年高二上学期期末考试化学试题选择性必修1专题1第一单元 突破1 反应热知识的综合应用广东省佛山市第一中学2021-2022学年高二上学期第一次段考化学试题 广东省广州市白云中学2023-2024学年高二上学期期中考试化学试题
6 . 依据图示关系, 等于
等于
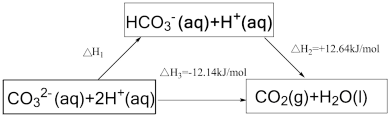
 等于
等于
A.+0.5 | B.-0.5 | C.+24.78 | D.-24.78 |
您最近一年使用:0次
2022-01-23更新
|
310次组卷
|
4卷引用:内蒙古通辽市开鲁县第一中学2021-2022学年高一下学期期中考试化学试题
名校
7 . 氮化铝导热性好,热膨胀系数小,是良好的耐热冲击材料,可用炭热还原 制取。已知:
制取。已知:
①
②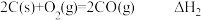
③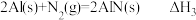
则反应 的
的 为
为
 制取。已知:
制取。已知:①

②
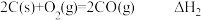
③
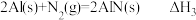
则反应
 的
的 为
为A. | B. |
C. | D. |
您最近一年使用:0次
2022-01-21更新
|
450次组卷
|
2卷引用:浙江省宁波效实中学2021-2022学年高一下学期期中考试化学(选考)试题
名校
解题方法
8 . 环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
已知: (g)=
(g)= (g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
(g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
 (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
(g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
则氢气和碘蒸气反应生成碘化氢气体的热化学方程式为
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。已知:
 (g)=
(g)= (g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
(g)+H2(g) ΔH1= +100.3 kJ·mol-1 ① (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
(g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②则氢气和碘蒸气反应生成碘化氢气体的热化学方程式为
| A.H2(g)+I2(s)=2HI(g) ΔH= -11.0 kJ·mol-1 |
| B.H2(g)+I2(g)=2HI(g) ΔH= -11.0 kJ·mol-1 |
| C.H2+I2=2HI ΔH= -11.0 kJ·mol-1 |
| D.H2(g)+I2(g)=2HI(g) ΔH= +11.0 kJ·mol-1 |
您最近一年使用:0次
2021-11-03更新
|
306次组卷
|
3卷引用:山西长治上党区第一中学校2021-2022学年高一下学期期末考试化学试题
9 . 已知:a.C2H2(g)+ H2(g)= C2H4(g)ΔH<0
b. 2CH4(g)= C2H4(g)+ 2H2(g)ΔH>0
判断以下3个热化学方程式:
①C(s)+ 2H2(g)= CH4(g)ΔH1
②C(s)+ H2(g)=
H2(g)=  C2H2(g)ΔH2
C2H2(g)ΔH2
③C(s)+ H2(g)= C2H4(g)ΔH3
C2H4(g)ΔH3
ΔH1、ΔH2、ΔH3由大到小的顺序是( )
b. 2CH4(g)= C2H4(g)+ 2H2(g)ΔH>0
判断以下3个热化学方程式:
①C(s)+ 2H2(g)= CH4(g)ΔH1
②C(s)+
 H2(g)=
H2(g)=  C2H2(g)ΔH2
C2H2(g)ΔH2③C(s)+ H2(g)=
 C2H4(g)ΔH3
C2H4(g)ΔH3ΔH1、ΔH2、ΔH3由大到小的顺序是( )
| A.ΔH2 >ΔH3 >ΔH1 | B.ΔH3 >ΔH2 >ΔH1 |
| C.ΔH3 >ΔH1 >ΔH2 | D.ΔH1 >ΔH2 >ΔH3 |
您最近一年使用:0次
2016-12-09更新
|
542次组卷
|
12卷引用:湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题
湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题新疆哈密市第十五中学2019-2020学年高一上学期期末考试化学试题广东省梅州市蕉岭县蕉岭中学2022-2023学年高三上学期高二第二次质检化学试题2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷西藏自治区拉萨中学2017-2018学年高二上学期第二次月考理综化学试题【全国百强校】内蒙古巴彦淖尔一中2018-2019学年高二上学期期中考试化学试题贵州省龙里中学2019-2020学年高二上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题河南省内乡县第三高级中学2021-2022学年高二上学期第一次月考化学试卷(已下线)BBWYhjhx1102云南省文山州广南县第十中学校2023-2024学年高二上学期期中考试化学试题



