解题方法
1 . (1)研究 、
、 等大气污染气体的处理方法具有重要的意义。
等大气污染气体的处理方法具有重要的意义。
已知:①
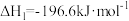
②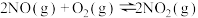
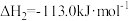
则反应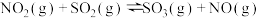 的
的
_______  。
。
(2)t℃时,将2mol 和1mol
和1mol 通入体积为2L的恒温、恒容密闭容器中,发生如下反应:
通入体积为2L的恒温、恒容密闭容器中,发生如下反应: ,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
①下列叙述能证明该反应已达到化学平衡状态的是_______ (选填字母)。
A.容器内压强不再发生变化
B. 的体积分数不再发生变化
的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmol 的同时消耗nmol
的同时消耗nmol
E.相同时间内消耗2nmol 的同时生成nmol
的同时生成nmol
F.混合气体密度不再变化
②从反应开始到达化学平衡,生成 的平均反应速率为
的平均反应速率为___ ;平衡时, 的转化率为
的转化率为___ 。
(3)已知 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是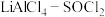 。电池的总反应可表示为
。电池的总反应可表示为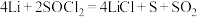 。请回答下列问题:
。请回答下列问题:
①电池的负极材料为_______ ,发生的电极反应为_______ 。
②电池正极发生的电极反应为_______ 。
 、
、 等大气污染气体的处理方法具有重要的意义。
等大气污染气体的处理方法具有重要的意义。已知:①

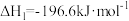
②
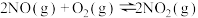
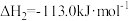
则反应
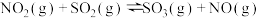 的
的
 。
。(2)t℃时,将2mol
 和1mol
和1mol 通入体积为2L的恒温、恒容密闭容器中,发生如下反应:
通入体积为2L的恒温、恒容密闭容器中,发生如下反应: ,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:①下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化
B.
 的体积分数不再发生变化
的体积分数不再发生变化C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmol
 的同时消耗nmol
的同时消耗nmol
E.相同时间内消耗2nmol
 的同时生成nmol
的同时生成nmol
F.混合气体密度不再变化
②从反应开始到达化学平衡,生成
 的平均反应速率为
的平均反应速率为 的转化率为
的转化率为(3)已知
 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是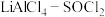 。电池的总反应可表示为
。电池的总反应可表示为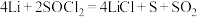 。请回答下列问题:
。请回答下列问题:①电池的负极材料为
②电池正极发生的电极反应为
您最近一年使用:0次
2 . 选择性催化还原法(SCR)是目前应用最为广泛的氮氧化物NOx的净化方法,其原理是利用NH3在特定催化剂作用下将NOx还原为N2。
主反应:4NH3(g) +4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH1
4N2(g)+6H2O(g) ΔH1
副反应:4NH3(g)+ 3O2(g) 2N2(g)+6H2O(g) ΔH2
2N2(g)+6H2O(g) ΔH2
(1)在无氧条件下,NH3也可还原NO:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3,
5N2(g)+6H2O(g) ΔH3,
则ΔH2=___________ (用含ΔH1、ΔH3的式子表示)。一定温度下,向2 L密闭刚性容器(含催化剂)中投入2 mol NH3和3 mol NO,发生反应4NH3(g)+6NO(g)  5N2(g)+ 6H2O(g)。达到平衡状态时,NO的转化率为60 %,则平衡常数为
5N2(g)+ 6H2O(g)。达到平衡状态时,NO的转化率为60 %,则平衡常数为___________ mol·L-1(列出计算式即可)。
(2)目前使用的SCR催化剂是V2O5-WO3/TiO2,关于该催化剂的说法正确的是___________ 。
A.能加快反应速率,并且改变反应的焓变
B.能增大NH3还原NOx反应的平衡常数
C.具有选择性,能降低特定反应的活化能
(3)催化剂V2O5-WO3/TiO2中的V2O5是活性组分。在石英微型反应器中以一定流速通过烟气[n(O2):n(NH3):n(NO)=71:1:1],在不同温度下进行该催化还原反应,V2O5的质量分数对单位时间内NO去除率的影响如图所示。
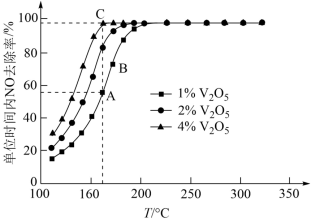
①从起始至对应A、B、C三点的平均反应速率由大到小的顺序为___________ 。
②V2O5的质量分数对该催化剂活性的影响是___________ 。
(4)NO2存在如下平衡:2NO2(g) N2O4(g) △H<0,在一定条件下,NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)= k2·p(N2O4)。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系k1=
N2O4(g) △H<0,在一定条件下,NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)= k2·p(N2O4)。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系k1=_____ 。
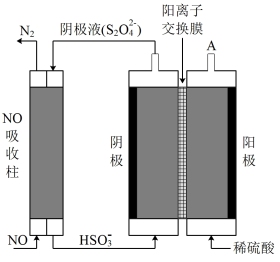
(5)还可用间接电解法除NO。其原理如图所示,则电解池阴极的电极反应为___________ 。
主反应:4NH3(g) +4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH1
4N2(g)+6H2O(g) ΔH1副反应:4NH3(g)+ 3O2(g)
 2N2(g)+6H2O(g) ΔH2
2N2(g)+6H2O(g) ΔH2(1)在无氧条件下,NH3也可还原NO:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH3,
5N2(g)+6H2O(g) ΔH3,则ΔH2=
 5N2(g)+ 6H2O(g)。达到平衡状态时,NO的转化率为60 %,则平衡常数为
5N2(g)+ 6H2O(g)。达到平衡状态时,NO的转化率为60 %,则平衡常数为(2)目前使用的SCR催化剂是V2O5-WO3/TiO2,关于该催化剂的说法正确的是
A.能加快反应速率,并且改变反应的焓变
B.能增大NH3还原NOx反应的平衡常数
C.具有选择性,能降低特定反应的活化能
(3)催化剂V2O5-WO3/TiO2中的V2O5是活性组分。在石英微型反应器中以一定流速通过烟气[n(O2):n(NH3):n(NO)=71:1:1],在不同温度下进行该催化还原反应,V2O5的质量分数对单位时间内NO去除率的影响如图所示。

①从起始至对应A、B、C三点的平均反应速率由大到小的顺序为
②V2O5的质量分数对该催化剂活性的影响是
(4)NO2存在如下平衡:2NO2(g)
 N2O4(g) △H<0,在一定条件下,NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)= k2·p(N2O4)。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系k1=
N2O4(g) △H<0,在一定条件下,NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)= k2·p(N2O4)。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系k1=(5)还可用间接电解法除NO。其原理如图所示,则电解池阴极的电极反应为

您最近一年使用:0次
解题方法
3 .  、
、 、
、 等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
(1)二甲醚( )被誉为“21世纪的清洁燃料”,由
)被誉为“21世纪的清洁燃料”,由 和
和 制备二甲醚的反应原理如下:
制备二甲醚的反应原理如下:


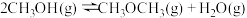
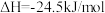
已知: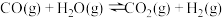
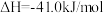
则 的
的
_______ 。
(2)200℃,在2L的密闭容器中充入
 和
和
 ,发生反应
,发生反应 (I);
(I); (II),
(II), 达到平衡,平衡时
达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则:
,则:
① 内,反应(Ⅰ)平均反应速率
内,反应(Ⅰ)平均反应速率
_______ 。
②反应(Ⅱ)中 的转化率
的转化率
_______ 。
(3)利用电化学原理将 、
、 转化为重要化工原料,装置如图所示:
转化为重要化工原料,装置如图所示:

①若A为 ,B为
,B为 ,C为
,C为 ,则通入
,则通入 一极的电极反应式为
一极的电极反应式为_______ 。
②若A为 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为_______ 。
 、
、 、
、 等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。(1)二甲醚(
 )被誉为“21世纪的清洁燃料”,由
)被誉为“21世纪的清洁燃料”,由 和
和 制备二甲醚的反应原理如下:
制备二甲醚的反应原理如下:

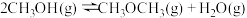
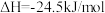
已知:
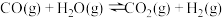
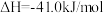
则
 的
的
(2)200℃,在2L的密闭容器中充入

 和
和
 ,发生反应
,发生反应 (I);
(I); (II),
(II), 达到平衡,平衡时
达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则:
,则:①
 内,反应(Ⅰ)平均反应速率
内,反应(Ⅰ)平均反应速率
②反应(Ⅱ)中
 的转化率
的转化率
(3)利用电化学原理将
 、
、 转化为重要化工原料,装置如图所示:
转化为重要化工原料,装置如图所示:
①若A为
 ,B为
,B为 ,C为
,C为 ,则通入
,则通入 一极的电极反应式为
一极的电极反应式为②若A为
 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为
您最近一年使用:0次



