1 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a) CH4(g)+CO2(g) ⇌ 2CO(g)+2H2(g) ∆H1
b) CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ∆H2
c) CH4(g) ⇌ C(s)+2H2(g) ∆H3
d) 2CO(g) ⇌ CO2(g)+C(s) ∆H4
e) CO(g)+H2(g) ⇌ H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=___________ (写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
(3)一定条件下,CH4分解形成碳的反应历程如图1所示。该历程分___________ 步进行,其中,第___________ 步的正反应活化能最大。 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。
①反应a、c、e中,属于吸热反应的有___________ (填字母)。
②反应c的相对压力平衡常数表达式为K =
=___________ 。
(5)CO2用途广泛,写出基于其物理性质的一种用途:___________ 。
a) CH4(g)+CO2(g) ⇌ 2CO(g)+2H2(g) ∆H1
b) CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ∆H2
c) CH4(g) ⇌ C(s)+2H2(g) ∆H3
d) 2CO(g) ⇌ CO2(g)+C(s) ∆H4
e) CO(g)+H2(g) ⇌ H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
| A.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加 |
| B.移去部分C(s),反应c、d、e的平衡均向右移动 |
| C.加入反应a的催化剂,可提高CH4的平衡转化率 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |
(3)一定条件下,CH4分解形成碳的反应历程如图1所示。该历程分
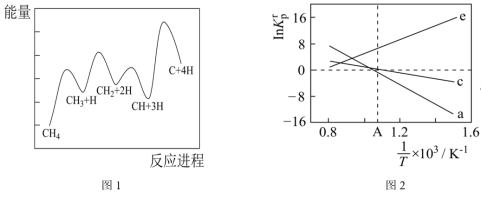
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。①反应a、c、e中,属于吸热反应的有
②反应c的相对压力平衡常数表达式为K
 =
=(5)CO2用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
解题方法
2 . 甲醛( )在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
反应I:

反应Ⅱ: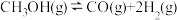

已知:①平衡状态下,甲醛选择性 ;甲醛的收率
;甲醛的收率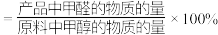 。
。
②几种物质的燃烧热( )如下表:
)如下表:
回答下列问题:
(1)
___________ ,反应I的正反应活化能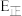
___________ (填“>”或“<”)逆反应活化能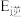 。
。
(2)反应I、反应Ⅱ的反应历程可表示为:
历程i:……
历程ii: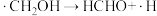
历程iii:
历程iV: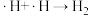
写出历程i的反应方程式:___________ 。
(3)将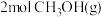 加入容积为
加入容积为 的刚性密闭容器中,温度对平衡状态下
的刚性密闭容器中,温度对平衡状态下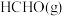 的选择性和收率的影响如图所示。
的选择性和收率的影响如图所示。___________ (填“I”或“Ⅱ”),判断的依据是___________ 。
②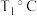 ,反应进行到
,反应进行到 时达到平衡,此时
时达到平衡,此时 的转化率为
的转化率为___________ ,
___________ ,反应I的平衡常数
___________  。
。
 )在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:反应I:


反应Ⅱ:
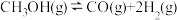

已知:①平衡状态下,甲醛选择性
 ;甲醛的收率
;甲醛的收率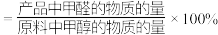 。
。②几种物质的燃烧热(
 )如下表:
)如下表:| 物质 |  | 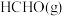 |  |  |
燃烧热 |  |  |  | 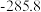 |
(1)

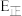
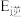 。
。(2)反应I、反应Ⅱ的反应历程可表示为:
历程i:……
历程ii:
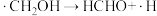
历程iii:

历程iV:
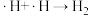
写出历程i的反应方程式:
(3)将
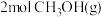 加入容积为
加入容积为 的刚性密闭容器中,温度对平衡状态下
的刚性密闭容器中,温度对平衡状态下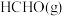 的选择性和收率的影响如图所示。
的选择性和收率的影响如图所示。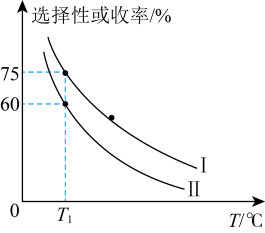
②
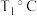 ,反应进行到
,反应进行到 时达到平衡,此时
时达到平衡,此时 的转化率为
的转化率为

 。
。
您最近一年使用:0次
3 . 下列方案设计、现象和结论正确的是
| 方案设计 | 现象 | 结论 | |
| A | 将适量硫粉和铁粉混合堆成条状。用灼热的玻璃棒触及一端,当混合物呈红热状态时,移开玻璃棒。 | 混合物继续保持红热并持续扩散,粉末呈黑色 | Fe和S反应为放热反应 |
| B | 将银粉分别加入硫酸和HI溶液中 | 前者无明显现象,后者生成无色气体和黄色沉淀 | 氧化性:H2SO4<HI |
| C | 取适量Na2SO3溶液于试管中,测定pH然后加热一段时间,冷却至原温度,再次测定该溶液的pH | pH变小 | SO32-水解过程为放热过程 |
| D | 向有机物样品中加入过量NaOH后,再加入新制Cu(OH)2 | 加热后产生砖红色沉淀 | 该有机物为醛 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 .  -月桂烯与
-月桂烯与 的加成反应的部分机理和反应势能变化如图所示。
的加成反应的部分机理和反应势能变化如图所示。
 -月桂烯与
-月桂烯与 的加成反应的部分机理和反应势能变化如图所示。
的加成反应的部分机理和反应势能变化如图所示。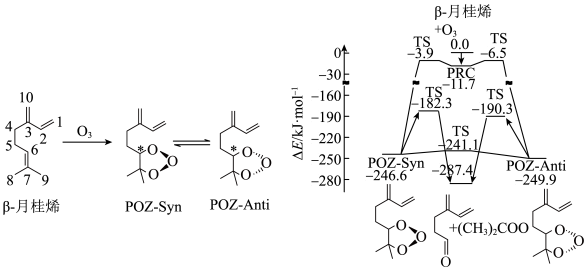
A. -月桂烯与丁基苯互为同分异构体 -月桂烯与丁基苯互为同分异构体 |
| B.POZ-Anti比POZ-Syn更稳定 |
C.升高温度,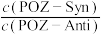 一定减小 一定减小 |
D. -月桂烯与 -月桂烯与 经历两种历程得到 经历两种历程得到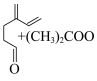 释放的能量相同 释放的能量相同 |
您最近一年使用:0次
名校
解题方法
5 . 甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
| A.CO的燃烧热为﹣566.0kJ•mol﹣1 |
| B.2molCO和1molO2的总能量比2molCO2的总能量低 |
| C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3kJ |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) ΔH=﹣1453.28kJ•mol﹣1 |
您最近一年使用:0次
名校
6 . 光照条件下乙苯与氯气反应生成两种一氯取代物,反应过程中的能量变化如图所示[选择性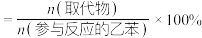 ],下列说法正确的是
],下列说法正确的是
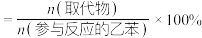 ],下列说法正确的是
],下列说法正确的是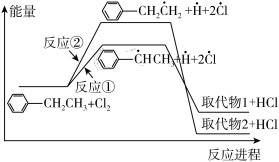
A.稳定性: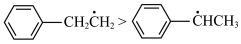 |
| B.生成相同物质的量的取代物2比取代物1吸收的热量更多 |
| C.反应①达到平衡状态后,升高温度,正、逆反应速率均增大,但正反应速率增大更明显 |
| D.一定条件下,选择合适的催化剂可以提高取代物1的选择性 |
您最近一年使用:0次
2024-06-02更新
|
215次组卷
|
2卷引用:2024届河北省部分高中高三下学期二模化学试题
名校
7 . 纳米碗 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由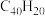 分子经过连续5步氢抽提和闭环脱氢反应生成。
分子经过连续5步氢抽提和闭环脱氢反应生成。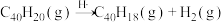 的反应机理和能量变化如图所示:
的反应机理和能量变化如图所示:
 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由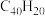 分子经过连续5步氢抽提和闭环脱氢反应生成。
分子经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能量变化如图所示:
的反应机理和能量变化如图所示: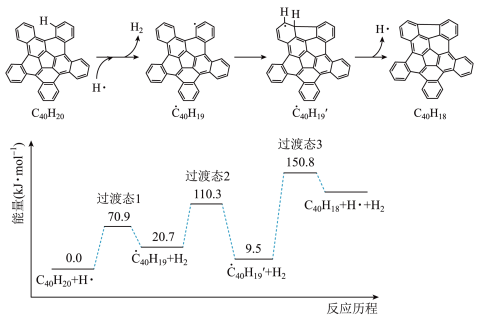
| A.图示历程中包含3个基元反应,其中速率最慢的是第3个 |
B. 反应中 反应中 被还原 被还原 |
C. 纳米碗中五元环和六元环结构的数目分别为6、10 纳米碗中五元环和六元环结构的数目分别为6、10 |
D.1mol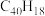 完全加氢成环烷烃需要20mol 完全加氢成环烷烃需要20mol |
您最近一年使用:0次
2024-06-02更新
|
96次组卷
|
2卷引用:2024届安徽省合肥市高三下学期最后一卷三模化学试题
8 . 自然界中存在若干循环,这些循环是自然界中物质和能量的交换方式,它们相互作用、相互影响,维持着生态系统的平衡。下列叙述正确的是
A.碳循环:碳循环只涉及CO2和 之间的转化 之间的转化 |
| B.氮循环:氮循环中的氮只发生氧化反应 |
| C.水循环:水循环涉及吸热过程和放热过程 |
| D.硫循环:硫循环的过程只在大气中进行 |
您最近一年使用:0次
9 . 中国传统文化源远流长,为世界文明作出巨大贡献。以下对中国传统文化理解正确的是
| A.《本草纲目》记载“盖此矾色绿,味酸,烧之则赤”,“矾”指的是CuSO4•5H2O |
| B.《劝学》中“冰,水为之,而寒于水”,说明冰的能量更高 |
| C.《己亥杂诗》中“落红不是无情物,化作春泥更护花”,蕴含着自然界中的碳、氮循环 |
| D.《杨柳歌》中“独忆飞絮鹅毛下,非复青丝马尾垂”,“飞絮”的化学成分为蛋白质 |
您最近一年使用:0次
2024-05-31更新
|
156次组卷
|
2卷引用:2024届陕西省渭南市临渭区高三下学期三模理综试题-高中化学
解题方法
10 . 银及其化合物在催化与电化学等领域中具有重要应用。已知:①在银催化下,乙烯与氧气反应生成乙醛(CH3-CHO)和环氧乙烷(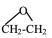 )。下图所示是两反应分步进行的历程图:
)。下图所示是两反应分步进行的历程图:
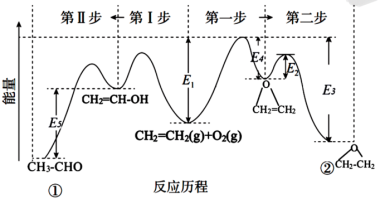
i:2CH2=CH2(g)+O2(g)⇌2CH2=CH-OH(g) ΔH1
ii:CH2=CH-OH(g) ⇌CH3-CHO(g) ΔH2
③乙烯与氧气反应生成环氧乙烷的分步反应方程式为:
iii:2CH2=CH2(g)+O2(g) 2
2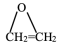 (g) ΔH3
(g) ΔH3
iv: (g)
(g)
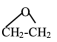 (g) ΔH4
(g) ΔH4
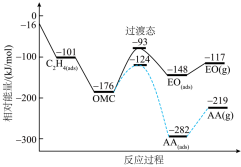
(2)根据已知条件③,乙烯与氧气反应生成环氧乙烷的热化学方程式为:
(3)根据已知条件④,中间体OMC生成吸附态AA(ads)的活化能为
 。
。(4)某温度下,在一体积为1L的恒容密闭容器中,充入1.8molCH2=CH2(g)和0.8molO2(g)发生反应:2CH2=CH2(g)+O2(g)⇌2CH3-CHO(g) ΔH,反应进行10min后到达平衡,体系中各气体的体积分数随反应温度的变化如下图所示
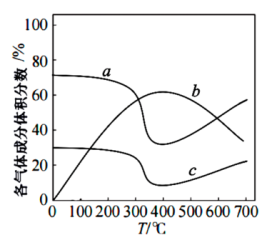
②温度为400℃,达到平衡时,化学反应速率v(O2)=
③温度为600℃,该反应的平衡常数Kc=
(5)乙醛燃料电池有广泛的应用前景,其工作原理如图所示
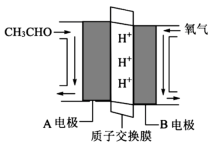
②A电极上的电极方程式为:
您最近一年使用:0次



