1 . 在一定固定容积的密闭容器中,CO2(g)与一定量的C(s)发生进行如下化学反应:CO2(g)+C(s)⇌2CO(g).
①该反应为_____ 反应(填“吸热”或“放热”).
②该反应的反应速率随时间的变化图象如图所示,则下列说法正确的是_____ (填序号).

a.t1时刻该反应已经处于化学平衡状态
b.t2时刻c(CO2)=c(CO)
c.t2时刻该反应仍然处于化学平衡状态
d.t2时刻,改变的条件可能是增大了C的物质的量.
①该反应为
②该反应的反应速率随时间的变化图象如图所示,则下列说法正确的是

a.t1时刻该反应已经处于化学平衡状态
b.t2时刻c(CO2)=c(CO)
c.t2时刻该反应仍然处于化学平衡状态
d.t2时刻,改变的条件可能是增大了C的物质的量.
您最近一年使用:0次
14-15高二上·河南周口·阶段练习
名校
解题方法
2 . 煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)=CO2(g) ΔH=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g) ΔH=E2 ②
H2(g)+ 1/2 O2(g)=H2O(g) ΔH=E3 ③
CO(g)+ 1/2 O2(g)=CO2(g) ΔH=E4 ④
回答:(1)与途径a相比途径b有较多的优点,即__________ 。
(2)上述四个热化学方程式中的哪个反应ΔH>0?_______ 。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为_________
a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)=CO2(g) ΔH=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g) ΔH=E2 ②
H2(g)+ 1/2 O2(g)=H2O(g) ΔH=E3 ③
CO(g)+ 1/2 O2(g)=CO2(g) ΔH=E4 ④
回答:(1)与途径a相比途径b有较多的优点,即
(2)上述四个热化学方程式中的哪个反应ΔH>0?
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为
您最近一年使用:0次
2016-12-09更新
|
339次组卷
|
6卷引用:2014-2015学年河南省周口中英文学校高二10月月考化学试卷
10-11高一下·广东汕头·期中
名校
解题方法
3 . (1)下图是等质量的碳酸钠、碳酸氢钠粉末分别与足量的盐酸发生反应时的情景,产生二氧化碳气体的体积较多的试管中加入的固体试剂是________ ,当反应结束时,A、B中消耗的盐酸的质量之比为________ 。
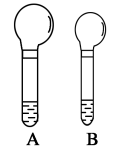
(2)实验过程中我们还能感受到碳酸钠与盐酸反应时是放热反应,而碳酸氢钠与盐酸反应时表现为吸热。在A、B试管的反应过程中,反应体系的能量变化的总趋势分别对应于A为________ ,B为________ (填“a”或“b”)。
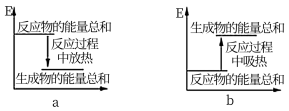

(2)实验过程中我们还能感受到碳酸钠与盐酸反应时是放热反应,而碳酸氢钠与盐酸反应时表现为吸热。在A、B试管的反应过程中,反应体系的能量变化的总趋势分别对应于A为

您最近一年使用:0次
2016-12-09更新
|
315次组卷
|
5卷引用:2010-2011学年广东省汕头市金山中学高一下学期期中考试化学试卷
(已下线)2010-2011学年广东省汕头市金山中学高一下学期期中考试化学试卷(已下线)2012年沪科版高中化学4.2化学变化中的能量变化练习卷辽宁省沈阳铁路实验中学2018-2019学年高一下学期4月月考化学试题(已下线)1.1.1 化学反应的焓变(1)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)5.3.1 化学变化中的能量变化(第1课时)-【帮课堂】高一化学同步精品讲义(沪科版2020必修第二册)
4 . 城市使用的燃料,现大多为煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它有煤炭与水蒸气在高温下反应制得,故又称水煤气。试回答:
(1)写出制取水煤气的主要化学方程式____________________ ,该反应是_________ 反应(填吸热、放热)。
(2)设液化石油气的主要成分为丁烷(C4H10),其充分燃烧后产物为CO2和H2O,试比较完全燃烧等质量的C4H10及CO所需的氧气的质量比(结果保留1位小数)____________________ 。
(1)写出制取水煤气的主要化学方程式
(2)设液化石油气的主要成分为丁烷(C4H10),其充分燃烧后产物为CO2和H2O,试比较完全燃烧等质量的C4H10及CO所需的氧气的质量比(结果保留1位小数)
您最近一年使用:0次
5 . (1)下列反应中,属于放热反应的是_______ 。
A.煤气化为水煤气B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑C.乙烯在氧气中燃烧 D.高温煅烧石灰石使其分解E.铝热反应F.葡萄糖在人体内氧化分解
(2)在化学上经常使用的氢核磁共振谱是根据不同化学环境的氢原子在氢核磁共振谱中给出的信号不同来确定有机物分子中不同氢原子的。下列有机物分子在氢核磁共振谱中给出两种信号的是_______ 。
①CH3Cl ②CH3CH2OH ③HCOOH ④CH3COOCH3 ⑤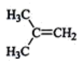 ⑥
⑥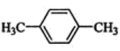 ⑦
⑦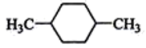 ⑧
⑧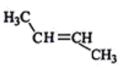
A.煤气化为水煤气B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑C.乙烯在氧气中燃烧 D.高温煅烧石灰石使其分解E.铝热反应F.葡萄糖在人体内氧化分解
(2)在化学上经常使用的氢核磁共振谱是根据不同化学环境的氢原子在氢核磁共振谱中给出的信号不同来确定有机物分子中不同氢原子的。下列有机物分子在氢核磁共振谱中给出两种信号的是
①CH3Cl ②CH3CH2OH ③HCOOH ④CH3COOCH3 ⑤
 ⑥
⑥ ⑦
⑦ ⑧
⑧
您最近一年使用:0次
6 . 下列反应中,属于放热反应的是__________ ,属于吸热反应的是___________
①食物在空气中腐败 ②生石灰与水作用制熟石灰 ③碳和二氧化碳化合生成CO ④酸与碱中和反应 ⑤加热KClO3和MnO2的混合物制O2⑥将氯化铵晶体和氢氧化钡晶体混合均匀放在日光下暴晒
①食物在空气中腐败 ②生石灰与水作用制熟石灰 ③碳和二氧化碳化合生成CO ④酸与碱中和反应 ⑤加热KClO3和MnO2的混合物制O2⑥将氯化铵晶体和氢氧化钡晶体混合均匀放在日光下暴晒
您最近一年使用:0次
7 . 如图是某同学在实验室中进行铝热反应的实验装置,实验中他观察到的现象之一为:“纸漏斗的下部被烧穿,有熔融物落入沙中”
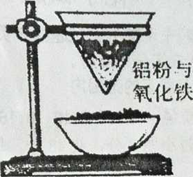
该反应的化学方程式是_______ ,其能量变化可用下图中的____ (填“a”或“b”)表示。

在反应中用到了镁条和氯酸钾,氯酸钾的作用是________ .

该反应的化学方程式是

在反应中用到了镁条和氯酸钾,氯酸钾的作用是
您最近一年使用:0次
10-11高一下·江西上饶·期中
8 . 下列反应中,属于放热反应的是_____________ 。
① 煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ② 燃烧木炭取暖 ③生石灰与水反应 ④ 酸与碱的中和反应 ⑤ 氢气还原氧化铜 ⑥ 灼热的木炭与CO2反应
① 煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ② 燃烧木炭取暖 ③生石灰与水反应 ④ 酸与碱的中和反应 ⑤ 氢气还原氧化铜 ⑥ 灼热的木炭与CO2反应
您最近一年使用:0次
10-11高一下·四川雅安·期中
9 . 下列反应属于放热反应的是_____ ;属于吸热反应的是_______ 。
A. 锌粒与稀H2SO4反应制取H2 B. 氢气在氧气中燃烧
C. 碳酸钙高温分解成氧化钙和二氧化碳 D. 氢氧化钾和硫酸中和
E.Ba(OH)2·8H2O与NH4Cl反应 F. C与CO2高温生成CO
G.葡萄糖在人体内氧化分解 H.钢铁制品生锈的反应
A. 锌粒与稀H2SO4反应制取H2 B. 氢气在氧气中燃烧
C. 碳酸钙高温分解成氧化钙和二氧化碳 D. 氢氧化钾和硫酸中和
E.Ba(OH)2·8H2O与NH4Cl反应 F. C与CO2高温生成CO
G.葡萄糖在人体内氧化分解 H.钢铁制品生锈的反应
您最近一年使用:0次
10 . 能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
① 2H2(g)+O2(g)=2H2O(l) H=-570 kJ·mol-1;
H=-570 kJ·mol-1;
② H2(g)+1/2O2(g)=H2O(g) H=-242kJ·mol-1;
H=-242kJ·mol-1;
③ C(s)+1/2O2(g)=CO(g) H= —110.5 kJ·mol-1;
H= —110.5 kJ·mol-1;
④ C(s)+O2(g)=CO2(g) H=-393.5 kJ·mol-1;
H=-393.5 kJ·mol-1;
⑤ CO2(g) +2H2O(g)=2CH4(g) +2 O2(g) H= +890 kJ·mol-1;
H= +890 kJ·mol-1;
回答下列问题:
(1)上述反应中属于吸热反应的是________
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s) + H2O(g)= H2(g)+ CO (g) H=akJ·mol-1;则a=
H=akJ·mol-1;则a=_______ ;该反应的熵 S
S________ 0(选填“>”、“=”、“<”)。
① 2H2(g)+O2(g)=2H2O(l)
 H=-570 kJ·mol-1;
H=-570 kJ·mol-1;② H2(g)+1/2O2(g)=H2O(g)
 H=-242kJ·mol-1;
H=-242kJ·mol-1;③ C(s)+1/2O2(g)=CO(g)
 H= —110.5 kJ·mol-1;
H= —110.5 kJ·mol-1;④ C(s)+O2(g)=CO2(g)
 H=-393.5 kJ·mol-1;
H=-393.5 kJ·mol-1;⑤ CO2(g) +2H2O(g)=2CH4(g) +2 O2(g)
 H= +890 kJ·mol-1;
H= +890 kJ·mol-1;回答下列问题:
(1)上述反应中属于吸热反应的是
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s) + H2O(g)= H2(g)+ CO (g)
 H=akJ·mol-1;则a=
H=akJ·mol-1;则a= S
S
您最近一年使用:0次



