解题方法
1 . 按要求回答下列问题:
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
(2)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应(反应物、产物均为气体),反应中各物质物质的量的变化如图所示。___________ 。
②在0~6s内,B的平均反应速率为___________ 。
③6s后容器内的压强与开始时压强之比为___________ 。
(3)已知CH3OCH3的结构式为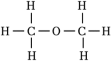 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 ___________ (填字母)。
a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
| A.甲烷的燃烧 |
| B.CO2通入灼热的炭层 |
| C.石灰石受热分解 |
| D.碘升华 |

②在0~6s内,B的平均反应速率为
③6s后容器内的压强与开始时压强之比为
(3)已知CH3OCH3的结构式为
 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
您最近一年使用:0次
名校
解题方法
2 . 化学反应中常伴随着能量变化。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因___________ 。
(2)该反应的能量变化可用下图中的___________ 表示(填序号)。___________ 。t2~t3速率变化的主要原因是___________ 。
(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式___________ 。
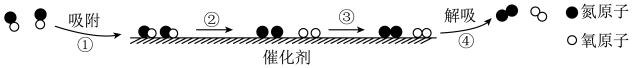
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。___________ 键断裂,此过程___________ (放出或者吸收)能量。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因
(2)该反应的能量变化可用下图中的


(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题:
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、
)、 、
、 等物质。
等物质。
①汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。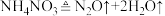 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。_______ 转化为化学能。
②根据数据计算,分解1 mol 需
需_______ (填“吸收”或“释放”)_______ kJ的能量。
(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应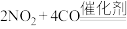
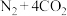 ,
,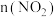 时间变化如表:
时间变化如表:
0~2s内用CO表示该反应的平均速率为_______ 。
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。
①能说明该反应已达到平衡状态的标志是_______ (填标号)
A.反应速率
B.容器内压强不再随时间而发生变化
C.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
D.容器内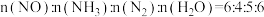
②某次实验中测得容器内NO及 的物质的量随时间变化如图。
的物质的量随时间变化如图。
_______  (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是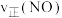
_______ 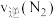 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠(
 )、
)、 、
、 等物质。
等物质。①汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.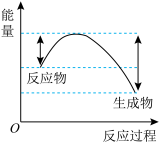 B.
B.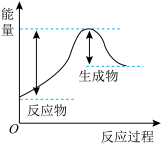 C.
C.
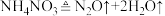 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
②根据数据计算,分解1 mol
 需
需(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应
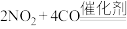
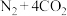 ,
,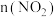 时间变化如表:
时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
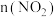 /mol /mol | a | b | c | d | e | f |
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率

B.容器内压强不再随时间而发生变化
C.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化D.容器内
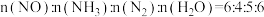
②某次实验中测得容器内NO及
 的物质的量随时间变化如图。
的物质的量随时间变化如图。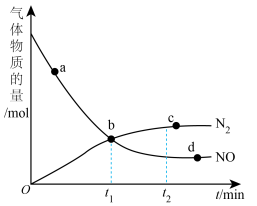

 (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是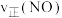
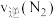 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
名校
4 . 化学反应中会伴随放热和吸热的现象,请回答下列问题:
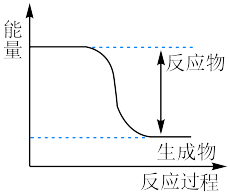
在人体内,O2与葡萄糖反应生成H2O和CO2的能量变化如图所示:___________ (填“放热”或“吸热”)反应,断开氧气分子中的化学键会___________ (填“放出”或“吸收”)能量,形成H-O键会___________ (填“放出”或“吸收”)能量,反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物的总能量。
(2)某同学进行如下实验,研究化学反应中的热量变化。___________ (填“放热”或“吸热”)反应,Ba(OH)2·8H2O与NH4Cl的反应是___________ (填“放热”或“吸热”)反应。
(3)①中反应的离子方程式为___________ ,该反应的还原剂是___________ (填化学式)。
在人体内,O2与葡萄糖反应生成H2O和CO2的能量变化如图所示:
(2)某同学进行如下实验,研究化学反应中的热量变化。
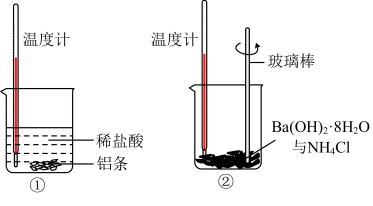
(3)①中反应的离子方程式为
您最近一年使用:0次
5 . 回答下列问题:
(1)反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,E3_______ ,E2_______ (填“增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ ( 填 “增大”、“减小”或“不变” )。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g) CH3OH(g) △H=
CH3OH(g) △H=____________ kJ•mol﹣1 (用a、b、c表示)。
(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g) CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。______ 0 (填“>”、“<”或“=”) ②p2_____ p1(填“>”、“<”或“=”);
(1)反应A(g)+B(g)
 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。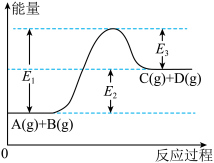
②在反应体系中加入催化剂,反应速率增大,E3
③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g)
 CH3OH(g) △H=
CH3OH(g) △H=(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g)
 CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。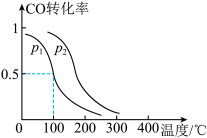
您最近一年使用:0次
解题方法
6 . I.回答下列问题。
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤ 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO
(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)___________ (填“吸收"或“放出”)的能量为___________ kJ。
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:___________ (填“氧化剂”或“还原剂”)。
(5)写出氧化炉中反应的化学方程式___________ 。
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤
 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
A.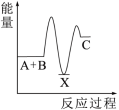 | B.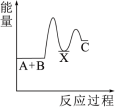 | C.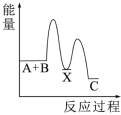 | D.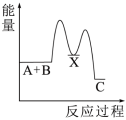 |
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
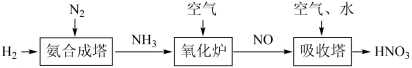
(5)写出氧化炉中反应的化学方程式
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
7 . 下图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应。___________ 。
(2)该反应是___________ (填“放热”或“吸热”)反应,结合实验现象写出判断依据___________ 。
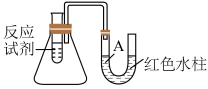
(2)该反应是
您最近一年使用:0次
2024-04-25更新
|
55次组卷
|
2卷引用:上海市松江二中2023-2024学年高一下学期期中测试 化学试卷
名校
解题方法
8 . 请完成下列问题:
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是___________ (填序号)。
①碳酸钙高温分解 ②生石灰和水的反应 ③ 在
在 中燃烧
中燃烧
(2)如图是原电池的装置图。请回答下列问题:___________ (填“正极”或“负极”),发生___________ 反应(填“氧化”或“还原”);电子由___________ 片通过导线流向___________ 片。(均填化学式)
②溶液中的 向
向___________ 片移动。(填化学式)
③Cu片上发生反应的电极反应式为___________ 。
④若Fe电极消耗5.6g,则外电路转移___________  。
。
现代社会中,人类的一切活动都离不开能量,化学反应中不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一;
(1)下列反应属于放热反应的是
①碳酸钙高温分解 ②生石灰和水的反应 ③
 在
在 中燃烧
中燃烧(2)如图是原电池的装置图。请回答下列问题:
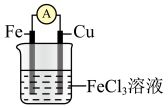
②溶液中的
 向
向③Cu片上发生反应的电极反应式为
④若Fe电极消耗5.6g,则外电路转移
 。
。
您最近一年使用:0次
9 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中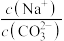
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中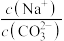
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次
解题方法
10 . 根据所学知识,回答下列问题。
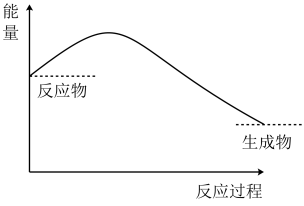
I.锌片与稀硫酸反应的能量变化特征如图所示:___________ 反应(填“吸热”或“放热”)。
(2)锌片和铜片用导线相连后,若将锌片和铜片浸泡在稀硫酸溶液中,可观察到铜片处的现象是___________ 。
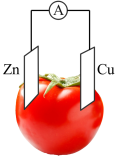
Ⅱ.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
(3)该实验目的是研究水果种类和___________ 对水果电池电流大小的影响。
(4)该实验装置中,正极的材料是___________ ,负极的电极反应式是___________ 。
(5)当有3.25gZn参与反应,转移的电子数目为___________ 。
I.锌片与稀硫酸反应的能量变化特征如图所示:
(2)锌片和铜片用导线相连后,若将锌片和铜片浸泡在稀硫酸溶液中,可观察到铜片处的现象是
Ⅱ.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
| 实验编号 | 水果种类 | 电极间距离/cm | 电流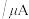 |
|
| 1 | 番茄 | 1 | 98.7 | |
| 2 | 番茄 | 2 | 72.5 | |
| 3 | 苹果 | 2 | 27.2 |
(3)该实验目的是研究水果种类和
(4)该实验装置中,正极的材料是
(5)当有3.25gZn参与反应,转移的电子数目为
您最近一年使用:0次