1 . 放热反应和吸热反应
(1)化学反应中的能量变化
若反应物的能量小于生成物的能量,则反应过程中___________ 能量;若反应物的能量大于生成物的能量,则反应过程中___________ 能量。
下图中,图1表示___________ 反应,图2表示___________ 反应。
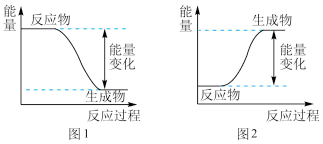
(2)放热反应和吸热反应
___________ 热的反应称为吸热反应,吸热反应的ΔH___________ 0。
___________ 热的反应称为放热反应,反热反应的ΔH___________ 0。
(3)常见的放热反应和吸热反应
根据反应过程中放出或吸收能量,可将化学反应分为放热反应和吸热反应。
常见的放热反应有:①燃烧反应;②中和反应;③金属与水或酸反应放出氢气;④大多数化合反应;⑤铝热反应。
常见的吸热反应有:①大多数分解反应;②需要持续加热的反应;③CO2+C 2CO,C+H2O
2CO,C+H2O CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
(4)放热过程和吸热过程
物质在发生物理变化时,也会放出或吸收能量。
常见的放热过程有:①浓硫酸稀释、NaOH溶于水;②物态变化:气态→液态→固态
常见的吸热过程有:①NH4NO3溶于水;②弱电解质的电离;③物态变化:固态→液态→气体
(1)化学反应中的能量变化
若反应物的能量小于生成物的能量,则反应过程中
下图中,图1表示

(2)放热反应和吸热反应
(3)常见的放热反应和吸热反应
根据反应过程中放出或吸收能量,可将化学反应分为放热反应和吸热反应。
常见的放热反应有:①燃烧反应;②中和反应;③金属与水或酸反应放出氢气;④大多数化合反应;⑤铝热反应。
常见的吸热反应有:①大多数分解反应;②需要持续加热的反应;③CO2+C
 2CO,C+H2O
2CO,C+H2O CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。(4)放热过程和吸热过程
物质在发生物理变化时,也会放出或吸收能量。
常见的放热过程有:①浓硫酸稀释、NaOH溶于水;②物态变化:气态→液态→固态
常见的吸热过程有:①NH4NO3溶于水;②弱电解质的电离;③物态变化:固态→液态→气体
您最近一年使用:0次
解题方法
2 . 完成下列问题
(1)下列反应中,属于放热反应的是___________ ,属于吸热反应的是___________ 。
①Ba(OH)2·8H2O晶体与NH4Cl晶体 ②炸药爆炸 ③生石灰与水作用制熟石灰
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是___________ ,负极的电极反应式是 ___________ 。
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了6.5g,铜表面析出了氢气___________ L(标准状况),导线中通过___________ mol e-。
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为___________ 热反应,中和反应都是___________ 热反应,其实质是___________ (用离子方程式表示)。
(1)下列反应中,属于放热反应的是
①Ba(OH)2·8H2O晶体与NH4Cl晶体 ②炸药爆炸 ③生石灰与水作用制熟石灰
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了6.5g,铜表面析出了氢气
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为
您最近一年使用:0次
名校
3 . CO是重要化工原料和清洁能源。
I.
(1)CO(g)+NO2(g) ⇌ CO2(g)+NO(g)改变下列条件,反应速率增大的是_______
(2)一定温度下,在2L恒容密闭容器中投入x mol CO(g)和x mol NO2(g),发生上述反应,经过t min达到平衡,CO的转化率为a。
①下列情况表明上述反应达到平衡状态的是_______
A.混合气体的密度保持不变 B.混合气体的摩尔质量保持不变
C.气体总压强保持不变 D.NO的消耗速率等于CO的消耗速率
②0-t min间CO的平均速率v(CO)=_______________
Ⅱ.CO是一种清洁能源。
(3)CO空气碱性燃料电池能量转化率高,电池反应为2CO+O2+4KOH=2K2CO3+2H2O。在_______ (填“正”或“负”)极区通入空气,写出负极反应式:________________ 。
Ⅲ.CO 是一种常用的化工原料。
(4)工业上利用CO和H2制备甲醇: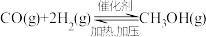
已知该反应为放热反应。下列图像符合上述反应中能量变化的是______ (填“甲”或“乙”)

I.
(1)CO(g)+NO2(g) ⇌ CO2(g)+NO(g)改变下列条件,反应速率增大的是_______
| A.降温 | B.缩小体积 | C.加入催化剂 | D.减压 |
①下列情况表明上述反应达到平衡状态的是
A.混合气体的密度保持不变 B.混合气体的摩尔质量保持不变
C.气体总压强保持不变 D.NO的消耗速率等于CO的消耗速率
②0-t min间CO的平均速率v(CO)=
Ⅱ.CO是一种清洁能源。
(3)CO空气碱性燃料电池能量转化率高,电池反应为2CO+O2+4KOH=2K2CO3+2H2O。在
Ⅲ.CO 是一种常用的化工原料。
(4)工业上利用CO和H2制备甲醇:
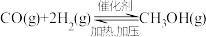
已知该反应为放热反应。下列图像符合上述反应中能量变化的是

您最近一年使用:0次
4 . 从微观角度理解反应热的实质
以H2(g)+Cl2(g)=2HCl(g)反应的能量变化为例说明,如图所示:
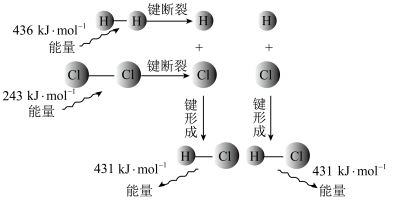
由图可知:
①图示:化学反应过程中形成化学键、断裂化学键能量变化可用如图表示:

其中,_____ 表示反应物断裂化学键吸收的总热量,_____ 表示生成物形成化学键放出的总热量,E1与E2的差值表示_____ 。上述反应过程表示该反应为_____ 反应。
②焓变计算公式:ΔH=E总(断键)-E总(成键)
以H2(g)+Cl2(g)=2HCl(g)反应的能量变化为例说明,如图所示:

由图可知:
| 化学键 | 反应中能量变化 | |
| 断裂或形成1mol化学键的能量变化 | 断裂或形成化学键的总能量变化 | |
| H—H | 吸收 | 共吸收 |
| Cl—Cl | 吸收 | |
| H—Cl | 放出 | 共放出 |
| 结论 | H2(g)+Cl2(g)=2HCl(g)的反应热ΔH= | |

其中,
②焓变计算公式:ΔH=E总(断键)-E总(成键)
您最近一年使用:0次
名校
解题方法
5 . 氢气是未来最理想的能源之一,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O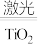 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)氢气用于燃料电池时,实现________ 能转化为________ 能。水分解时,断裂的化学键为________ 键,分解海水的反应属于_______ (填“放热”或“吸热”)反应。
(2)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪声、高效率的特点。如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。

①输入氢气的一极为________ 极。
②写出正极反应式:________ 。
③若将此燃料电池改为以甲烷和氧气为原料时,负极反应式为_______ 。
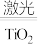 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:(1)氢气用于燃料电池时,实现
(2)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪声、高效率的特点。如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。

①输入氢气的一极为
②写出正极反应式:
③若将此燃料电池改为以甲烷和氧气为原料时,负极反应式为
您最近一年使用:0次
2023-06-27更新
|
65次组卷
|
2卷引用:河南省栾川县第一高级中学2022-2023学年高一下学期6月阶段测试化学试题
名校
6 . 按要求回答下列问题:
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气
⑤甲烷在氧气中的燃烧反应 ⑥NaHCO3与盐酸的反应
(2)反应C(s)+H2O(g) CO(g)+H2(g)在一个密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是___________ 。
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
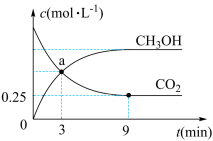
从3min到9min,v(CO2)=___________ (结果保留两位有效数字);
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。
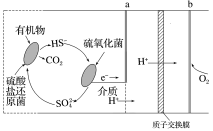
①该电池正极电极反应式为___________ 。
②当电路中有0.5mol电子发生转移,则有___________ mol的H+通过质子交换膜。
(5)H2O2在 催化下可发生分解反应,为探究一定温度下H2O2溶液的浓度、
催化下可发生分解反应,为探究一定温度下H2O2溶液的浓度、 的浓度对H2O2分解速率的影响情况,某同学设计了如下实验,内容见下表:
的浓度对H2O2分解速率的影响情况,某同学设计了如下实验,内容见下表:
①
___________ 。
②实验Ⅰ、Ⅲ相比,若实验Ⅲ中产生气泡的速率较快,由此可得出的结论是___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气
⑤甲烷在氧气中的燃烧反应 ⑥NaHCO3与盐酸的反应
(2)反应C(s)+H2O(g)
 CO(g)+H2(g)在一个密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
从3min到9min,v(CO2)=
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。

①该电池正极电极反应式为
②当电路中有0.5mol电子发生转移,则有
(5)H2O2在
 催化下可发生分解反应,为探究一定温度下H2O2溶液的浓度、
催化下可发生分解反应,为探究一定温度下H2O2溶液的浓度、 的浓度对H2O2分解速率的影响情况,某同学设计了如下实验,内容见下表:
的浓度对H2O2分解速率的影响情况,某同学设计了如下实验,内容见下表:| 实验序号 | 实验所用试剂 | ||||
酸性 溶液 溶液 | H2O2溶液 |  | |||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | |
| Ⅰ | 4 | 0.1 | 3 | 2 | 3 |
| Ⅱ | 4 | 0.1 | 2 | 2 | V1 |
| Ⅲ | 5 | 0.1 | V2 | 2 | 2 |

②实验Ⅰ、Ⅲ相比,若实验Ⅲ中产生气泡的速率较快,由此可得出的结论是
您最近一年使用:0次
解题方法
7 . 氮氧化物(NOx)是硝酸工业和汽车尾气产生的主要污染物之一,通过气体传感器可以测定其含量。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g) N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是_________ (填“放热反应”或“吸热反应”),反应中断开反应物中化学键吸收的总能量_________ (填“大于”或“小于”)形成生成物中化学键放出的总能量。

(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=_________ 。
②该条件下,NO的平衡转化率为_________ 。
③下列有关上述反应的说法正确的是_________ (填字母)。
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。
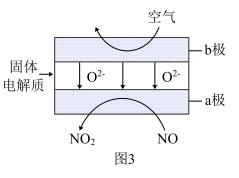
①a极是_________ (填“负极”或“正极”),发生的是_________ 反应(填“氧化”或“还原”)。
②工作时,a极的电极反应式是_________ 。
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是_________ 。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g)
 N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=
②该条件下,NO的平衡转化率为
③下列有关上述反应的说法正确的是
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。

①a极是
②工作时,a极的电极反应式是
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是
您最近一年使用:0次
名校
8 . 完成下列问题。
(1)已知H2与N2反应放热,相关物质键焓见下表。下列关系一定正确的是______。
(2)在下图中面出25℃时化合生成1mol 的能量变化
的能量变化__________ 。
(1)已知H2与N2反应放热,相关物质键焓见下表。下列关系一定正确的是______。
| 化学键 |  |  |  |
键焓 |  |  |  |
A.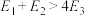 | B.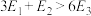 |
C.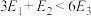 | D.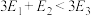 |
 的能量变化
的能量变化
您最近一年使用:0次
9 . 等质量的固体硫和硫蒸气完全燃烧,放出热量校多的是______ (选填“A:固体硫” 或“B:硫蒸气”)
您最近一年使用:0次
名校
10 . I.化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是_______ (填序号)。
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合 d.氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸与碳酸氢钠反应 f.铝和氧化铁高温下反应 g.灼热的木炭中通入 h.碘升华 i.石灰石受热分解 j.水蒸气液化 k.过氧化钠溶于水
h.碘升华 i.石灰石受热分解 j.水蒸气液化 k.过氧化钠溶于水
(2)下列图像分别表示有关反应的反应过程与能量变化的关系:
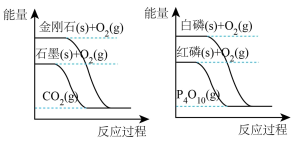
据此判断下列说法中正确的是_______ (填序号)。
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.在一定条件下,石墨转化为金刚石为吸热反应
c.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
d.白磷与氧气反应,断开化学键所吸收的热量大于形成新的化学键所释放的能量
f.红磷的能量高于 的能量
的能量
Ⅱ.碳是一种常见元素,它以多种形式广泛存在于大气、地壳和生物之中。请回答:
(3)碳元素在元素周期表中的位置为_______ ,大气中存在温室气体 ,写出
,写出 的电子式
的电子式_______ 。
(4)工业上可利用焦炭制粗硅,写出该反应的化学方程式_______ ,该反应_______ (填“能”或“不能”)说明碳的非金属性大于硅。
Ⅲ.将等物质的量的气体A、B混合于2L的密闭容器中,发生如下反应: ,5min后,测得D的浓度为
,5min后,测得D的浓度为 ,
,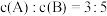 ,C的平均反应速率为
,C的平均反应速率为 。回答下列问题:
。回答下列问题:
(5)此时A的浓度: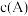 =
=_______  。
。
(6)B的平均反应速率: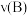 =
=_______  。
。
(7)x的值为_______ 。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合 d.氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸与碳酸氢钠反应 f.铝和氧化铁高温下反应 g.灼热的木炭中通入
 h.碘升华 i.石灰石受热分解 j.水蒸气液化 k.过氧化钠溶于水
h.碘升华 i.石灰石受热分解 j.水蒸气液化 k.过氧化钠溶于水(2)下列图像分别表示有关反应的反应过程与能量变化的关系:

据此判断下列说法中正确的是
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.在一定条件下,石墨转化为金刚石为吸热反应
c.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
d.白磷与氧气反应,断开化学键所吸收的热量大于形成新的化学键所释放的能量
f.红磷的能量高于
 的能量
的能量Ⅱ.碳是一种常见元素,它以多种形式广泛存在于大气、地壳和生物之中。请回答:
(3)碳元素在元素周期表中的位置为
 ,写出
,写出 的电子式
的电子式(4)工业上可利用焦炭制粗硅,写出该反应的化学方程式
Ⅲ.将等物质的量的气体A、B混合于2L的密闭容器中,发生如下反应:
 ,5min后,测得D的浓度为
,5min后,测得D的浓度为 ,
,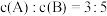 ,C的平均反应速率为
,C的平均反应速率为 。回答下列问题:
。回答下列问题:(5)此时A的浓度:
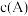 =
= 。
。(6)B的平均反应速率:
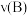 =
= 。
。(7)x的值为
您最近一年使用:0次



