化学反应中会伴随放热和吸热的现象,请回答下列问题:
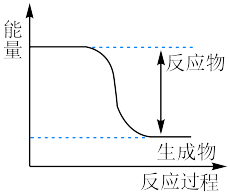
在人体内,O2与葡萄糖反应生成H2O和CO2的能量变化如图所示:___________ (填“放热”或“吸热”)反应,断开氧气分子中的化学键会___________ (填“放出”或“吸收”)能量,形成H-O键会___________ (填“放出”或“吸收”)能量,反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物的总能量。
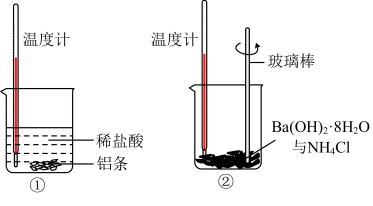
(2)某同学进行如下实验,研究化学反应中的热量变化。___________ (填“放热”或“吸热”)反应,Ba(OH)2·8H2O与NH4Cl的反应是___________ (填“放热”或“吸热”)反应。
(3)①中反应的离子方程式为___________ ,该反应的还原剂是___________ (填化学式)。
在人体内,O2与葡萄糖反应生成H2O和CO2的能量变化如图所示:
(2)某同学进行如下实验,研究化学反应中的热量变化。
(3)①中反应的离子方程式为
更新时间:2024-05-05 22:04:34
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】把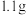 铁、铝混合物溶于
铁、铝混合物溶于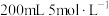 盐酸中,反应后溶液中
盐酸中,反应后溶液中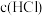 变为
变为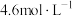 (溶液体积变化忽略不计)。求:
(溶液体积变化忽略不计)。求:
(1)反应中消耗 的物质的量为
的物质的量为___________ ;
(2)该混合物中铁的物质的量为___________ 。
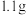 铁、铝混合物溶于
铁、铝混合物溶于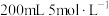 盐酸中,反应后溶液中
盐酸中,反应后溶液中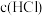 变为
变为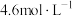 (溶液体积变化忽略不计)。求:
(溶液体积变化忽略不计)。求:(1)反应中消耗
 的物质的量为
的物质的量为(2)该混合物中铁的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】金属及其化合物在人类生活、生产中发挥着重要的作用.
(1)铁是人类应用最广的金属,工业上用铁矿石(主要成分为Fe2O3 )、焦炭、石灰石在高炉中冶炼得到,高炉炼铁的主要化学反应方程式为__________________ ,其中石灰石的作用是____________________ 。
(2)铝是常见的金属,铝制容器既不能存放酸性物质,也不能存放碱性物质,其原因分别用离子方程式表示:_____________ 、 _____________ 。
(1)铁是人类应用最广的金属,工业上用铁矿石(主要成分为Fe2O3 )、焦炭、石灰石在高炉中冶炼得到,高炉炼铁的主要化学反应方程式为
(2)铝是常见的金属,铝制容器既不能存放酸性物质,也不能存放碱性物质,其原因分别用离子方程式表示:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】有些盐的结晶水合物,白天在温度不太高时就能熔化(实质是溶于自身的结晶水中),同时吸收热量;在晚上又可缓慢凝固而释放热量,用以调节室温,称为潜热材料。现有几种盐的水合晶体有关数据如下
(1)上述四种水合晶体盐中最适宜用做潜热材料的两种盐是(用化学式表示)____________________________ ;______________________________ 。
(2)实际应用时最常采用的(由来源和成本考虑)应该是________________________ 。
| Na2S2O3·5H2O | CaCl2·6H2O | Na2SO4·10H2O | Na2HPO4·12H2O | |
| 熔点(℃) | 40.50 | 29.92 | 32.38 | 35.1 |
| 熔化热(kJ/mol) | 49.7 | 37.3 | 77 | 100.1 |
(1)上述四种水合晶体盐中最适宜用做潜热材料的两种盐是(用化学式表示)
(2)实际应用时最常采用的(由来源和成本考虑)应该是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
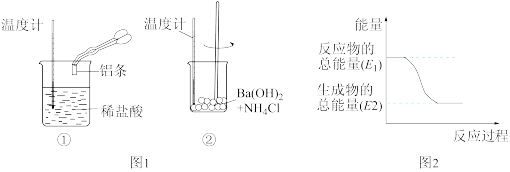
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是_______ 热反应,Ba(OH)2·8H2O与NH4Cl的反应是_______ 热反应。反应过程_______ (填“①”或“②”)的能量变化可用图2表示。
(2)已知:断裂1molH-H、1molO=O,1molH-O键吸收的能量依次为436kJ、498kJ、467kJ。在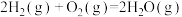 反应中,44.8L
反应中,44.8L (标准状况)完全反应放出的能量为
(标准状况)完全反应放出的能量为_______ 。

(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
(2)已知:断裂1molH-H、1molO=O,1molH-O键吸收的能量依次为436kJ、498kJ、467kJ。在
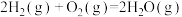 反应中,44.8L
反应中,44.8L (标准状况)完全反应放出的能量为
(标准状况)完全反应放出的能量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】判断吸热反应与放热反应
(1)下列变化:
①铝片与稀盐酸的反应;②Ba(OH)2·8H2O晶体与NH4Cl晶体混合反应;③浓硫酸溶于水;④氯酸钾分解制氧气;⑤生石灰与水反应生成熟石灰;⑥H2在Cl2中燃烧。属于吸热反应的是___________ (填序号),属于放热反应的是___________ (填序号)。
(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
(1)下列变化:
①铝片与稀盐酸的反应;②Ba(OH)2·8H2O晶体与NH4Cl晶体混合反应;③浓硫酸溶于水;④氯酸钾分解制氧气;⑤生石灰与水反应生成熟石灰;⑥H2在Cl2中燃烧。属于吸热反应的是
(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
A.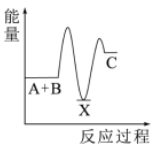 | B.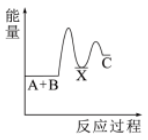 | C.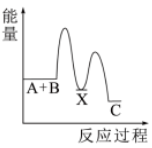 | D.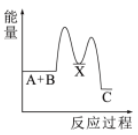 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。

(1)HCOOD催化释氢反应除生成CO2外,还生成__ (填化学式)。
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是__ 。

(1)HCOOD催化释氢反应除生成CO2外,还生成
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知氮化硅陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:3SiO2+6C+2N2 Si3N4+6CO。该反应过程中的能量变化如图所示:
Si3N4+6CO。该反应过程中的能量变化如图所示:
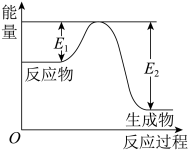
(1)该反应是_______ (填“吸热反应”或“放热反应”),ΔH_______ (填“>” “<”或“=”)0。
(2)该反应过程中,断裂旧化学键吸收的总能量_______ (填“>”“<”或“=”)形成新化学键释放的总能量。
(3)据题意判断N2与CO物质具有的能量大小关系_______ (填“大于”“小于”或“无法比较”)。
 Si3N4+6CO。该反应过程中的能量变化如图所示:
Si3N4+6CO。该反应过程中的能量变化如图所示:
(1)该反应是
(2)该反应过程中,断裂旧化学键吸收的总能量
(3)据题意判断N2与CO物质具有的能量大小关系
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应的过程不仅包括物质变化,还包括能量变化。研究化学能与其他形式能量之间的转化具有重要意义。
I.化学能转化为热能
(1)氢气在氯气中燃烧时产生苍白色火焰,并释放大量的热。若破坏1molH2中的化学键吸收的能量为Q1 kJ,破坏1mol Cl2中的化学键吸收的能量为O2 kJ,形成1mol HCl中的化学键释放的能量为Q3 kJ。则由H2和Cl2反应生成1mol HCl时,释放的能量为______ kJ(用含Q1、Q2、Q3的代数式表示)。
Ⅱ.化学能转化为电能
原电池是将化学能转化为电能的装置,其构成要素可用图1来表示:

(2)氢氧燃料电池(如图2)中,正极材料和负极材料均可选用______ ;正极的电极反应式为______ ;电池工作时,溶液中的OH—移向______ 极(填“正”或“负”)。
(3)如果将反应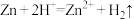 设计成原电池,则负极材料为
设计成原电池,则负极材料为______ (填化学式,下同)正极反应产物为______ ;离子导体为______ 。
(4)如果以Mg、Al为电极材料,NaOH溶液为离子导体,设计成原电池,则Al电极上的电极反应式为______ 。
I.化学能转化为热能
(1)氢气在氯气中燃烧时产生苍白色火焰,并释放大量的热。若破坏1molH2中的化学键吸收的能量为Q1 kJ,破坏1mol Cl2中的化学键吸收的能量为O2 kJ,形成1mol HCl中的化学键释放的能量为Q3 kJ。则由H2和Cl2反应生成1mol HCl时,释放的能量为
Ⅱ.化学能转化为电能
原电池是将化学能转化为电能的装置,其构成要素可用图1来表示:

(2)氢氧燃料电池(如图2)中,正极材料和负极材料均可选用
(3)如果将反应
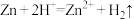 设计成原电池,则负极材料为
设计成原电池,则负极材料为(4)如果以Mg、Al为电极材料,NaOH溶液为离子导体,设计成原电池,则Al电极上的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有反应①Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑②Fe+H2SO4=FeSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是___________ (填序号,下同),能设计成原电池的是___________ 。
(2)铁铜原电池的装置如图所示。
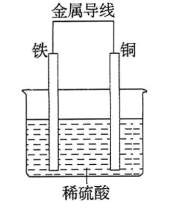
①铁作___________ (填“正极”或“负极”),溶液中的H+向___________ (填“铁”或“铜”)电极方向移动。
②正极的现象是___________ 。负极的电极方程式为___________ 。
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为___________ L。
(1)两反应中属于吸热反应的是
(2)铁铜原电池的装置如图所示。

①铁作
②正极的现象是
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)某反应过程的能量变化如图所示。请填写下列空白。
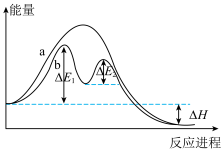
反应过程___________ (填“a”或“b”)有催化剂参与。该反应为___________ 反应(填“放热”或“吸热”),反应热为___________ 。
(2)写出热化学方程式: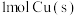 与适量
与适量 反应生成
反应生成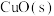 ,放出157.3kJ的热量:
,放出157.3kJ的热量:___________ 。
(3)温度对化学平衡移动的影响如图所示。
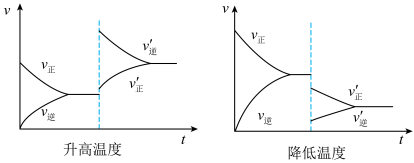
升高温度,平衡向___________ 反应方向移动;降低温度,平衡向___________ 反应方向移动。
(1)某反应过程的能量变化如图所示。请填写下列空白。

反应过程
(2)写出热化学方程式:
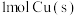 与适量
与适量 反应生成
反应生成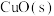 ,放出157.3kJ的热量:
,放出157.3kJ的热量:(3)温度对化学平衡移动的影响如图所示。

升高温度,平衡向
您最近一年使用:0次

 反应过程的能量变化如图所示:
反应过程的能量变化如图所示: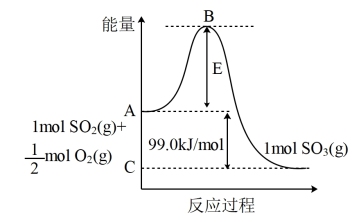
 为
为
 ,请根据题给条件求出反应
,请根据题给条件求出反应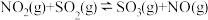 的焓变
的焓变


