1 . 苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
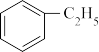 (g)
(g)
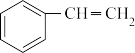 (g)+H2(g) ΔH
(g)+H2(g) ΔH
(1)已知部分物质的燃烧热数据如下表:
则
_______ 。
(2)下列关于反应的说法正确的是_______(填序号)
(3)工业装置通常采用铁基氧化物催化剂,通入过热水蒸气(615~645℃)、水油比(水与乙苯质量比)1.4~1.8、常压的条件下发生乙苯的催化脱氢反应。
①反应中通入水蒸气的作用是_______ 。
②将物质的量分数组成为m%乙苯(g)、n% 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为_______ ,平衡常数
_______ (以分压表示,分压=总压×物质的量分数)
(4)近年来,有研究者发现若将上述生产过程中通入 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯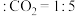 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
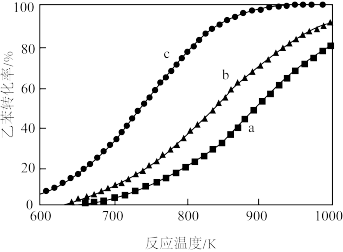
则乙苯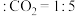 对应的曲线为
对应的曲线为_______ (填“a”,“b”或“c”),理由是_______ 。
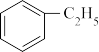 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH(1)已知部分物质的燃烧热数据如下表:
| 物质 | 乙苯 | 苯乙烯 | 氢气 |
燃烧热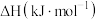 | -4610.2 | -4441.8 | -285.8 |

(2)下列关于反应的说法正确的是_______(填序号)
| A.高温有利于反应自发进行 |
| B.工业生产中应尽可能提高反应温度,并增大压强,以提高原料的利用率 |
| C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大 |
| D.选择合适的催化剂可以缩短达到平衡的时间,但不会提高生成物中苯乙烯的含量 |
①反应中通入水蒸气的作用是
②将物质的量分数组成为m%乙苯(g)、n%
 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为
(4)近年来,有研究者发现若将上述生产过程中通入
 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯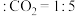 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
则乙苯
 对应的曲线为
对应的曲线为
您最近半年使用:0次
名校
解题方法
2 . 化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫作反应热。由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)下列∆H表示物质燃烧热的是_______ ;不能表示物质中和热的是_______ 。(填字母)
A.H2(g)+ O2(g)=2H2O(g) ∆H1
O2(g)=2H2O(g) ∆H1
B.C(s)+ O2(g)=CO(g) ∆H2
O2(g)=CO(g) ∆H2
C.CH4(g)+2O2g)=CO2(g)+2H2O(l) ∆H3
D.C(s)+O2(g)=CO2(g) ∆H4
E.C6H12O6(s)+3O2(g)=6CO(g)+6H2O(1) ∆H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ∆H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ∆H7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ∆H8
(2)2.00 g C2H2气体完全燃烧生成液态水和CO2气体,放出99.8kJ的热量,写出该反应燃烧热的热化学方程式:_______
(3)充分燃烧一定量的丁烷放出的热量为Q,生成的CO2恰好与100mL浓度为4mol∙L-1的KOH溶液完全反应生成正盐。则燃烧lmol丁烷放出的热量为_______ 。
(4)4.4g丙烷完全燃烧生成的CO2与100 mL浓度为4mol∙L-1的KOH溶液恰好完全反应,则反应后的溶液中酸式盐的物质的量是_______ mol
(5)氢能源有可能实现能源的贮存,也有可能实现经济,高效的输送。研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如,LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.65、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附840体积的氢气(钯粉的密度为10.64g∙cm-3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式_____ 。
(1)下列∆H表示物质燃烧热的是
A.H2(g)+
 O2(g)=2H2O(g) ∆H1
O2(g)=2H2O(g) ∆H1 B.C(s)+
 O2(g)=CO(g) ∆H2
O2(g)=CO(g) ∆H2C.CH4(g)+2O2g)=CO2(g)+2H2O(l) ∆H3
D.C(s)+O2(g)=CO2(g) ∆H4
E.C6H12O6(s)+3O2(g)=6CO(g)+6H2O(1) ∆H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ∆H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ∆H7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ∆H8
(2)2.00 g C2H2气体完全燃烧生成液态水和CO2气体,放出99.8kJ的热量,写出该反应燃烧热的热化学方程式:
(3)充分燃烧一定量的丁烷放出的热量为Q,生成的CO2恰好与100mL浓度为4mol∙L-1的KOH溶液完全反应生成正盐。则燃烧lmol丁烷放出的热量为
(4)4.4g丙烷完全燃烧生成的CO2与100 mL浓度为4mol∙L-1的KOH溶液恰好完全反应,则反应后的溶液中酸式盐的物质的量是
(5)氢能源有可能实现能源的贮存,也有可能实现经济,高效的输送。研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如,LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.65、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附840体积的氢气(钯粉的密度为10.64g∙cm-3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式
您最近半年使用:0次
名校
3 . 我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下获得较高反应速率,反应过程如图:
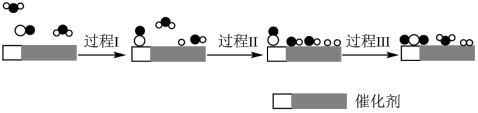
| A.若已知CO和H2的标准燃烧热,由此可推算出该反应的ΔH |
| B.过程Ⅰ、过程Ⅱ均为吸热过程,且吸收的热量相等 |
| C.在该反应过程中,实际有两个H2O参与反应,断裂了三个氢氧键 |
| D.使用催化剂降低了水煤气变换反应的ΔH,提高了反应速率 |
您最近半年使用:0次
2020-05-07更新
|
480次组卷
|
2卷引用:浙江省台州市2020届高三4月教学质量评估化学试题



